Міжнародні настанови з визначення, класифікації, діагностики та лікування кропив’янки
Переклала й адаптувала канд. мед. наук Ольга Королюк
Міжнародні настанови 2026 року є оновленням настанов EAACI/GA2LEN/EuroGuiDerm/APAAACI 2022 року щодо кропив’янки. Рекомендації створено з ініціативи Глобальної мережі передового досвіду в галузі алергії й астми (GA2LEN), Центрів довідкової роботи та передового досвіду з кропив’янки й ангіоневротичного набряку (UCARe, ACARE), Європейського дерматологічного форуму (EDF), Азійсько-Тихоокеанської асоціації алергії, астми та клінічної імунології (APAAACI), Американської академії дерматології (AAD), Британського товариства алергії та клінічної імунології (BSACI) й Академії алергії та клінічної імунології країн Перської затоки (GA2CI). До робочої групи увійшли 213 експертів з 59 країн; їх підтримувала команда методологів EuroGuiDerm з урахуванням думки учасників гібридної консенсусної конференції, що відбулася 6 грудня 2024 року в Берліні, Німеччина. Мета настанов – надати визначення та класифікації кропив’янки для полегшення інтерпретації даних з різних центрів і регіонів світу щодо основних причин, тригерів, супутніх захворювань, впливів на пацієнтів і суспільство, а також терапевтичної чутливості підтипів кропив’янки. Рекомендації стосовно діагностики та лікування поширених підтипів кропив’янки сформульовано за стандартизованою системою (табл. 1) з огляду на різноманітність пацієнтів, лікарів, медичних систем і доступу до діагностики та лікування. 
Визначення
Кропив’янка – стан, що характеризується появою уртикарного висипу (пухирів), ангіоневротичного набряку (АН) або їх поєднанням. Кропив’янку потрібно диференціювати з низкою схожих за проявами клінічних станів, як-от анафілаксія, автоімунні синдроми, уртикарний васкуліт, АН, індукований брадикініном, спадковий АН (САН).
- Висип (пухирі) має три типові ознаки:
- чітко окреслений поверхневий центральний набряк змінної форми та розміру, майже завжди оточений рефлекторною еритемою;
- відчуття свербіння, іноді печіння;
- швидкоплинність: нормалізація стану шкіри протягом 30 хвилин – 24 годин.
- АН характеризується:
- раптовим вираженим глибоким набряком нижніх шарів дерми, підшкірної клітковини чи слизових оболонок тілесного кольору або з почервонінням;
- відчуттям поколювання, печіння, стискання, іноді болю, але не свербіння;
- повільнішим зникненням порівняно з висипом (до 72 годин).
Класифікація кропив’янки за тривалістю та значенням провокувальних чинників
Спектр клінічних проявів кропив’янки дуже широкий. В одного пацієнта можуть співіснувати ≥2 різних підтипів кропив’янки. Класифікація кропив’янки ґрунтується на двох основних критеріях:
- Тривалість: гостра чи хронічна.
- Роль визначених тригерів: індукована чи спонтанна.
- Гостра кропив’янка (ГК) визначається як поява пухирів, АН або їх поєднання протягом ≤6 тижнів.
- За хронічної кропив’янки (ХК) тривалість клінічних проявів становить >6 тижнів. Клінічні симптоми й ознаки можуть бути щоденними, майже щоденними або періодичними.
У разі хронічної спонтанної кропив’янки (ХСК) клінічний перебіг не має визначеного фізичного провокувального чинника. Епізоди ХСК можуть повторюватися після місяців чи навіть років повної ремісії. Індукована кропив’янка характеризується наявністю чітких і специфічних тригерів, що призводять до появи клінічних проявів.
- Тригери є визначеними – симптоми завжди виникають після впливу на індивідуальному пороговому рівні, але ніколи за їх відсутності.
- Тригери є специфічними – кожен підтип індукованої кропив’янки зумовлює певний тригер (наприклад, холод за холодової кропив’янки), який не має значення для інших форм.
Зазвичай симптоми хронічної індукованої кропив’янки (ХІК) з’являються впродовж 10 хвилин після впливу тригера та зникають протягом 1-3 годин після його усунення. Існують рідкісні підтипи ХІК, коли для появи симптомів потрібна комбінація ≥2 специфічних тригерів, наприклад індукована холодом холінергічна кропив’янка. У деяких пацієнтів з ХСК можливе посилення висипу чи АН під дією тригерів (стрес, інфекції). У пацієнтів з різними підтипами кропив’янки кожен з підтипів може по-різному реагувати на лікування.  Класифікація підтипів ХК для клінічного використання (табл. 2) відповідає попередній версії настанов.
Класифікація підтипів ХК для клінічного використання (табл. 2) відповідає попередній версії настанов. 
 Низка клінічних станів (табл. 3) можуть мати схожі клінічні ознаки, але не вважаються типами кропив’янки через принципово відмінні патофізіологічні механізми та/або клінічні прояви.
Низка клінічних станів (табл. 3) можуть мати схожі клінічні ознаки, але не вважаються типами кропив’янки через принципово відмінні патофізіологічні механізми та/або клінічні прояви. 
Патофізіологія
Кропив’янка переважно спричиняється тучними клітинами, але тригери, що їх активують, різні й індивідуальні для кожного пацієнта. Крім гістамінового рецептора, на тучних клітинах задіяні інші рецептори, зокрема споріднений з Мas, з’єднаний із G-білком рецептор з родини Х2 (MRGPRX2). Також до появи ХСК можуть призводити інші типи клітин і медіаторів: Т-клітини (взаємодія через OX40/OX40L або цитокіни), В-клітини (вироблення автоантитіл), еозинофіли (вивільнення агоністів MRGPRX2), нейтрофіли, базофіли, макрофаги, сенсорні нерви (вивільнення нейропептидів) тощо. У понад половини пацієнтів патофізіологія ХСК зумовлена двома основними автоімунними механізмами (I тип – автоалергія за участю автоантитіл IgE проти автоалергенів; IIb тип – за участю автоантитіл IgG), які часто поєднуються. Крім того, в багатьох випадках виявляються ознаки супутніх захворювань, спричинених запаленням 2-го типу. Залишається незрозумілим, скільки саме чинників фактично беруть участь в активації тучних клітин за кропив’янки. Наслідком активації тучних клітин є вивільнення медіаторів (гістамін, фактор активації тромбоцитів), відповідальних за стимуляцію сенсорних нервів (свербіж), розширення судин (еритема) та хемоатракцію запальних клітин. Гістологічними ознаками кропив’янки є дегранульовані тучні клітини, набряк верхніх-середніх шарів дерми, розширення й надмірна проникність посткапілярних венул і лімфатичних судин верхніх шарів дерми. При АН подібні зміни переважають у нижній частині дерми та підшкірному шарі. У ділянках пухирів спостерігається змішаний запальний периваскулярний інфільтрат, що складається з Т-клітин, еозинофілів, нейтрофілів, базофілів, макрофагів. Схожі ознаки можливі при різноманітних запальних станах, тому не є специфічними. Для диференціації різних підтипів кропив’янки важливо знайти специфічніші гістологічні біомаркери. Для уртикарного васкуліту характерним є некроз стінки судин, хоча в деяких випадках ХСК з тривалими пухирями можливе певне перекриття. З’являються докази, що зміни кишкового мікробіому можуть відігравати роль у патофізіології кропив’янки. Дослідження ролі мікробіому та використання пробіотиків може відкрити нові терапевтичні шляхи.
Діагностика
Першим кроком у діагностиці кропив’янки є ретельний збір анамнезу, включно із супутніми хворобами та коморбідністю. Другим кроком є фізичне обстеження пацієнта. Пухирі й АН швидко регресують і на момент огляду часто відсутні; тому важливо переглянути попередню документацію, включно з наданими пацієнтом зображеннями пухирів та/або АН. Третій крок передбачає діагностичне обстеження: обов’язкові тести та розширену діагностичну програму залежно від типу й підтипу кропив’янки (табл. 4). 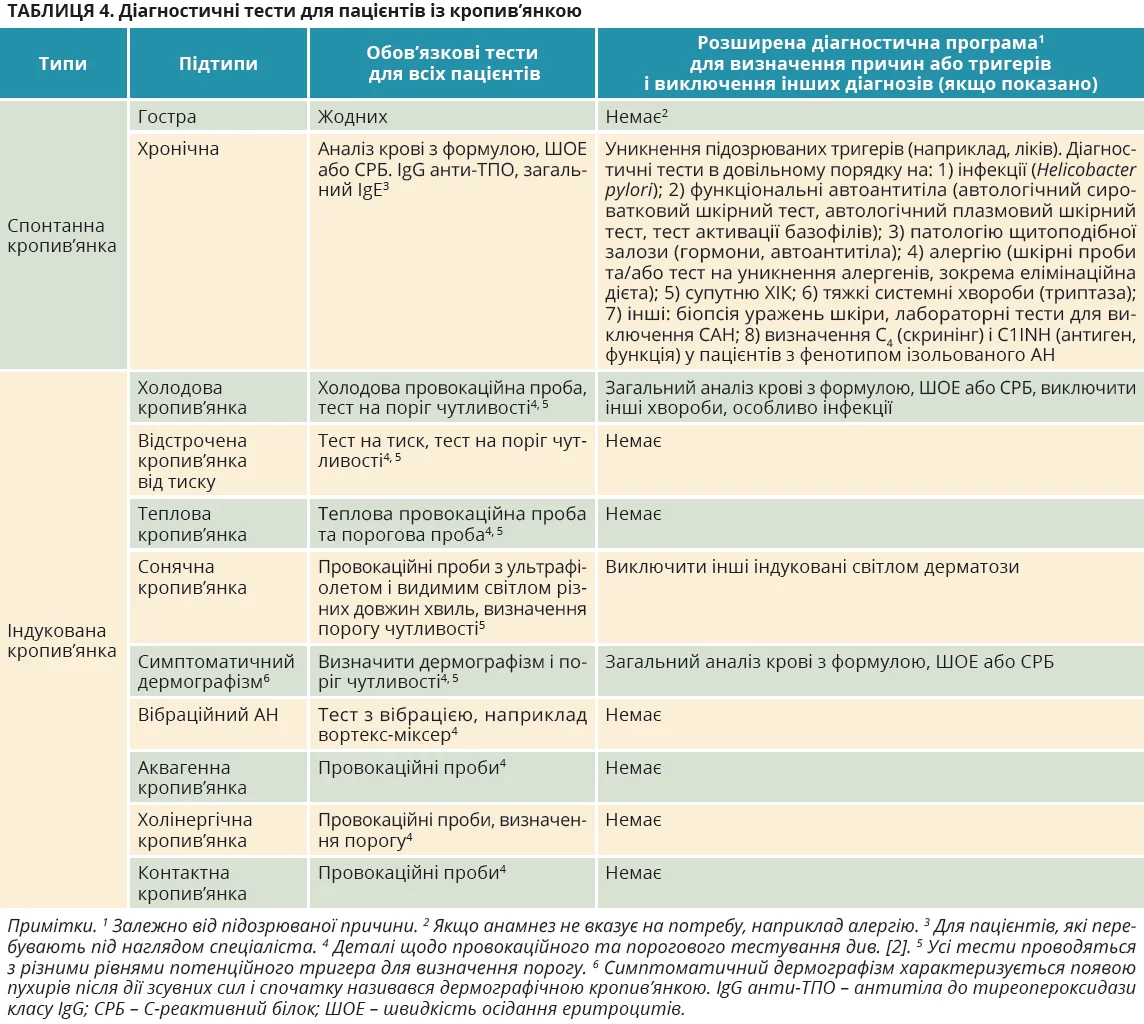 Украй важливо, щоб лікар і пацієнт чітко розуміли цілі всіх діагностичних тестів, шукаючи баланс між потребою проведення тесту та бажанням пацієнта виявити причину. Крім того, ХК є автоімунним станом, тому випадки з позитивними тестами на IgE‑опосередковану харчову алергію радше вказують на коморбідність, аніж на причинний зв’язок із кропив’янкою.
Украй важливо, щоб лікар і пацієнт чітко розуміли цілі всіх діагностичних тестів, шукаючи баланс між потребою проведення тесту та бажанням пацієнта виявити причину. Крім того, ХК є автоімунним станом, тому випадки з позитивними тестами на IgE‑опосередковану харчову алергію радше вказують на коморбідність, аніж на причинний зв’язок із кропив’янкою.
- Діагностичне обстеження при ГК
Завдяки самообмежувальній природі ГК зазвичай не потребує діагностичного обстеження, крім ретельного збору анамнезу для виявлення можливих тригерів. Єдиним винятком є підозра на ГК, спричинену харчовою алергією в сенсибілізованих пацієнтів або лікарською гіперчутливістю, особливо до нестероїдних протизапальних препаратів (НПЗП). У таких випадках алергологічні тести, включно з провокаційними, можуть підтвердити причинний зв’язок між дією тригерів і кропив’янкою, а також знайти безпечні альтернативи або толерантні дози для пацієнтів, які постійно приймають НПЗП через інші медичні стани. Щоб уникнути повторного контакту з тригерами, корисною є освітня робота з пацієнтом. Дуже важливо диференціювати ГК від інших станів, що супроводжуються появою пухирів (наприклад, гострої анафілаксії). 
- Діагностичне обстеження при ХСК
В усіх випадках ХСК діагностика має включати ретельний збір анамнезу, об’єктивне обстеження з оглядом зображень пухирів та/або АН і основні скринінгові тести, а також оцінювання активності й контролю хвороби. Дуже корисно використовувати валідовані шкали, які ґрунтуються на результатах звітів пацієнта, як-от шкала активності кропив’янки протягом 7 днів (UAS7), тест контролю кропив’янки (UCT) тощо. Базові тести охоплюють розгорнутий загальний аналіз крові, рівень СРБ та/або ШОЕ для виключення системних захворювань, паразитарних інвазій, гіпереозинофілії й автоімунних станів, зокрема системного вовчака. У пацієнтів, які перебувають під наглядом спеціаліста, можна провести додаткові тести – загальний IgE, IgG анти-ТПО, що можуть виявитися корисними для прогнозування відповіді на омалізумаб. Подальші діагностичні кроки (табл. 4) залежать від отриманих результатів. Основні цілі діагностичного обстеження підсумовано в таблиці 5. 
Підтвердження ХСК і диференційний діагноз
Диференційний діагноз ХСК визначається даними анамнезу пацієнта та підтверджується відповідними тестами (табл. 4). Поява пухирів або АН можлива в пацієнтів з іншими хворобами (рис. 1). У разі ізольованих пухирів треба виключити уртикарний васкуліт і автозапальні хвороби (синдром Шніцлера, CAPS). У разі рецидивів АН без пухирів диференційний діагноз має включати АН, опосередкований брадикініном: зумовлений інгібіторами ангіотензинперетворювального ферменту (АПФ) або гліптинами, CАН. 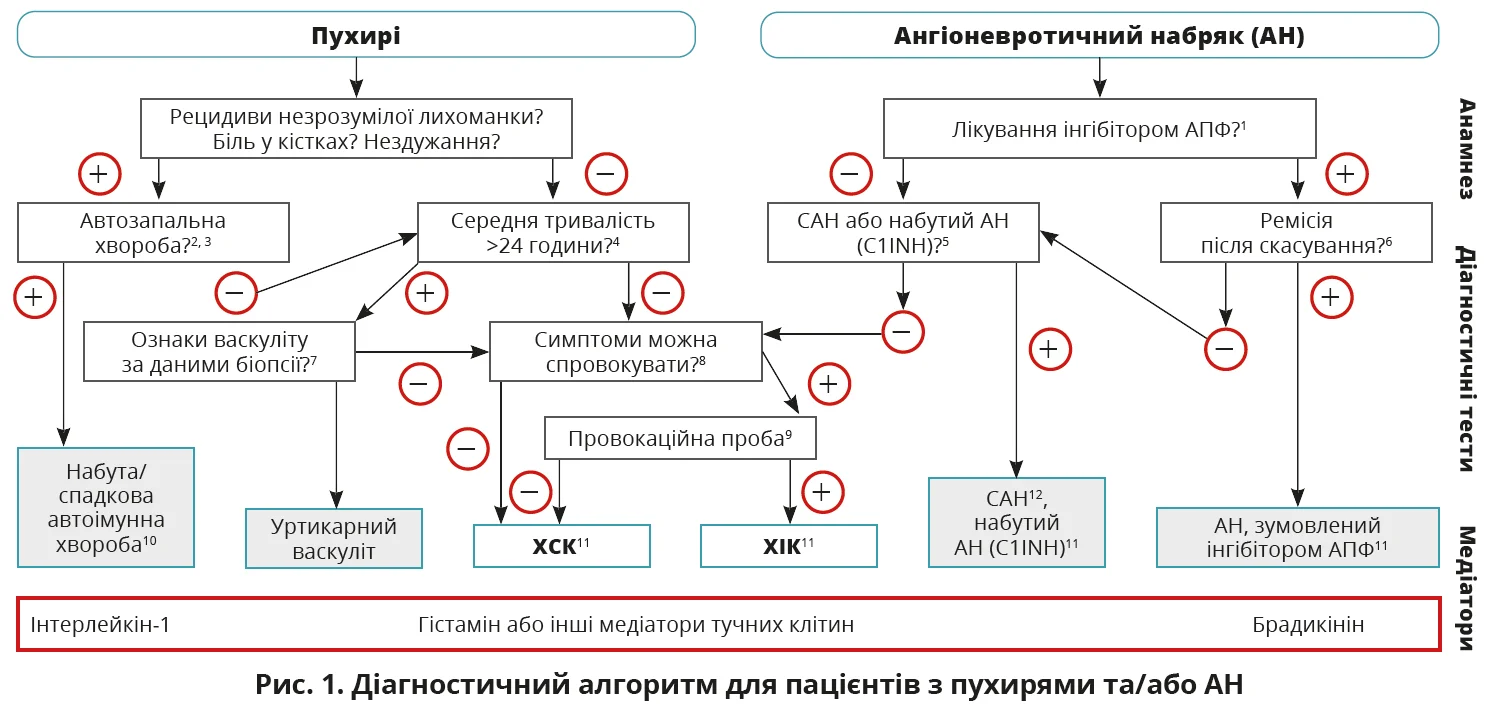 Примітки. C1INH – дефіцит C1-інгібітора. 1 Крім інгібіторів АПФ, блокатори рецепторів ангіотензину II типу 1 (сартани), інгібітори дипептидилпептидази-4 (гліптини) й інгібітори неприлізину можуть спричиняти АН. 2 Слід зібрати докладний сімейний анамнез, з’ясувати вік початку хвороби. 3 Перевірити, чи підвищені маркери запалення (CРБ, ШОЕ), наявність парапротеїнемії в дорослих, шукати ознаки інфільтратів, багатих на нейтрофіли, в біопсії шкіри; виконати аналіз генних мутацій на спадкові періодичні гарячкові синдроми (наприклад, асоційований із кріопірином) за підозри. 4 Пацієнтів слід запитати, як довго триває кожен епізод висипки. 5 Провести тест на рівень і функцію комплементу C4, C1INH; додатково перевірити C1q й антитіла до C1INH, якщо підозрюється набутий АН; виконати аналіз генних мутацій, якщо попередні тести не виявили відхилень, але анамнез свідчить про САН. 6 Ремісія настає впродовж кількох днів, зрідка – до 6 місяців після скасування інгібіторів АПФ. 7 Пошкодження дрібних судин у сосочковому й ретикулярному шарах дерми та/або фібриноїдні відкладення в периваскулярних й інтерстиційних ділянках свідчать про уртикарний васкуліт. 8 Пацієнтів слід запитати, чи можуть вони спровокувати появу пухирів. 9 У пацієнтів з анамнезом, що вказує на ХІК, треба провести стандартизовану провокаційну пробу відповідно до міжнародних консенсусних рекомендацій [3]. 10 Набуті автоімунні синдроми: синдром Шніцлера, системний ювенільний ідіопатичний артрит, хвороба Стілла в дорослих; спадкові автоімунні синдроми включають CAPS – FCAS, MWS, NOMID, рідше синдром гіпер-IgD та періодичний синдром, асоційований з рецептором фактора некрозу пухлин-α. 11 У рідкісних випадках рецидивів АН не опосередкований медіаторами тучних клітин або брадикініном; патомеханізми залишаються невідомими – ідіопатичний АН. 12 Відомо кілька підтипів САН: САН-1 – зумовлений дефіцитом C1-інгібітора; САН-2 – зумовлений дисфункцією C1-інгібітора; САН-nC1INH – САН з нормальним рівнем C1-інгібітора, спричинений мутаціями фактора XII, ангіопоетину-1, плазміногену, кініногену, міоферліну, гепарансульфат-глюкозамін-3-O-сульфотрансферази-6, карбоксипептидази N або невідомими причинами.
Примітки. C1INH – дефіцит C1-інгібітора. 1 Крім інгібіторів АПФ, блокатори рецепторів ангіотензину II типу 1 (сартани), інгібітори дипептидилпептидази-4 (гліптини) й інгібітори неприлізину можуть спричиняти АН. 2 Слід зібрати докладний сімейний анамнез, з’ясувати вік початку хвороби. 3 Перевірити, чи підвищені маркери запалення (CРБ, ШОЕ), наявність парапротеїнемії в дорослих, шукати ознаки інфільтратів, багатих на нейтрофіли, в біопсії шкіри; виконати аналіз генних мутацій на спадкові періодичні гарячкові синдроми (наприклад, асоційований із кріопірином) за підозри. 4 Пацієнтів слід запитати, як довго триває кожен епізод висипки. 5 Провести тест на рівень і функцію комплементу C4, C1INH; додатково перевірити C1q й антитіла до C1INH, якщо підозрюється набутий АН; виконати аналіз генних мутацій, якщо попередні тести не виявили відхилень, але анамнез свідчить про САН. 6 Ремісія настає впродовж кількох днів, зрідка – до 6 місяців після скасування інгібіторів АПФ. 7 Пошкодження дрібних судин у сосочковому й ретикулярному шарах дерми та/або фібриноїдні відкладення в периваскулярних й інтерстиційних ділянках свідчать про уртикарний васкуліт. 8 Пацієнтів слід запитати, чи можуть вони спровокувати появу пухирів. 9 У пацієнтів з анамнезом, що вказує на ХІК, треба провести стандартизовану провокаційну пробу відповідно до міжнародних консенсусних рекомендацій [3]. 10 Набуті автоімунні синдроми: синдром Шніцлера, системний ювенільний ідіопатичний артрит, хвороба Стілла в дорослих; спадкові автоімунні синдроми включають CAPS – FCAS, MWS, NOMID, рідше синдром гіпер-IgD та періодичний синдром, асоційований з рецептором фактора некрозу пухлин-α. 11 У рідкісних випадках рецидивів АН не опосередкований медіаторами тучних клітин або брадикініном; патомеханізми залишаються невідомими – ідіопатичний АН. 12 Відомо кілька підтипів САН: САН-1 – зумовлений дефіцитом C1-інгібітора; САН-2 – зумовлений дисфункцією C1-інгібітора; САН-nC1INH – САН з нормальним рівнем C1-інгібітора, спричинений мутаціями фактора XII, ангіопоетину-1, плазміногену, кініногену, міоферліну, гепарансульфат-глюкозамін-3-O-сульфотрансферази-6, карбоксипептидази N або невідомими причинами.
Виявлення основних причин
Патогенез ХСК ще не повністю вивчений, але добре відомо, що клінічні прояви зумовлені активацією тучних клітин шкіри з подальшим вивільненням і впливом медіаторів. ГК часто виникає після інфекцій верхніх дихальних шляхів, включно з коронавірусною хворобою (COVID-19); деякі випадки переростають у ХСК. Зрідка ХСК можуть спричиняти хронічні безсимптомні інфекції чи злоякісні пухлини. Проте невідомо, як інфекції пов’язані з автоімунітетом I або IIb типу. ХСК з автоімунітетом IIb типу часто асоціюється з підвищеним рівнем СРБ, низькою кількістю еозинофілів і базофілів, низьким або дуже низьким рівнем загального IgE та підвищеним рівнем IgG анти-ТПО.  Хоча клінічний зв’язок між лабораторними маркерами й ендотипами кропив’янки доведено, їхня практична користь обмежена через відсутність досліджень. Порогові значення можна пропонувати, але вони не придатні для остаточної класифікації. Додаткові спеціалізовані методи, як-от тест активації базофілів для ХСК з автоімунітетом IIb типу, можуть надати додаткову інформацію, проте не є рутинними й мають ґрунтуватися на анамнезі, огляді та базових аналізах. До потенційних причин і обтяжливих чинників відносять хвороби щитоподібної залози, інфекції, рак, запалення, їжу й ліки. Загальні інтенсивні та дорогі програми скринінгу не рекомендуються. Поширеність причин може суттєво відрізнятися між регіонами та потребує подальшого вивчення.
Хоча клінічний зв’язок між лабораторними маркерами й ендотипами кропив’янки доведено, їхня практична користь обмежена через відсутність досліджень. Порогові значення можна пропонувати, але вони не придатні для остаточної класифікації. Додаткові спеціалізовані методи, як-от тест активації базофілів для ХСК з автоімунітетом IIb типу, можуть надати додаткову інформацію, проте не є рутинними й мають ґрунтуватися на анамнезі, огляді та базових аналізах. До потенційних причин і обтяжливих чинників відносять хвороби щитоподібної залози, інфекції, рак, запалення, їжу й ліки. Загальні інтенсивні та дорогі програми скринінгу не рекомендуються. Поширеність причин може суттєво відрізнятися між регіонами та потребує подальшого вивчення.
Виявлення відповідних умов, що посилюють активність ХСК
Важливо визначати чинники, які погіршують перебіг ХСК: ліки, їжа, стрес, інфекції тощо. Ліки можуть зумовлювати кропив’янку через як IgE-опосередковані реакції (наприклад, пеніцилін), так й IgE-незалежні механізми (наприклад, НПЗП). Лікарі повинні уточнювати приймання НПЗП і радити уникати їх, якщо реакцію підтверджено; парацетамол та інгібітори циклооксигенази-2 вважаються безпечнішими. За потреби низьких доз аспірину як антитромботичної терапії можливе заміщення іншим препаратом на 4 тижні для перевірки причинності. Рутинне проведення провокаційних тестів з НПЗП не рекомендується, але може виявитися корисним для оцінювання толерантності під час ремісії. Харчова алергія зрідка є тригером ХСК. Вона може співіснувати з кропив’янкою (наприклад, оральний алергічний синдром). Неалергічні реакції на їжу також можуть погіршувати ХСК. В окремих випадках можливе застосування діагностичних дієт (низькопсевдоалергенних, низькогістамінних) протягом 2-3 тижнів, але вони не мають затримувати ефективне лікування. Слід уникати надмірної діагностики «гістамінової непереносимості», щоб не спричиняти необґрунтовані обмеження та зловживання добавками. Стрес також погіршує перебіг ХСК; близько третини пацієнтів вважають його значущим фактором. Лікарі мають запитувати пацієнтів про вплив стресу й інформувати їх про користь заходів для зниження стресу.
Виявлення супутніх захворювань і наслідків ХСК
Найчастішими супутніми станами при ХСК є ХІК, автоімунні хвороби, метаболічний синдром і алергії. Наслідками ХСК є психічні розлади (депресія, тривога), сексуальні дисфункції та порушення сну. Дослідження показують зв’язок ХСК з підвищеною смертністю, особливо через самогубство, ймовірно, через коморбідність. Тому будь-які дані анамнезу, огляду чи базових тестів, що вказують на супутній стан, мають бути підставою для додаткових обстежень (анкетування, провокаційні проби, лабораторні тести, направлення до спеціаліста). Виявлено декілька біомаркерів, що свідчать про коморбідність, зокрема автоімунні стани. Деякі препарати для лікування кропив’янки також впливають на коморбідність (табл. 6). 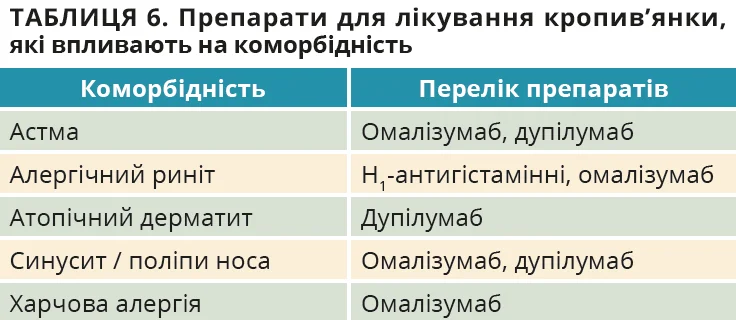
Визначення предикторів перебігу та відповіді на лікування
Тривалість, активність і відповідь ХСК на лікування пов’язані з клінічними характеристиками й лабораторними маркерами. Жоден з них не є точним предиктором, але вони допомагають оцінити тяжкість, імовірну тривалість і очікувані результати терапії. Наприклад, супутня ХІК, висока активність, підвищення СРБ і наявність АН указують на довший перебіг ХСК та гіршу відповідь на Н1-антигістамінні засоби (Н1-АГЗ).
Оцінювання активності, впливу та контролю хвороби
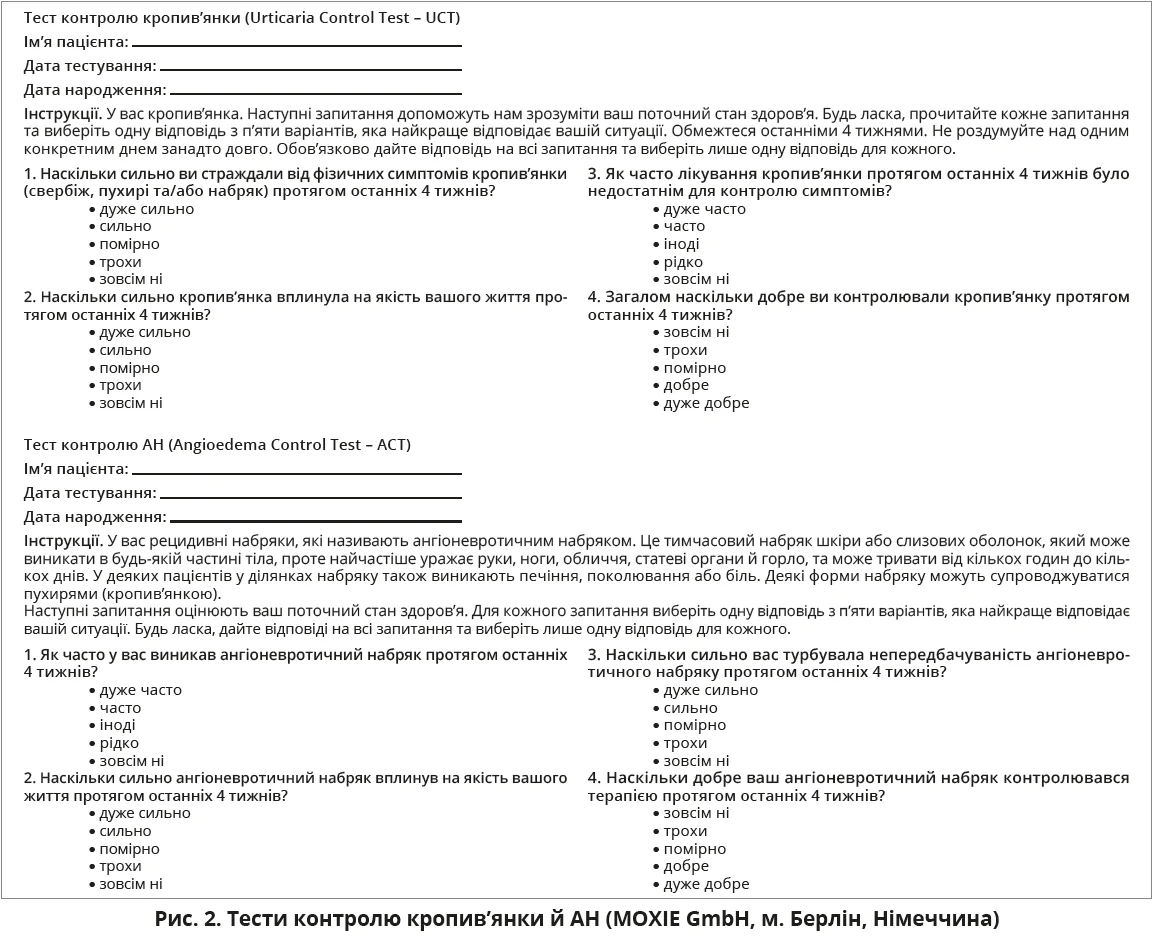
В усіх пацієнтів з ХСК під час кожного візиту слід оцінювати активність, вплив і контроль хвороби за допомогою валідованих інструментів на підставі записів пацієнтів. Шкала UAS7 забезпечує стандартизовану оцінку активності кропив’янки впродовж 7 днів і рекомендована для рутинного використання в дослідженнях і клінічній практиці. Для пацієнтів з ХСК й АН слід додатково застосовувати шкалу AAS (табл. 7). Щоденне ведення пацієнтом UAS/ААS на папері або в застосунку впродовж місяця дає змогу відстежувати коливання та виявляти чинники загострення. Крім активності, слід оцінювати вплив кропив’янки на якість життя, застосовуючи опитувальники CU-Q2oL, коли є пухирі, й AE-QoL, коли є АН. Для оцінювання контролю ХСК та ХІК використовують UCT за наявності пухирів, а також тест контролю АН (AECT) за наявності АН (рис. 2). Це прості інструменти із 4 запитань, які оцінюють симптоми за останні 4 тижні. Пороги для добре контрольованої хвороби – 12 із 16 балів за UCT та 10 балів за AECT. Оцінка допомагає в прийнятті рішень щодо лікування. 
- Діагностичне обстеження при ХІК
Основні завдання: виключити диференційні діагнози, визначити підтип ХІК і встановити пороги тригерів. Для більшості підтипів існують валідовані провокаційні проби: холодова й теплова кропив’янка – пристрій TempTest; симптоматичний дермографізм – дермографометри (Dermographic Tester, FricTest); компресійна кропив’янка – Dermographic Tester; холінергічна кропив’янка – градуйовані тести, наприклад велоергометрія; контактна й аквагенна кропив’янка – відповідні шкірні провокаційні тести. Контроль хвороби оцінюють за порогами провокаційних проб і валідованими інструментами (UCT, AECT). Для кількох підтипів ХІК доступні або розробляються специфічні опитувальники для визначення активності та впливу. 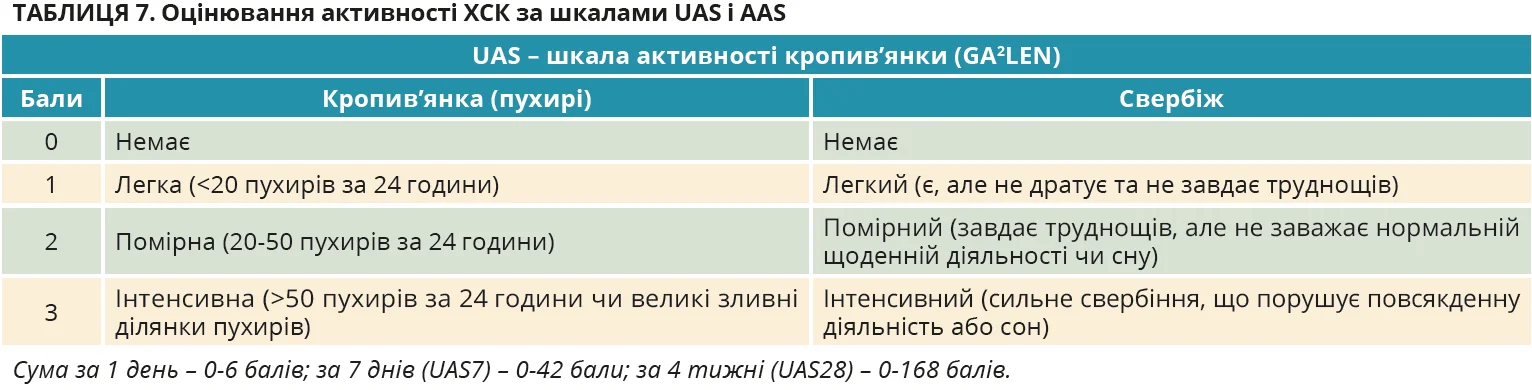

- Діагностика в дітей
Кропив’янка може виникати в будь‑якому віці, навіть у дітей і немовлят. Поширеність ХІК і ХСК, їхні характеристики, причини та відповідь на лікування в дітей подібні до таких у дорослих. Діагностика ХСК у дітей має ті самі завдання: виключення диференційних діагнозів (зокрема, CAPS), визначення тригерів, оцінювання активності, впливу й контролю. Шкали UAS7 та UCT валідовані для дітей, інших специфічних інструментів поки що немає. У дітей з ХІК варто проводити провокаційні тести та визначати пороги тригерів настільки, наскільки це дозволяють вік і співпраця дитини.
Лікування кропив’янки
- Основні положення
- Мета лікування: максимально ефективно й безпечно лікувати до повного зникнення проявів хвороби, досягти постійного контролю (UAS = 0 / UCT = 16) і нормалізації якості життя.
- Підхід передбачає: а) пошук і, якщо змога, усунення причин; б) уникнення провокувальних чинників; в) індукцію толерантності при деяких ХІК; г) фармакотерапію, яка запобігає вивільненню або дії медіаторів тучних клітин.
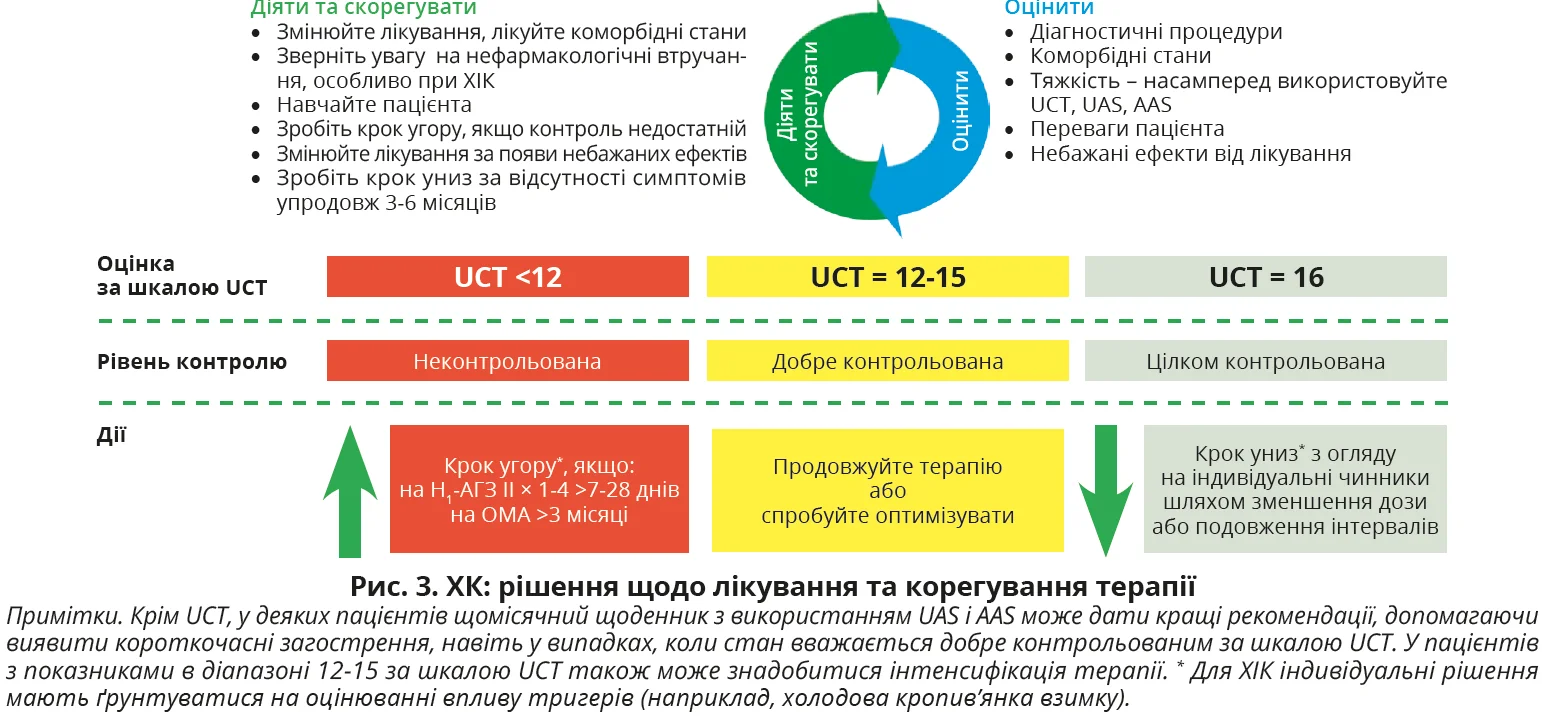
- Лікування має тривати «стільки, скільки потрібно, але якнайменше», зважаючи на активність. Це означає корекцію терапії за принципом: оцінити ® діяти ® скорегувати ® переоцінити (рис. 3).
- Виявлення й усунення причин і уникнення провокувальних чинників
У більшості пацієнтів причини кропив’янки невідомі та не можуть бути усунені. Плазмаферез може давати тимчасовий ефект, але досвід і докази обмежені, а процедура дорога. Уникнення тригерів може бути корисним. Пацієнтам з ХІК слід уникати конкретних провокаторів (наприклад, холод за холодової кропив’янки), а пацієнтам з ХСК – індивідуально значущих неспецифічних чинників (стрес, НПЗП). Важливо зберігати баланс: уникнення тригерів не має суттєво обмежувати якість життя чи соціальну активність (наприклад, повна відмова від фізичних вправ або перебування на сонці не є метою пацієнтоорієнтованої стратегії).
- Лікарські засоби
Слід повністю скасувати або замінити іншими всі ліки, які підозрюються як тригери. Препарати, що спричиняють реакції гіперчутливості (особливо НПЗП), можуть не тільки провокувати, але й погіршувати перебіг ХСК, тому їх усунення лише частково покращує симптоми. 
- Чіткі та специфічні тригери при ХІК
Уникнення або зменшення впливу специфічних тригерів за ХІК може знизити появу пухирів і АН, хоча цього зазвичай недостатньо для контролю хвороби. Пацієнтів слід повідомити, як розпізнавати та мінімізувати контакт із тригерами. Наприклад, у разі відстроченої кропив’янки від тиску пояснити, що тиск – це співвідношення сили до площі; отже, розширення ручки важкої сумки може зменшити симптоми. При холодовій кропив’янці треба уникати впливу холодного вітру, а при сонячній кропив’янці важливо точно визначити діапазон хвиль, що спричиняють реакцію, для правильного вибору сонцезахисних кремів чи ламп з фільтром УФ-A. Проте в багатьох пацієнтів поріг чутливості низький, тому цілковите уникнення симптомів практично неможливе. Зокрема, виражений дермографізм іноді плутають з ХСК, адже навіть вільний одяг чи випадкове чухання можуть спричинити появу пухирів.
- Інфекції та запальні процеси
На відміну від ХІК, ХСК може асоціюватися з різними інфекційними й запальними хворобами та введенням вакцин. Дані досліджень суперечливі та мають методологічні обмеження. Серед інфекційних чинників ХСК варто згадати H. pylori, хворобу Лайма та бактерійні назофарингеальні інфекції. Асоціація інфекції H. pylori з кропив’янкою не завжди очевидна, а ефективність ерадикації низька. Власне, тригером радше є гастрит, а не H. pylori; симптоми кропив’янки зникають лише після належного лікування гастриту. Кишкові паразити, які не часто трапляються в розвинених країнах, також підлягають елімінації за показаннями. Щодо хронічних запальних захворювань, то потенційним тригером ХСК вважаються хронічні гастрити, рефлюкс-езофагіти, запалення жовчних шляхів чи жовчного міхура.
- Зменшення функціональних автоантитіл
Плазмаферез може тимчасово допомогти тяжким пацієнтам, але через високу вартість і обмежений досвід застосовується лише в разі ХСК з позитивними автоантитілами, резистентними до інших методів лікування. Імуносупресивні препарати (наприклад, циклоспорин) можуть знижувати рівень автоантитіл і активованих Т-клітин.
- Їжа
Опосередкована IgE харчова алергія є дуже рідкісною причиною ХСК, але в разі виявлення уникнення алергену сприяє ремісії. У деяких пацієнтів з ХСК спостерігаються псевдоалергічні реакції на природні харчові інгредієнти або добавки. Дієти з низьким умістом псевдоалергенів і гістаміну можуть покращувати симптоми. Їх критикують через відсутність доказів у подвійно сліпих дослідженнях, але всі відкриті дослідження показали користь. Перевагою дієт є відсутність витрат на ліки, проте ефективність залежить від співпраці пацієнта та регіональних харчових звичок.
- Індукція толерантності
Індукція толерантності може бути корисною при деяких підтипах ХІК – холодовій, холінергічній і сонячній. Однак ефект зазвичай нетривалий, тому потрібен щоденний контрольований вплив стимулу на пороговому рівні, що часто не приймається пацієнтами. Наприклад, за холодової кропив’янки для підтримання толерантності потрібні щоденні холодні ванни чи душі.
- Симптоматична фармакотерапія
Мета та потреба тривалого, але корегованого лікування
Основною метою лікування кропив’янки є досягнення цілковитого контролю симптомів із продовженням безпечного лікування до зникнення хвороби. Досягнення мети включає уникнення тригерів і фармакотерапію мінімально ефективною дозою або комбінацією препаратів. Пацієнти мають бути під постійним наглядом. Терапію потрібно корегувати залежно від симптомів. За підвищення дози (крок угору) варто враховувати час початку дії; наприклад, Н1-АГЗ не дають додаткового ефекту після 1-2 тижнів через насиченість рецепторів. За зниження дози (крок униз) вибір залежить від вартості й інших чинників.
Цілі лікування
Сучасні методи лікування спрямовані на блокаду медіаторів тучних клітин на нервах і ендотелії; зменшення їх активації автоімунними тригерами; регуляцію імунітету 2-го типу; пригнічення або зменшення кількості тучних клітин. Загальною метою лікування є цілковитий контроль симптомів; у майбутньому – створення підходу, що забезпечить вилікування. Фармакотерапія має бути безперервною, доки потрібна. Наприклад, неседативні Н1-АГЗ II покоління (Н1-АГЗ II) варто приймати щодня для профілактики, а не «за потреби». Вони безпечні при тривалому застосуванні, зокрема й під час вагітності. Механізм дії полягає у зворотному агоністичному впливі на H1-рецептори, стабілізуючи їх у неактивному стані. У разі ХІК можливе індивідуальне рішення, зважаючи на наявність і передбачуваність тригерів: тривале приймання Н1-АГЗ II за відсутності контролю чи високої активності хвороби або короткочасне профілактичне лікування перед впливом відповідного тригера.
Лікування Н1-АГЗ
Н1-АГЗ I покоління використовуються з 1950-х років, але мають виражені седативні й антихолінергічні ефекти, взаємодіють з алкоголем і ліками, порушують сон, навчання та виконання складних сенсомоторних завдань, як-от керування автомобілем. Сучасні настанови не рекомендують їх застосування, особливо в дітей, ґрунтуючись на вагомих доказах щодо потенційно серйозних побічних ефектів і повідомленнях про летальні випадки через передозування. Сучасні Н1-АГЗ II позбавлені антихолінергічних ефектів, а їхня седативна дія мінімальна чи відсутня. Проте астемізол і терфенадин демонструють кардіотоксичність у разі взаємодії з інгібіторами CYP3A4 (кетоконазол, еритроміцин) і більше не використовуються. Для лікування кропив’янки доведено ефективність біластину, цетиризину, дезлоратадину, ебастину, фексофенадину, левоцетиризину, лоратадину, мізоластину та рупатадину, але прямого порівняння між усіма препаратами поки що не проводилося. Настанови рекомендують застосування стандартних доз сучасних Н1-АГЗ II як симптоматичної терапії першої лінії. Препарати мають швидкий початок дії без тахіфілаксії; дозу можна корегувати (наприклад, залежно від температури при холодовій кропив’янці). У рідкісних випадках Н1-АГЗ можуть спричиняти загострення кропив’янки; таким пацієнтам показаний омалізумаб. Декілька досліджень продемонстрували користь від використання H1-АГЗ II у дозах, до 4 разів вищих, аніж стандартні, в пацієнтів із кропив’янкою. Дослідження стосувалися біластину, цетиризину, дезлоратадину, ебастину, фексофенадину, левоцетиризину, мізоластину та рупатадину. 
 У пацієнтів із кропив’янкою, які недостатньо реагують на стандартну дозу H1-АГЗ II, дослідження та клінічні дані підтверджують, що підвищення дози є ефективнішим і доцільнішим, аніж поєднання різних H1-АГЗ II. Настанови наголошують на можливості чотириразового підвищення дози (рис. 4), але пацієнтів слід поінформувати, що це застосування поза межами офіційно затверджених показань (off-label).
У пацієнтів із кропив’янкою, які недостатньо реагують на стандартну дозу H1-АГЗ II, дослідження та клінічні дані підтверджують, що підвищення дози є ефективнішим і доцільнішим, аніж поєднання різних H1-АГЗ II. Настанови наголошують на можливості чотириразового підвищення дози (рис. 4), але пацієнтів слід поінформувати, що це застосування поза межами офіційно затверджених показань (off-label). 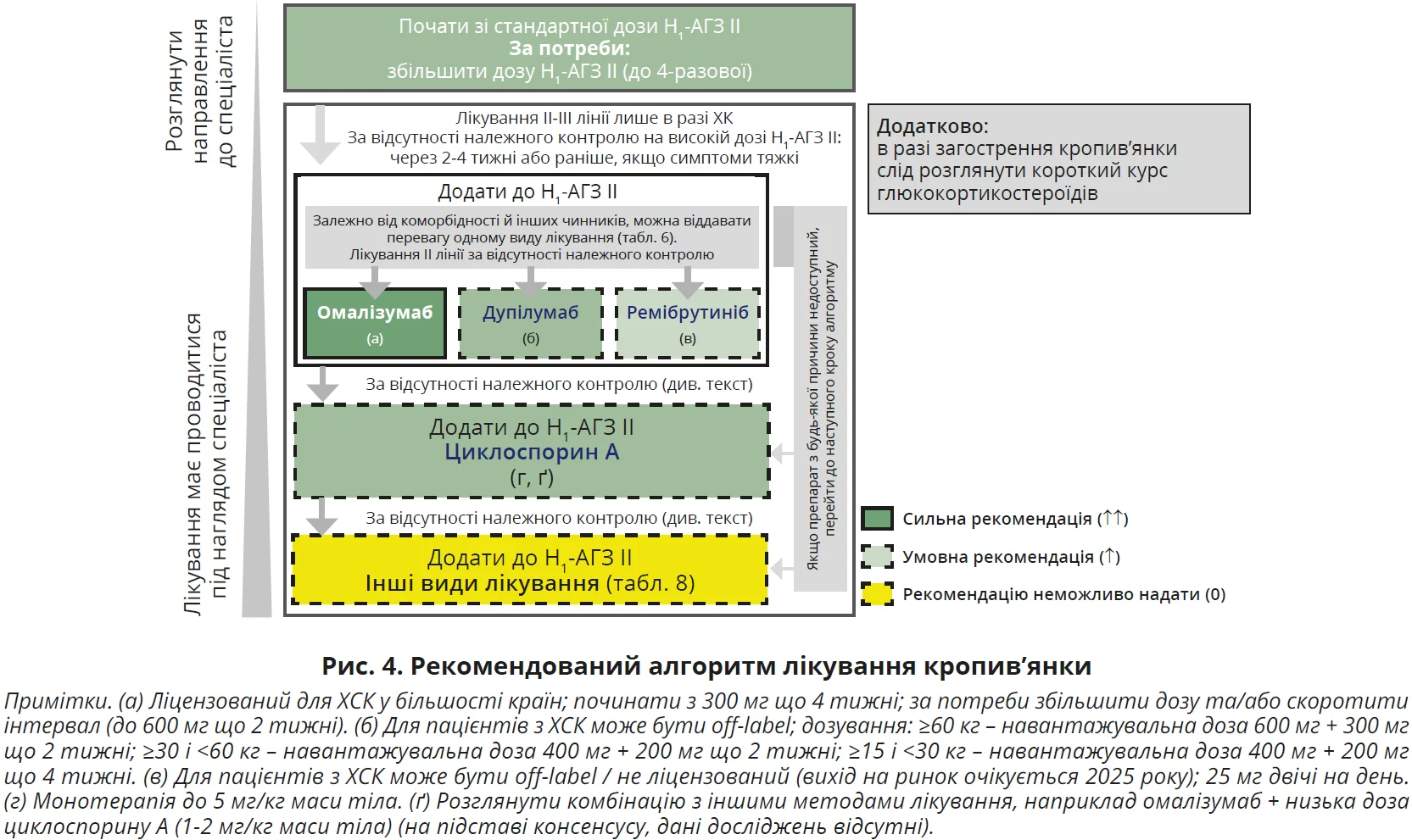 Водночас чотириразове підвищення дози включене в настанови з 2000 року, серйозних побічних ефектів або кумуляції за тривалого використання не описано. У популяційному дослідженні, проведеному в Тайвані (2011-2017), виявлено підвищений ризик деменції при збільшенні кумулятивної дози в пацієнтів з алергічним ринітом, які приймали АГЗ. Проте методологія була недосить надійною, а пізніший аналіз даних TriNetX (GUF 2024) цього не підтвердив.
Водночас чотириразове підвищення дози включене в настанови з 2000 року, серйозних побічних ефектів або кумуляції за тривалого використання не описано. У популяційному дослідженні, проведеному в Тайвані (2011-2017), виявлено підвищений ризик деменції при збільшенні кумулятивної дози в пацієнтів з алергічним ринітом, які приймали АГЗ. Проте методологія була недосить надійною, а пізніший аналіз даних TriNetX (GUF 2024) цього не підтвердив.
Лікування омалізумабом
Майже в усіх країнах світу омалізумаб (моноклональне анти-IgE-антитіло) є єдиним ліцензованим додатковим методом лікування кропив’янки, який призначають за відсутності достатнього ефекту від H1-АГЗ II. Препарат довів високу ефективність і безпеку при ХСК, а також у разі деяких форм ХІК – холінергічної, холодової, сонячної, теплової кропив’янки, симптоматичного дермографізму та відстроченої кропив’янки від тиску. У пацієнтів з ХСК запобігає появі пухирів і АН, значно покращує якість життя, підходить для довготривалого лікування й ефективний у разі рецидивів після скасування. Рекомендована початкова доза – 300 мг що 4 тижні як додаток до H1-АГЗ. Дозування не залежить від рівня IgE та маси тіла. Якщо ефект недостатній, можливе підвищення дози до 600 мг або скорочення інтервалу між уведенням до 2 тижнів (off-label). Важливо пам’ятати, що початок дії препарату зазвичай повільний. Після 3 місяців цілковитого контролю інтервал між уведенням можна поступово подовжувати до появи перших симптомів. Толерантності чи утворення блокувальних антитіл не описано. Основна причина припинення терапії – добре контрольована хвороба, а не побічні ефекти або неефективність. 
Лікування дупілумабом
Дупілумаб – моноклональне антитіло проти IL‑4Rα, що блокує дію інтерлейкіну-4 (IL‑4) й IL‑13. На відміну від омалізумабу, дупілумаб демонструє ефективність навіть за низького рівня IgE; може бути корисним у разі супутньої астми, хронічного риносинуситу з поліпами й атопічного дерматиту. Схвалений для лікування кропив’янки в США, ОАЕ, Бразилії та Японії; з 2025 року очікується ліцензування в інших країнах. 
Лікування ремібрутинібом
Ремібрутиніб – інгібітор тирозинкінази Брутона. У дослідженнях фази II та III продемонстрував ефективність як додаткове лікування ХСК і сприятливий профіль безпеки. У вересні 2025 року схвалений Управлінням США з контролю продовольства та медикаментів (FDA) як пероральний засіб для дорослих пацієнтів з ХСК, що залишаються симптоматичними на терапії H1-АГЗ. Не потребує ін’єкцій чи лабораторного моніторингу. Може застосовуватися в усіх пацієнтів з ХСК, особливо в тих, хто не відповідає на високі дози H1-АГЗ й омалізумаб. Його включення до алгоритму лікування підтверджують високоякісні результати. Користь показали різні дози, але найефективнішою вважається дозування 25 мг двічі на добу. 
Лікування циклоспорином
Циклоспорин – імуносупресивний засіб, що безпосередньо, але помірно впливає на вивільнення медіаторів тучних клітин. Призначається в дозі 3-5 мг/кг на добу для пацієнтів з ХСК, які не відповідають на H1-АГЗ II й омалізумаб. Ефективність у комбінації з H1-АГЗ II доведено в плацебо-контрольованих і відкритих дослідженнях, але не рекомендується як стандарт через високий ризик побічних ефектів, особливо за тривалого застосування. Утім, баланс користі та ризику циклоспорину кращий, аніж довготривале застосування стероїдів. Для кропив’янки циклоспорин є терапією off-label, показаний лише в тяжких випадках, резистентних до всіх ліцензованих методів лікування; може виявитися ефективним у пацієнтів з ХСК IIb типу, низьким рівнем IgE й іншими маркерами автоімунності. 
Інші симптоматичні методи лікування
Антагоністи лейкотрієнових рецепторів (АЛР) досліджувалися в кількох рандомізованих клінічних дослідженнях, але результати важко порівнювати через гетерогенність популяцій пацієнтів. Загалом рівень доказів ефективності АЛР у разі кропив’янки низький; найбільше даних є для монтелукасту. Топічні кортикостероїди ефективні при багатьох алергічних хворобах, але не при кропив’янці (виняток – альтернативна терапія кропив’янки внаслідок тиску на стопи, низький рівень доказів). Щодо системних кортикостероїдів, то потрібні високі дози (20-50 мг на день преднізолону для дорослих), що за тривалого застосування спричиняє значні побічні ефекти. Тому довготривале використання не рекомендується. У деяких країнах (Німеччина, Японія) стероїди не ліцензовані для ХК.  Отже, H1-АГЗ в дозах, до 4 разів вищих від стандартних, контролюють симптоми в більшості пацієнтів, але за резистентності потрібні альтернативи. Настанови рекомендують дотримуватися алгоритму лікування (рис. 4). Обмеженнями для призначення омалізумабу, дупілумабу та ремібрутинібу є висока вартість, для циклоспорину – проблеми безпеки. Терапію слід вибирати з огляду на статус ліцензування й економічні аспекти. Через можливі коливання тяжкості та спонтанні ремісії рекомендується переглядати лікування що 3-6 місяців (рис. 3). Інші методи лікування поза алгоритмом здебільшого мають низький рівень доказів, за винятком бенралізумабу (помірна якість доказів), який не показав статистично значущої ефективності в класичному дослідженні при ХК, але може розглядатися в пацієнтів із супутньою еозинофільною астмою. Доказів щодо ефективності Н2-антагоністів, АЛР, гідроксихлорохіну, метотрексату й дапсону недостатньо, хоча вони можуть бути актуальними, коли ресурси обмежені. Сульфасалазин, інтерферон, плазмаферез, фототерапія, внутрішньовенні імуноглобуліни мають низьку якість доказів або описані лише в серіях випадків, але можуть бути корисними в окремих пацієнтів у відповідному клінічному контексті. Такі альтернативи слід обговорювати з пацієнтом, адже вони не мають офіційних показань для лікування кропив’янки.
Отже, H1-АГЗ в дозах, до 4 разів вищих від стандартних, контролюють симптоми в більшості пацієнтів, але за резистентності потрібні альтернативи. Настанови рекомендують дотримуватися алгоритму лікування (рис. 4). Обмеженнями для призначення омалізумабу, дупілумабу та ремібрутинібу є висока вартість, для циклоспорину – проблеми безпеки. Терапію слід вибирати з огляду на статус ліцензування й економічні аспекти. Через можливі коливання тяжкості та спонтанні ремісії рекомендується переглядати лікування що 3-6 місяців (рис. 3). Інші методи лікування поза алгоритмом здебільшого мають низький рівень доказів, за винятком бенралізумабу (помірна якість доказів), який не показав статистично значущої ефективності в класичному дослідженні при ХК, але може розглядатися в пацієнтів із супутньою еозинофільною астмою. Доказів щодо ефективності Н2-антагоністів, АЛР, гідроксихлорохіну, метотрексату й дапсону недостатньо, хоча вони можуть бути актуальними, коли ресурси обмежені. Сульфасалазин, інтерферон, плазмаферез, фототерапія, внутрішньовенні імуноглобуліни мають низьку якість доказів або описані лише в серіях випадків, але можуть бути корисними в окремих пацієнтів у відповідному клінічному контексті. Такі альтернативи слід обговорювати з пацієнтом, адже вони не мають офіційних показань для лікування кропив’янки.  Моноклональні антитіла до IL-23, фактора некрозу пухлин-α та внутрішньовенний імуноглобулін успішно застосовувалися лише в окремих випадках. Використання цих препаратів можливе лише в спеціалізованих центрах як остання опція. У разі поєднання ХСК із симптоматичним дермографізмом можливе додавання до Н1-АГЗ фототерапії (УФ-B, УФ-A, PUVA) на 1-3 місяці з обережністю через канцерогенний ризик. Методи лікування, визнані неефективними в контрольованих дослідженнях, не мають застосовуватися: транексамова кислота та кромоглікат натрію при ХСК, ніфедипін за дермографізму, колхіцин й індометацин за компресійної кропив’янки. Водночас пілотне дослідження показало потенційну ефективність гепарину та транексамової кислоти в пацієнтів з підвищеним рівнем D-димеру.
Моноклональні антитіла до IL-23, фактора некрозу пухлин-α та внутрішньовенний імуноглобулін успішно застосовувалися лише в окремих випадках. Використання цих препаратів можливе лише в спеціалізованих центрах як остання опція. У разі поєднання ХСК із симптоматичним дермографізмом можливе додавання до Н1-АГЗ фототерапії (УФ-B, УФ-A, PUVA) на 1-3 місяці з обережністю через канцерогенний ризик. Методи лікування, визнані неефективними в контрольованих дослідженнях, не мають застосовуватися: транексамова кислота та кромоглікат натрію при ХСК, ніфедипін за дермографізму, колхіцин й індометацин за компресійної кропив’янки. Водночас пілотне дослідження показало потенційну ефективність гепарину та транексамової кислоти в пацієнтів з підвищеним рівнем D-димеру. 
- Лікування особливих популяцій
Діти
Багато лікарів досі призначають дітям Н1-АГЗ I покоління, вважаючи їх безпечнішими через триваліший досвід застосування. Проте ці препарати не рекомендуються як терапія першої лінії через гірший профіль безпеки та негативний вплив на навчання. У дітей доведено ефективність і безпеку таких Н1-АГЗ II: біластин, цетиризин, дезлоратадин, фексофенадин, левоцетиризин, лоратадин, рупатадин. Вибір залежить від віку та доступності лікарських форм (сироп, розчинні таблетки). Ліцензований мінімальний вік застосування відрізняється між країнами, деякі препарати доступні для немовлят. Подальші кроки слід робити обережно, адже підвищення доз та інші методи мало досліджені в дітей. Омалізумаб дозволений для лікування астми із 6 років; це єдиний схвалений біологічний препарат для рефрактерної до Н1-АГЗ ХСК у дітей віком ≥12 років. Дупілумаб дозволений для атопічної екземи із 6 місяців; проходить випробування в дітей віком ≥2 років з неконтрольованою ХСК. Циклоспорин використовується в трансплантології навіть у дуже малих дітей. Короткі курси кортикостероїдів можна призначати лише у виняткових випадках. 
Вагітні та жінки, які годують груддю
Принципи лікування вагітних і жінок, що годують груддю, подібні: уникати системних препаратів, особливо в першому триместрі вагітності, намагаючись забезпечити оптимальну терапію. У дослідженні PREG-CU загострення кропив’янки у вагітних, що потребували невідкладної допомоги, асоціювалися з передчасними пологами. Загалом сучасні Н1-АГЗ II (лоратадин, дезлоратадин, цетиризин, левоцетиризин) вважаються найбезпечнішими; даних про вроджені вади немає, хоча дослідження обмежені. Усі Н1-АГЗ виділяються в грудне молоко, але перевага віддається засобам II покоління, бо препарати I покоління можуть спричиняти седативний ефект у немовлят. Підвищення доз Н1-АГЗ у вагітних не досліджене й можливе лише з великою обережністю. Омалізумаб застосовувався під час вагітності без ознак тератогенності. Циклоспорин не тератогенний, але ембріотоксичний у тварин, асоціюється з передчасними пологами та низькою масою тіла новонароджених.  Література
Література
- Zuberbier T., Abdul Hameed Ansari Z., Abdul Latiff A.H., et al. The international guideline for the definition, classification, diagnosis and management of urticaria. Allergy. 2026 Feb 6. doi: 10.1111/all.70210.
- Magerl M., Altrichter S., Borzova E., et al. The definition, diagnostic testing, and management of chronic inducible urticarias – the EAACI/GA(2)LEN/EDF/UNEV consensus recommendations 2016 update and revision. Allergy. 2016 Jun; 71 (6): 780-802. doi: 10.1111/all.12884.
- Maurer M., Abuzakouk M., Bérard F., et al. The burden of chronic spontaneous urticaria is substantial: real-world evidence from ASSURE-CSU. Allergy. 2017 Dec; 72 (12): 2005-2016. doi: 10.1111/all.13209.