Визначення стандартів підготовки алергологів з питань захворювань опасистих клітин: консенсус Європейської академії алергії та клінічної імунології
Переклала й адаптувала канд. мед. наук Світлана Опімах
Захворювання мастоцитів (опасистих клітин – ОК), як-от мастоцитоз і синдром активації мастоцитів (САМ), – це група складних і часто виснажливих станів, що потребують спеціалізованих знань і лікування. Ці розлади проявляються в широкому клінічному спектрі від малосимптомних випадків (як-от безсимптомний шкірний мастоцитоз – ШМ) до рецидивних епізодів анафілаксії.
У 3,5-5% пацієнтів з анафілаксією та близько 22% пацієнтів з алергією на отруту перетинчастокрилих, які потребують імунотерапії, підґрунтям патології є клональність ОК. До двох третин пацієнтів із системним мастоцитозом (СМ) без шкірних уражень мають анафілаксію. Поширена думка, що всі пацієнти з мастоцитозом стикаються з непередбачуваним ризиком анафілаксії, часто призводить до емпіричного та непотрібного уникнення лікарських засобів (нестероїдних протизапальних препаратів, опіатів/опіоїдів, нейром’язових блокаторів, радіоконтрастних речовин, хінолонів, ванкоміцину), вакцин і так званих продуктів-гістамінолібераторів (як-от помідорів, молюсків, арахісу). Уникнення таких подразників часто є даремним, оскільки пов’язаний з ними ризик активації ОК зазвичай низький, подібний до ризику в загальній популяції.
Робоча група Європейської академії алергії та клінічної імунології (European Academy of Allergy & Clinical Immunology – EAACI) має на меті надати експертні рекомендації щодо мінімальних вимог і стандартів навчання з розладів ОК для алергологів і клінічних імунологів.
Визначення
Мастоцитоз охоплює спектр гетерогенних клінічних проявів, які характеризуються накопиченням клональних і фенотипово аберантних ОК у різних тканинах і органах, як-от шкіра, кістковий мозок (КМ) і шлунково-кишковий тракт (ШКТ), що часто проявляється ознаками активації ОК. Діагноз
мастоцитозу встановлюється за наявності діагностичних критеріїв шкірного та/або системного мастоцитозу (табл. 1). Пацієнтам без ШМ, у яких виявлено клональні ОК (що експресують CD25 або в яких виявлено мутацію KIT-гена) та які не відповідають критеріям СМ, діагностують синдром активації моноклональних мастоцитів.
САМ є окремою нозологією та характеризується рецидивними, тяжкими, системними симптомами активації ОК. САМ діагностують за виконання всіх трьох діагностичних критеріїв (клінічних, лабораторних і критеріїв терапевтичної відповіді). Клінічний критерій стосується щонайменше двох тяжких епізодів з одночасним ураженням щонайменше двох систем органів, що зазвичай відповідає критеріям анафілаксії. Лабораторний критерій передбачає підвищення рівня медіатора ОК під час симптоматичних епізодів, як-от триптази сироватки крові, метаболітів гістаміну в сечі чи простагландину D2. Пов’язане з подією підвищення рівня триптази в сироватці крові, яке визначається за формулою ≥20% + 2 нг/мл порівняно з вихідними рівнями, є найспецифічнішим маркером активації ОК. Критерієм терапевтичної відповіді є зниження тяжкості та частоти епізодів активації ОК під впливом антимедіаторної терапії, препаратів, що стабілізують ОК, або обох.
Рекомендація 1
Алергологи та клінічні імунологи мають розуміти біологію й патогенез клональності ОК.
ОК походять з гемопоетичних стовбурових клітин і експресують широкий спектр рецепторів, які при зв’язуванні з їхнім (-ими) лігандом (-ами) призводять до різних шляхів активації (дегрануляція, поетапна дегрануляція та диференційне вивільнення медіаторів). Медіатори ОК поділяють на попередньо сформовані сполуки в гранулах (гістамін і триптаза), синтезовані de novo мембранні ліпідні медіатори, а також цитокіни. Багато із цих медіаторів відомі своєю дією на гладку мускулатуру (вазодилатація, бронхоконстрикція та скорочення гладкої мускулатури ШКТ), свербіж і набряк, вони також відповідають за запалення, ремоделювання тканин і метаболізм кісток.
ОК є єдиними гемопоетичними клітинами, які зберігають високу експресію KIT/CD117 за термінальної диференціації. За наявності активаційних мутацій KIT зазнає лігандонезалежної димеризації, що призводить до конститутивних каскадів фосфорилювання, котрі спричиняють проліферацію/накопичення мутованого клону ОК і можуть знижувати поріг активації ОК.
Рекомендація 2
Алергологи та клінічні імунологи мають набути досвіду в клінічному оцінюванні системних проявів активації та/або накопичення ОК.
Клінічні прояви розладів ОК гетерогенні. Важливими є розпізнавання як клональних, так і неклональних захворювань, пов’язаних з активацією ОК, розрізнення симптомів, зумовлених медіаторами, та симптомів, пов’язаних з інфільтрацією, а також знання про повний спектр ураження систем органів, від шкірних і шлунково-кишкових до серцево-судинних, скелетних і нейропсихіатричних проявів.
За визначенням, неклональні САМ проявляються рецидивною анафілаксією, опосередкованою IgE або не-IgE. Приблизно в половини пацієнтів із клональним САМ спостерігається анафілаксія. Особливу увагу варто приділяти тим, хто звертається із синкопе чи пресинкопе під час анафілаксії за відсутності ураження слизово-шкірних оболонок (без кропив’янки, свербежу або ангіоневротичного набряку). Наявність шкірних уражень мастоцитозу підтверджує діагноз клональних розладів ОК, тоді як рецидивні пресинкопе, синкопе чи напади непритомності та скелетні прояви, як-от остеопенія, остеопороз або остеосклероз у пацієнтів з анафілаксією, мають спонукати до подальшого обстеження. У пацієнтів з розладами ОК можуть одночасно спостерігатися шкірні (кропив’янка, ангіоневротичний набряк), шлунково-кишкові (нудота/блювання, печія, біль у животі, діарея, мальабсорбція, печінкова недостатність, асцит і вторинна гіпоальбумінемія), гематологічні (анемія, цитопенії, еозинофілія, моноцитоз), серцево-судинні (напади непритомності, синкопе, гіпотензія), нейропсихіатричні (мігрень, дизавтономія, когнітивні порушення, амнестичні зміни, проблеми з увагою), конституційні (втома, втрата ваги) прояви й органічна дисфункція (через інфільтрацію ОК) у задавнених випадках.
Рекомендація 3
Алергологи та клінічні імунологи повинні мати глибокі знання щодо розрізнення клональних і неклональних захворювань ОК.
Інструментами, що використовуються для виявлення клональності ОК, є гістопатологія КМ, проточна цитометрія КМ, високочутливі й ультрачутливі молекулярні аналізи для виявлення мутацій KIT, а також прогностичні алгоритми, як-от шкали REMA, NICAS і Karolinska.
Основні клінічні прояви незадавнених клональних мастоцитозних захворювань охоплюють анафілаксію, мастоцитозні ураження шкіри й остеопороз, тоді як задавнений мастоцитоз може проявлятися вже названими ознаками, а також пов’язаними з ними конституційними проявами й органічною дисфункцією. Клональність ОК полягає в присутності принаймні одного з таких симптомів: експресія ОК CD25, CD30 або CD2 (шкірна в разі ШМ, позашкірна в разі СМ), виявлення активувальної мутації KIT або наявність шкірних або позашкірних (як-от кісткова мастоцитома) мастоцитозних уражень. Для оцінювання клональності ОК у пацієнтів з анафілаксією в анамнезі проводять детальний збір анамнезу та ретельне обстеження (пошук типових шкірних мастоцитозних уражень, лімфаденопатії чи органомегалії). Про підвищену ймовірність клональності ОК свідчать ознаки, узагальнені в таблиці 2.
Рекомендація 4
Алергологи та клінічні імунологи мають розуміти важливі для діагностики й подальшого спостереження методи.
Біопсія позашкірних тканин, зокрема дослідження КМ, є важливою для діагностики СМ і потребує як аспіраційних, так і біопсійних зразків. Методи молекулярної біології можуть застосовуватися в цілих або фракціонованих зразках КМ або крові. Проточна цитометрія проводиться на свіжих зразках КМ і має включати мінімальну панель, а саме CD45, CD117, CD25, CD2 і CD30.
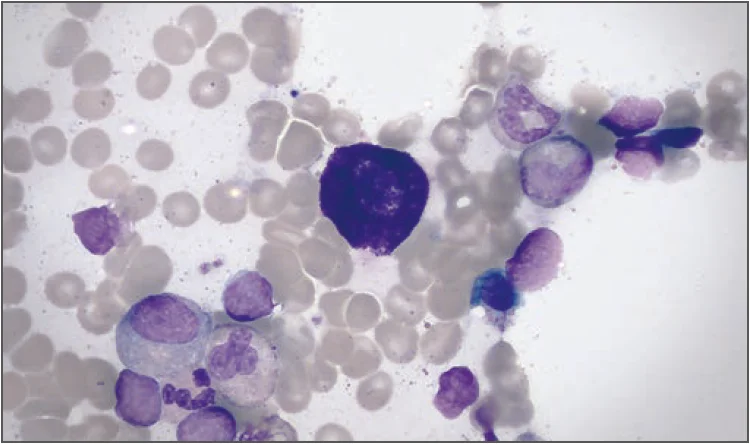
Біопсії тканин (тобто біопсія шкіри та КМ) залишаються вирішальними для діагностики мастоцитозу. У шкірі агрегати ОК або інтерстиційні дифузні інфільтрати, що містять ≥20 ОК на поле зору при високому збільшенні, свідчать про ШМ. Гістологічне дослідження КМ має оцінювати компактні агрегати ОК (≥15 клітин), збільшення інтерстиційних ОК і фіброз. Для обох випадків стандартним є імуногістохімічне фарбування моноклональними антитілами проти триптази й KIT. Цитологічний аналіз дає змогу ідентифікувати атипові морфології ОК: веретеноподібні, гіпогранульовані, багатолобатні/промастоцитарні та бластоподібні форми.
Кількісне визначення триптази в сироватці крові є наріжним каменем, що потребує знання преаналітичних факторів, часу (як-от від пів години до 2 годин після події для гострих зразків) і використання систем на основі FEIA (наприклад, ImmunoCAP, Phadia/Thermo Fisher Scientific Inc, м. Уппсала, Швеція). Триптаза сама по собі не є діагностичним критерієм. За рівня триптази >8 нг/мл генотипування TPSAB1 за допомогою цифрової полімеразно-ланцюгової реакції може ідентифікувати спадкову α-триптаземію.
Правильна класифікація СМ потребує лабораторних і візуалізаційних оцінок. Результати варто класифікувати в межах категорій B (що вказує на високе навантаження КМ) і C (що вказує на дисфункцію органів) (табл. 3).
Для пацієнтів з розладами ОК потрібне спостереження. У пацієнтів зі ШМ, неактивним СМ або мастоцитозом КМ, за яких симптоми активації ОК добре контролюються, спостереження може включати щорічну консультацію, під час якої оцінюються триптаза й інші параметри крові. Пацієнти з активним і задавненим СМ потребуватимуть частішого спостереження разом з гематологами.
Рекомендація 5
Алергологи та клінічні імунологи мають знати фармакологічні засоби для контролю симптомів активації ОК.
Основними класами препаратів для фармакологічного лікування розладів ОК є H1– і H2-антигістамінні препарати (АГП), стабілізатори мембран ОК (кромоглікат натрію, кетотифен), модифікатори лейкотрієнів, інгібітори циклооксигенази, біологічні препарати, як-от омалізумаб, та інгібітори тирозинкінази.
H1-АГП є основою антимедіаторної терапії як клональних, так і неклональних розладів ОК, їхню добову дозу, подібно до лікування хронічної спонтанної кропив’янки, можна підвищувати вчетверо від рекомендованої. Пацієнти з рефрактерною анафілаксією можуть отримати користь від приймання омалізумабу, H2-АГП і кромоглікату натрію. При рефрактерних шкірних припливах може бути корисною ацетилсаліцилова кислота (для пацієнтів з доведеною толерантністю) й антагоністи лейкотрієнів. У разі спазмів у животі та/або хронічної діареї можуть призначатися кромоглікат натрію, H2-АГП, курси перорального будесоніду, антагоністи лейкотрієнів і курси низьких доз глюкокортикоїдів (окрім будесоніду).
Пацієнтам з анафілаксією в анамнезі (за винятком випадків, коли вона суворо пов’язана з лікарськими засобами) варто призначити два автоін’єктори адреналіну.
Рекомендація 6
Алерголог і клінічний імунолог мають знати профілактичні заходи для уникнення епізодів активації ОК.
Профілактичними заходами для уникнення епізодів активації ОК є стратегії елімінації та премедикації, а також правильне проведення алерготестування.
Деякі експерти пропонують призначати загальні премедикації, як-от H1– і H2-АГП, антагоністи лейкотрієнових рецепторів і глюкокортикоїди, перед хірургічними процедурами, загальною анестезією та рентгенографічною візуалізацією з використанням радіоконтрастних речовин. Окрім того, перед процедурами, що проводяться під місцевою анестезією, та вакцинацією рекомендується застосовувати H1-АГП.
Рекомендація 7
Алергологи та клінічні імунологи мають отримати чіткі знання про імунотерапію отрутою комах.
Алергія на отруту перетинчастокрилих є найчастішим тригером анафілаксії в дорослих із клональними розладами ОК.
Імунотерапія отрутою показана всім пацієнтам з гіперчутливістю до отрути перетинчастокрилих, у яких виявлено IgE-опосередкований механізм. Однак у пацієнтів із клональними розладами ОК, незважаючи на алергію, часто спостерігаються низькі рівні загального та специфічного IgE, тому важливо бути ознайомленим з різними методами, які виявляють сенсибілізацію до IgE (тобто зниження порогу, що визначає сенсибілізацію до IgE, з 0,35 до 0,15 або навіть 0,1 кОА/л). У пацієнтів з мастоцитозом тривалість толерантності до отрут є коротшою, ніж у загальній популяції, що потребує подовження тривалості терапії.
Рекомендація 8
Стажери з алергології та клінічної імунології мають уміти ідентифікувати клінічні форми мастоцитозу з початком у дитячому віці.
Мастоцитоз зазвичай починається на двох етапах життя: в дитинстві чи в дорослому віці, лише невелика кількість випадків виникає в підлітковому віці. Мастоцитоз, що починається в дитинстві, переважно проявляється ураженням шкіри, системні форми є рідкісними, хоча й клінічно значущими. Ці пацієнти значно менш схильні до анафілаксії, ніж дорослі, а ті, хто має шкірну мастоцитому та дифузний ШМ, мають вищий ризик анафілаксії. Інші чинники ризику анафілаксії охоплюють підвищений рівень триптази, значне ураження шкіри, високу щільність ОК в ураженнях й утворення пухирів в ураженнях.
Рекомендація 9
Алергологи та клінічні імунологи мають розвивати необхідні комунікативні навички.
У більшості пацієнтів з мастоцитозом між появою симптомів і остаточним діагнозом часто минає кілька років. Загальні знання лікарів про ці стани зазвичай обмежені, тому пацієнти часто відчувають, що їх не розуміють. Окрім того, хоча пригнічений мастоцитоз становить невеликий відсоток випадків СМ, він іноді може бути смертельним.
Комунікативні навички корисні не лише для прояву емпатії й емоційної підтримки, але й для надання інформації у випадках з поганими клінічними результатами.
Рекомендація 10
Стажери мають отримувати знання про хвороби ОК або через ротацію в досвідченому центрі, або через безперервну медичну освіту.
Розлади мастоцитів – це гетерогенні хвороби, які потребують вузькоспеціалізованих діагностичних і терапевтичних підходів. Діагностичні процедури є точнішими, коли їх виконують у досвідчених референтних центрах. Клінічні ротації в референтних центрах з досвідом роботи з розладами ОК пропонують стажерам унікальні можливості закріпити теоретичні знання завдяки практичному досвіду, зокрема в застосуванні діагностичних критеріїв Всесвітньої організації охорони здоров’я, інтерпретації передової проточної цитометрії та молекулярної діагностики, а також у впровадженні персоналізованих стратегій запобігання й лікування в міждисциплінарному контексті.
Висновки
Швидкий розвиток досліджень, пов’язаних з розладами мастоцитів, і розширення клінічного застосування молекулярної діагностики, фармакогеноміки й біологічних препаратів вимагають, щоб майбутні алергологи та клінічні імунологи оволоділи фундаментальними знаннями та вміннями в цьому напрямі. Це є важливим не лише для точної діагностики й ефективного лікування, але й для належного використання нових діагностичних методів і цілеспрямованої терапії в клінічній практиці.
Література
Rama T., Gulen T., Brockow K., et al. Definition of standards for allergology specialty/subspecialty training in mast cell disorders, in Europe: a EAACI position paper. Authorea. 2026 Jan 29. DOI: 10.22541/au.176967556.62286692/v1.