Номенклатура алергічних захворювань і реакцій гіперчутливості: позиційний документ Європейської академії алергології та клінічної імунології
Підготувала канд. біол. наук Олександра Демецька
Стрімке зростання сучасних діагностичних інструментів, включаючи оміксні технології (епігеноміку, транскриптоміку, протеоміку, інтерактоміку, нанотехнології тощо), а також доступ пацієнтів до широкомасштабного медичного обслуговування сприяли появі значної кількості неупереджених даних, що дають змогу поглиблено характеризувати захворювання. Зокрема, для алергічних захворювань було виявлено нові ендотипи, що забезпечило поступовий перехід від опису, зосередженого на симптомах, до визначення біомаркерів і складних патогенетичних і метаболічних шляхів.
Новий позиційний документ Європейської академії алергології та клінічної імунології (EAACI) у відповідь на ці виклики представив сучасну номенклатуру алергічних захворювань, не відкидаючи при цьому попередні класифікації початку ХХ століття.
Нова концепція класифікації алергічних захворювань
У 2001 році номенклатурна робоча група EAACI під керівництвом професора Каролінського університету (Швеція) C. Йоханссона опублікувала номенклатуру алергічних захворювань. У цьому документі підвищена чутливість поділяється на такі категорії: реакції, опосередковані імуноглобуліном Е (IgE), які включають атопічні та неатопічні стани (укуси комах, харчова алергія, ліки, гельмінти); не-IgE-опосередковані розлади, які є клітинно-опосередкованими реакціями, що включають Т-лімфоцити (контактний дерматит), імуноглобулін G – IgG (алергічний альвеоліт) й інші імунні клітини, наприклад еозинофіли (гастроентеропатія); а також неалергічні реакції, до яких не залучені імунні механізми [21, 26].
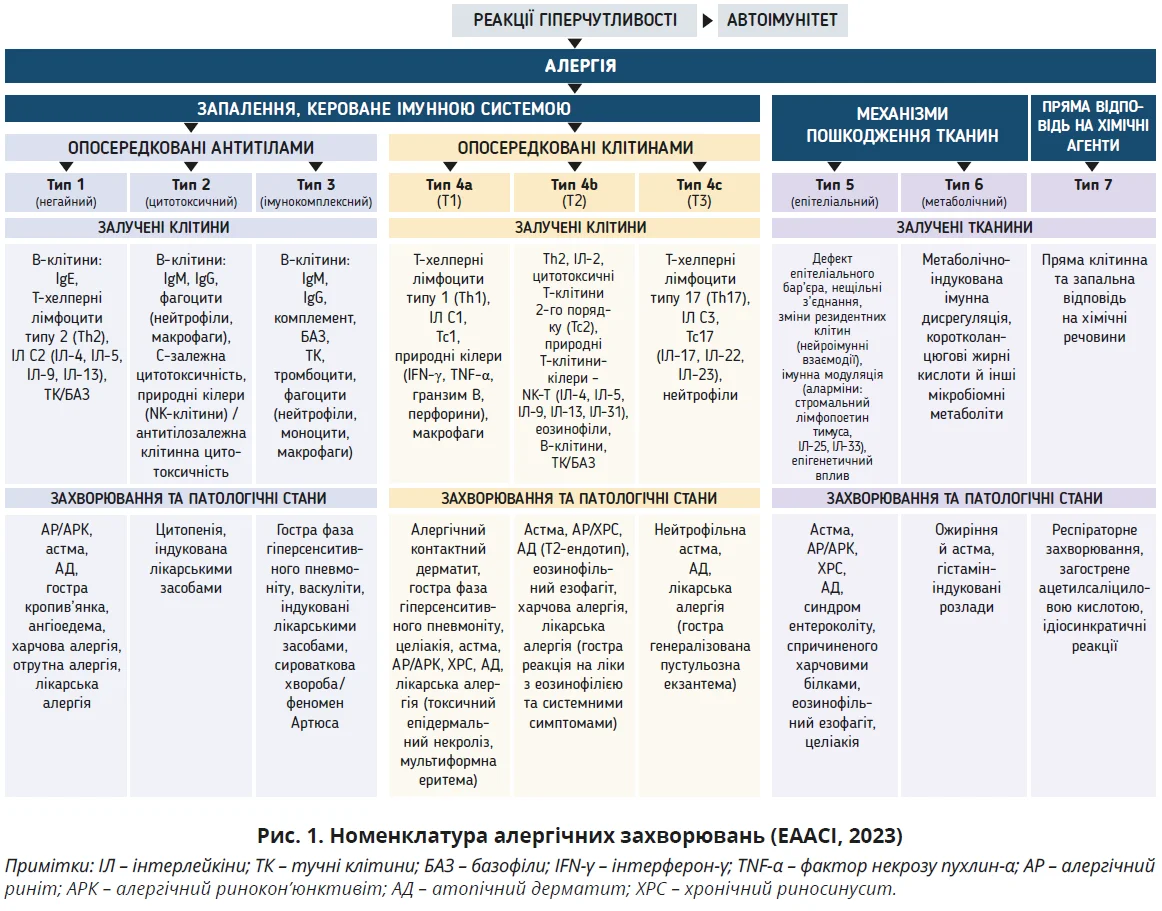
Зважаючи на прогрес у розумінні імунних механізмів і нових терапевтичних можливостей, новий позиційний документ EAACI містить необхідне оновлення власної попередньої номенклатури, а також класифікації Всесвітньої організації з питань алергії (рис. 1).
Нова концепція ґрунтується на розумінні різних характеристик і функцій комплексних імунних реакцій типів 1, 2 та 3, а також реакцій, опосередкованих тканинами, які відіграють вирішальну роль в імунозалежних розладах, як-от алергія або автоімунітет.
Сучасне визначення алергії має відображати патофізіологічну складність цих станів, зокрема таких, що зумовлені гіперчутливістю імунної системи, спричиненою нешкідливими речовинами довкілля. Хоча традиційно механізми алергії пов’язані з реакцією клітин Т2, останні відкриття показали ендотипи алергічних захворювань, що пов’язані зі шляхами активації Т1 або Т3, які раніше вважалися залученими до різноманітних імуноопосередкованих захворювань (у тому числі автоімунних), що характеризуються механізмами, відмінними від алергії [34-36].
Механізми найважливіших алергічних захворювань
Тип 1, або негайна відповідь
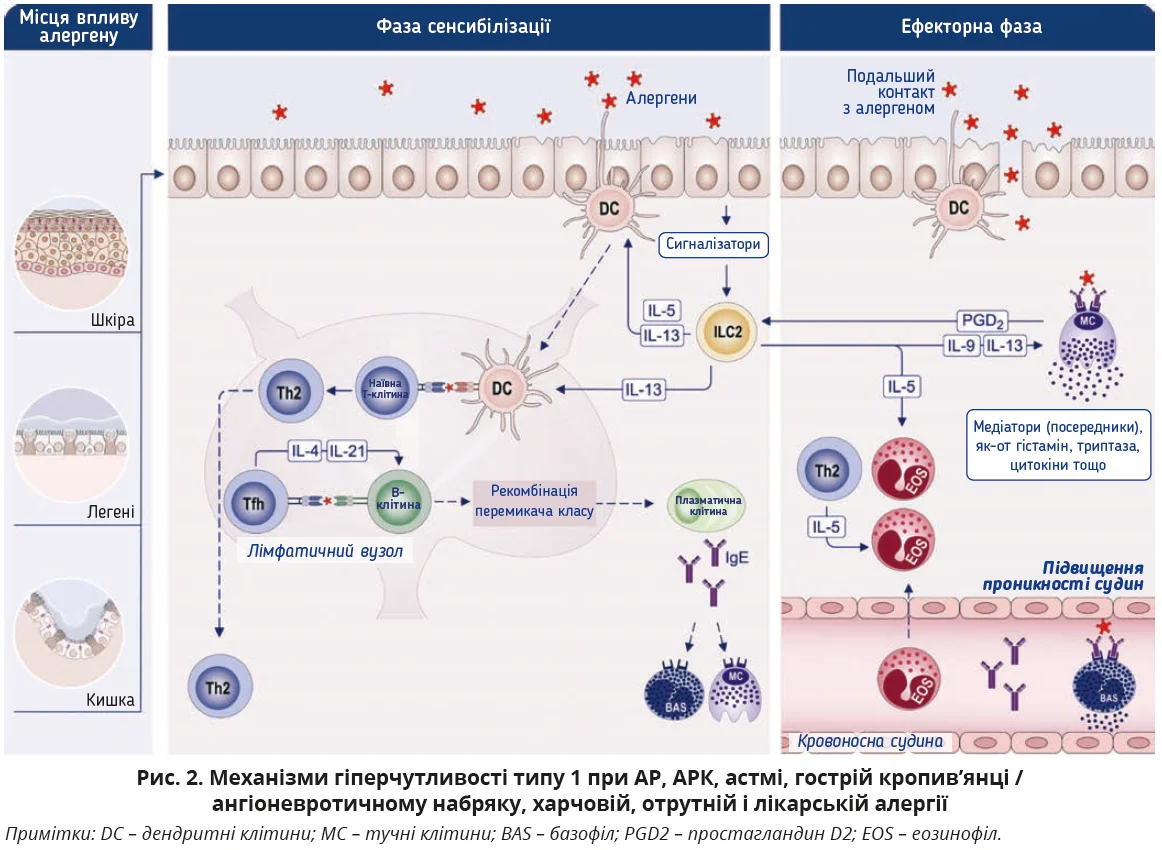
IgE-залежні реакції типу 1 включають фазу сенсибілізації й ефекторну фазу та виникають у пацієнтів з алергічним ринітом (АР), алергічним ринокон’юнктивітом (АРК), астмою, гострим атопічним дерматитом (АД), кропив’янкою / ангіоневротичним набряком, алергією на харчові продукти, отрути
та ліки (рис. 2) [40].
Класичними алергенами, що спричиняють гіперчутливість типу 1, є пилок (дерев, трав і бур’янів), кліщі домашнього пилу, спори цвілі, таргани, шерсть тварин, слина та сеча (котів, собак, хом’яків, морських свинок), отрути комах (бджіл, ос, мурах), харчові продукти (арахіс, горіхи, молоко, яйця, риба, молюски, соя, пшениця, фрукти, овочі), латекс (рукавички, повітряні кулі, презервативи) та ліки (пеніцилін й інші β-лактамні антибіотики, сироватки та вакцини, інсулін, моноклональні антитіла й інші білкові препарати).
Тип 2, або опосередкована антитілом реакція клітинної цитотоксичності
Реакції типу 2 зазвичай зумовлені ліками, які вважають причиною алергічної цитопенії. Проте реакції типу 2 є важливою патогенетичною подією при кількох автоімунних захворюваннях, як-от імунна тромбоцитопенія, автоімунна гемолітична анемія, автоімунна нейтропенія, хвороба Бірмера, синдром Гудпасчера, гемолітична хвороба плода та новонародженого (еритробластоз), міастенія ґравіс, пухирчатка й реакції на переливання крові, пов’язані з невідповідністю груп крові [61-64].
При лікарсько-залежних алергічних реакціях типу 2 препарат або його метаболіт спочатку зв’язується з білками на клітинній мембрані. Згодом антитіла проти ліків і комплекс «ліки – мембранний білок» зв’язують і активують комплемент або зв’язуються γ-рецептором Fc-фрагмента (FcγR) на ефекторній клітині, як-от NK-клітина, еозинофіл, макрофаг
або нейтрофіл, зрештою індукуючи цитоліз (рис. 3).
Реакції типу 3, або опосередковані імунним комплексом
Алергічні реакції типу 3 включають гостру фазу гіперсенситивного пневмоніту (алергічний альвеоліт), медикаментозний васкуліт, сироваткову хворобу та реакцію Артюса. Вони пов’язані з кількома автоімунними захворюваннями, включаючи системний червоний вовчак, ревматоїдний артрит і постстрептококовий гломерулонефрит [9].
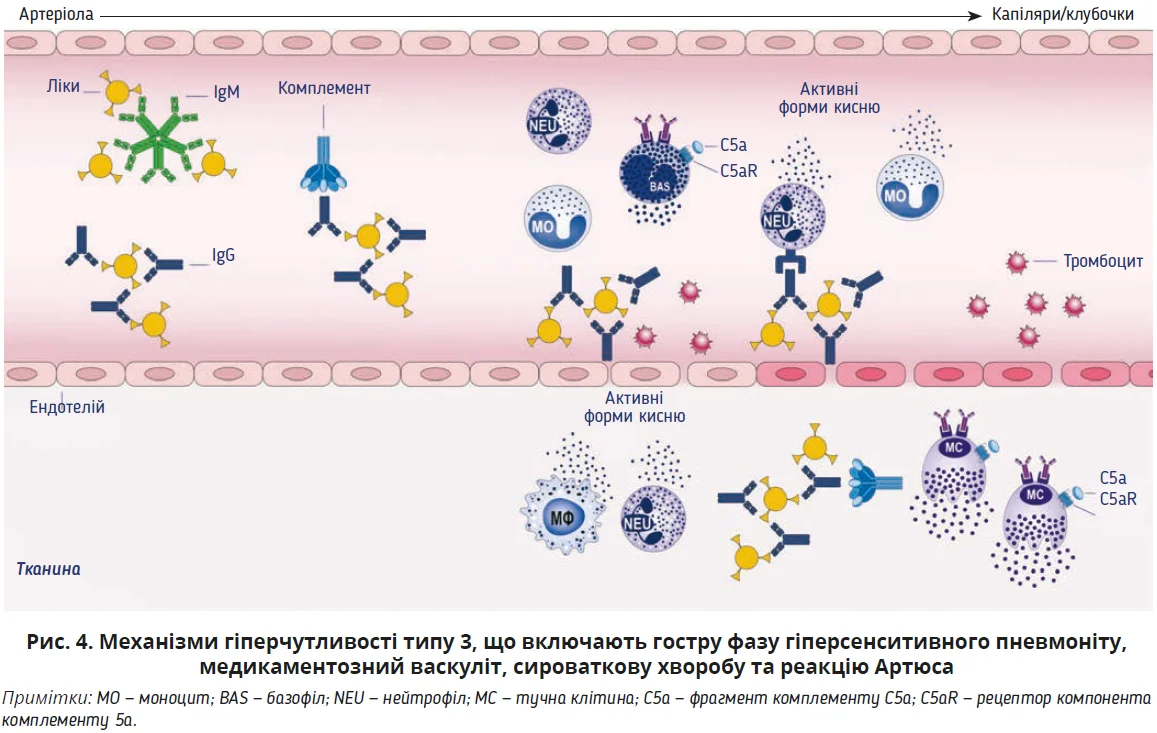
Алергічні реакції гіперчутливості типу 3 опосередковуються антитілами (IgM, IgG), які зв’язують розчинні антигени, наприклад ліки, отрути або інші алергени, з утворенням комплексів «антиген – антитіло». У результаті зниженого кліренсу внаслідок послаблення функції системи активації моноцитів або збільшення вироблення комплексів «антиген – антитіло» (наприклад, у разі хронічних інфекцій, автоімунних або неопластичних захворювань) імунні комплекси відкладаються в тканинах, які є пористими, й дають імунним комплексам змогу проникати в них і спричиняти запалення (невеликі кровоносні судини, синовіальна оболонка суглобів, клубочки нирок, легеневі альвеоли тощо).
Це призводить до позасудинної активації системи комплементу, який вивільняє хемотаксичні агенти, що приваблюють нейтрофіли, зумовлюючи запалення та пошкодження тканин (рис. 4) [69].
Тип 4, або клітинно-опосередковані реакції
Історично ці реакції називали «уповільненим типом» через спостереження, що симптоми розвиваються від кількох годин до днів після впливу. Різні підгрупи Т-клітин опосередковують відповіді типу 4 через різні специфічні шляхи, демонструючи високий ступінь гетерогенності, що відображає відмінні фенотипові особливості лімфоцитів пам’яті. Деякі механізми захворювання можна пояснити лише взаємодією кількох підтипів гіперчутливості типу 4.
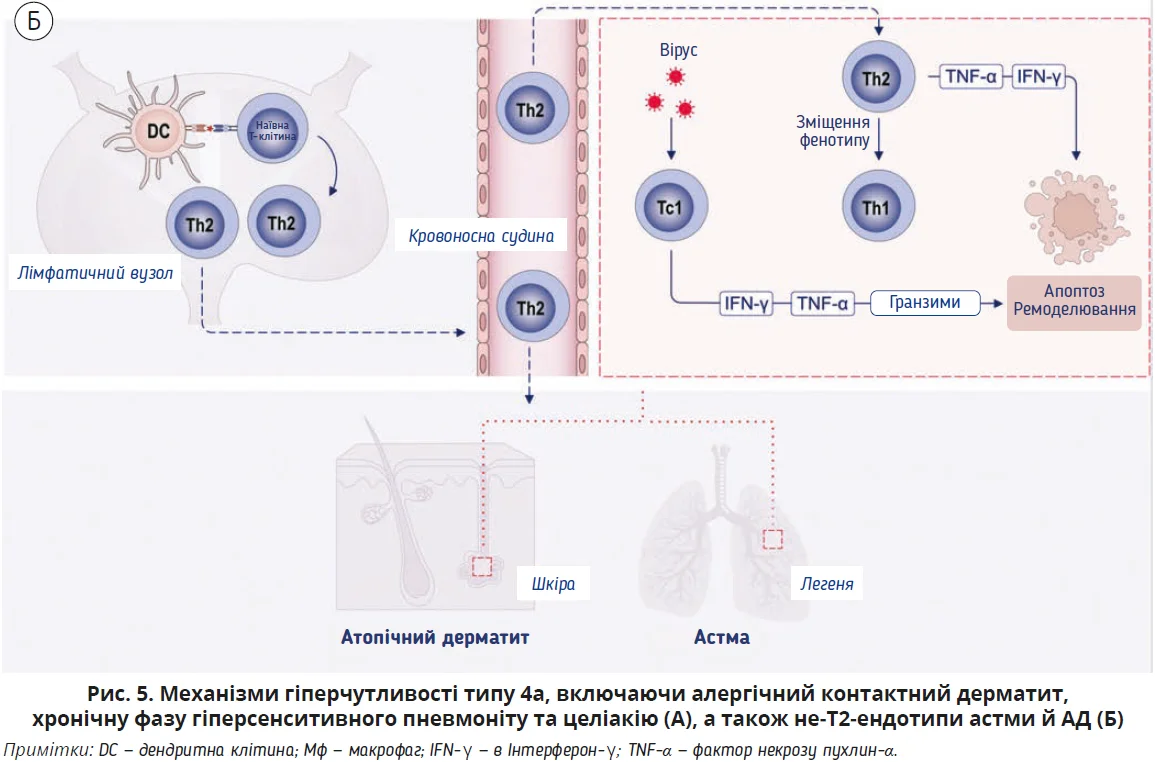
Тип 4a: імунна відповідь Т1
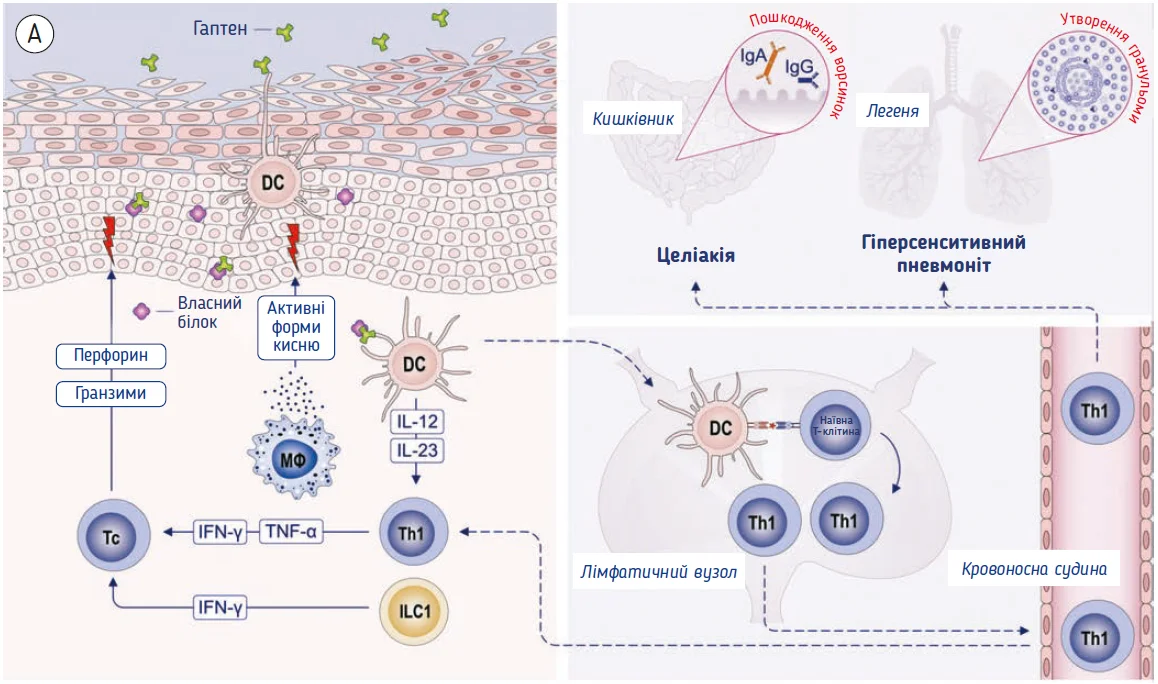
Реакції типу 4a вважають відповідями T1, опосередкованими клітинами пам’яті Th1 і Tc1, які набувають свого фенотипу під час впливу інтерлейкінів (ІЛ): ІЛ-12, ІЛ-23 й інтерферону-γ (IFN-γ). Типовими клінічними проявами реакції типу 4a є алергічний контактний дерматит, хронічна фаза гіперсенситивного пневмоніту та целіакія. Реакції типу 4a також можуть бути актуальними для не-T2-ендотипів астми, АР, хронічного риносинуситу (ХРС) або АД (рис. 5). Ці механізми також пояснюють немиттєві алергічні реакції на ліки, які виникають після гаптенізації препарату білком-носієм [75].
Тип 4b: імунна відповідь Т2
Найхарактерніший прояв реакції гіперчутливості типу 4b можна спостерігати в класичній алергічній реакції з хронічним запаленням дихальних шляхів при АР, ХРС, астмі й АД (ендотип Т2), харчовій алергії, еозинофільному езофагіті або білково-контактному дерматиті. Клітини Th2, ІЛ C2, природні кілери (NK-клітини), еозинофіли та макрофаги є головними гравцями в імунній відповіді типу 4b.
Гіперчутливість типу 4b і типу 1 збігаються на останній стадії, коли запускається синтез IgE. Клітини Е2 через вивільнені цитокіни (ІЛ-4, ІЛ-13) індукують синтез IgE. При цьому основний ефекторний механізм включає активацію еозинофілів через ІЛ-5. Окрім того, гіперчутливість типу 4b та типу 5 збігається в активації епітеліальних клітин і відкритті епітеліальних бар’єрів, а також дренажі запалення в просвіт бронхів.
Тип 4c: імунна відповідь Т3
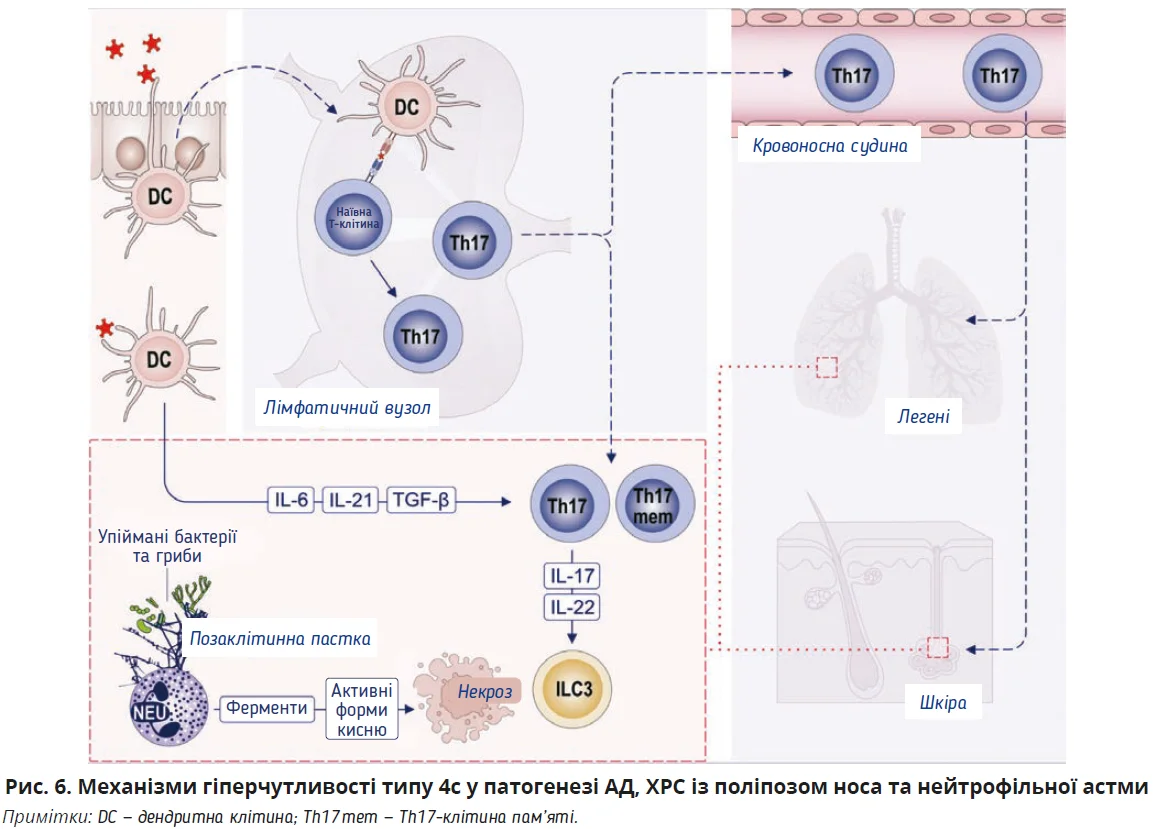
У разі гіперчутливості типу 4c клітини Th17 та ІЛ С3 відіграють ключову роль, продукуючи цитокіни сімейства ІЛ-17, які індукують залучення нейтрофіліві посилюють продукцію цитокінів Th2, що призводить до запалення. Певні бактеріальні та грибкові компоненти можуть стимулювати реакцію Th17. Ці відповіді призводять до пошкодження тканин через «дихальний вибух», вивільнення ферменту або нейтрофільну позаклітинну пастку (рис. 6) [105].
Тип 5: дефект епітеліального бар’єра
Останніми роками було досягнуто значного прогресу в розумінні різних фенотипів і ендотипів запальних захворювань слизової оболонки / шкіри, як-от хронічний АР, АРК, ХРС, АД, астма чи індукований харчовими білками синдром ентероколіту, еозинофільний езофагіт і целіакія.
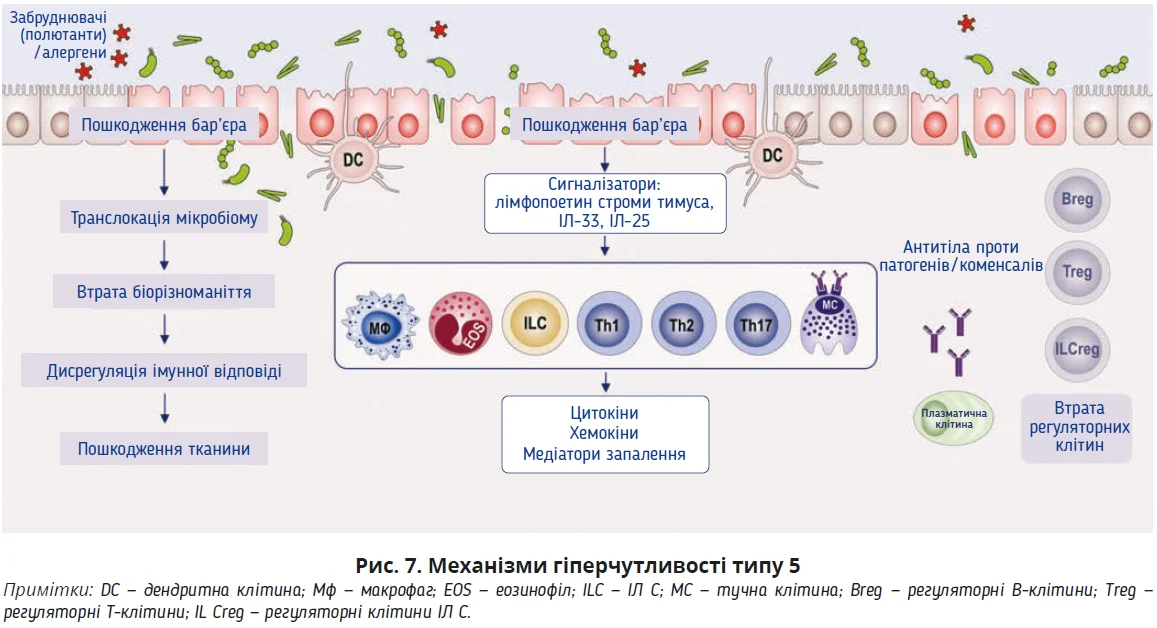
Було виявлено, що ці стани не є однорідними захворюваннями, а визначаються сукупністю симптомів, які можуть бути результатом різних патологічних механізмів [121]. У деяких випадках запальний процес відображає змінену бар’єрну функцію шкіри або слизової оболонки, а не є наслідком первинної імунної дисрегуляції [122]. Порушення функції епітеліального бар’єра полегшує активацію імунної системи та згодом призводить до хронічного запалення. Активація сенсорних нервів, що спричиняє розвиток симптомів алергії, також пов’язана зі втратою бар’єра (рис. 7).
Вплив забруднювачів повітря, хімічних речовин й інших чинників довкілля може порушити епітеліальні бар’єри та позначитися на мікробіомі й імунній системі. Це полегшує для чужорідних речовин і мікроорганізмів процес проникнення глибше до тканин, наслідком чого є імунна/запальна відповідь, яка може ініціювати або загострювати багато хронічних запальних захворювань [134].
Здорова мікробіота на поверхні слизового бар’єра регулює численні аспекти бар’єрного гомеостазу. Проте зменшення біорізноманіття та зміни у складі й метаболізмі мікробіоти кишківника та шкіри пов’язані з різними запальними станами, включаючи астму, алергічні захворювання, запальні захворювання кишківника, цукровий діабет 1 типу й ожиріння [136].
Тип 6: метаболічно нейтральний
Паралельно із загальним зростанням рівня ожиріння кількість пацієнтів з ожирінням і астмою різко зросла протягом останніх кількох років [138]. Ожиріння може впливати на запальні реакції безпосередньо (наприклад, через вивільнення медіаторів запалення із жирової тканини) або опосередковано (наприклад, через типові зміни в харчуванні, пов’язані з ожирінням, як-от високий рівень оброблених жирів і низький рівень клітковини) [140]. Збільшення індексу маси тіла пов’язано з підвищенням рівня циркулювальних медіаторів запалення та збільшенням кількості нейтрофілів і еозинофілів у крові [141].
У хворих на астму з ожирінням спостерігається додатковий вплив цих станів на посилення вивільнення прозапальних медіаторів і алергічне запалення дихальних шляхів, а також на модифікацію мікробіому кишківника, носа, ротової порожнини та легень, що є тісно пов’язаним із запальними реакціями [144].
Метаболічна дисрегуляція при діабеті й ожирінні також пов’язана з нещільністю епітеліального бар’єра. Імунні клітини, активовані в «дірявих» бар’єрних ділянках, особливо в кишківнику, можуть мігрувати до віддалених органів і спричиняти запалення. Паралельно з метаболічними змінами при ожирінні спостерігається порушення кишкової мікробіоти разом зі стійкою запальною реакцією низького ступеня в кишківнику та жировій тканині [146].
Дисбаланс мікробіому кишківника (дисбіоз) може призвести до відхилення імунної відповіді та збільшити ризик хронічних захворювань, включаючи алергію або автоімунітет. Показано, що гістамін, медіатор запалення, регулює імунну відповідь і синтезується в мікробіомі кишківника певними бактеріями, як-от Lactobacillus і Escherichia [147, 148]. Також нещодавно було ідентифіковано кілька нових імуномодифікувальних метаболітів (наприклад, метаболіти триптофану, коротколанцюгові жирні кислоти), нерегульована секреція котрих може також спричиняти розвиток алергії.
Тип 7: пряма клітинна та запальна відповідь на хімічні речовини
Реакції типу 7 виникають у пацієнтів з АР, АРК, астмою, АД, гострою кропив’янкою / ангіоневротичним набряком і алергією на ліки.
Ідіосинкратичні реакції включають перехресну гіперчутливість до нестероїдних протизапальних засобів (НПЗЗ), зокрема існує принаймні три різні фенотипи залежно від наявності чи відсутності основного респіраторного або шкірного захворювання: респіраторні захворювання, що загострюються НПЗЗ, у хворих із ринітом та/або астмою з поліпозом носа чи без нього; шкірні захворювання, загострені НПЗЗ, у пацієнтів із хронічною спонтанною кропив’янкою; НПЗЗ-індукована гостра кропив’янка / ангіоневротичний набряк у здорових осіб [151]. Останнім часом було широко описано інші фенотипи, що складаються з одночасної присутності шкірних і респіраторних симптомів після прийому НПЗЗ [152]. Основний механізм цих реакцій пов’язаний з інгібуванням циклооксигенази-1 і вивільненням ейкозаноїдних медіаторів у сприйнятливих осіб [153].
Висновки
Реакції гіперчутливості, описані Джеллом і Кумбсом, були розширені на дев’ять різних типів, що включають антитіла (1-3), клітинні (4a-c) та тканинні механізми (5-6), а також пряму відповідь на хімічні речовини (7). Типи 1-3 пов’язані з класичними та нещодавно описаними клінічними станами. Тип 4 (a-c) визначено й деталізовано відповідно до поточного розуміння відповідей T1, T2 та T3. Типи 5-6 включають дефекти епітеліального бар’єра й метаболічну імунну дисрегуляцію, тоді як прямі клітинні та запальні реакції на хімічні речовини охоплені типом 7. Прикметно, що в клінічних умовах може виникнути кілька комбінацій змішаних типів.
Новий підхід ґрунтується на механізмах захворювання й ендотипах, а не на фенотипах, що покращує розуміння зв’язку між різними алергічними захворюваннями, які можуть співіснувати в однієї людини, одночасно або в різні моменти часу протягом життя.
Головні відкриття включають роль підмножин Т-клітин, вірусних загострень, дисфункції епітеліального бар’єра тощо, а також можливість існування комбінації різних реакцій гіперчутливості.
Нова номенклатура має сприяти кращому розумінню етіології, механізмів, профілактики, діагностики та персоніфікованого лікування алергічних захворювань.
Література
Jutel M., et al. Nomenclature of allergic diseases and hypersensitivity reactions: Adapted to modern needs: An EAACI position paper. Allergy. 2023; 78 (11): 2851-2874. doi: 10.1111/all.15889.