Ефективність і безпека переходу на біластин у пацієнтів з рефрактерною хронічною спонтанною кропив’янкою (багатоцентрове відкрите рандомізоване порівняльне дослідження з паралельними групами H1-SWITCH)
Переклала й адаптувала д-р мед. наук Лариса Стрільчук
Хронічна кропив’янка (ХК) передбачає наявність уртикарних висипів, ангіоневротичного набряку або їх поєднання протягом більш ніж 6 тижнів. Підтип ХК, що виникає без очевидних тригерів, має назву хронічної спонтанної кропив’янки (ХСК). ХСК, яка вражає до 1% населення світу, негативно впливає на стан здоров’я та якість життя, а також становить значний соціально-економічний тягар. ХСК є поширенішою, ніж хронічна індукована кропив’янка, за якої симптоми спричиняються змінами температури, сонячним випромінюванням, впливом тиску чи води, холінергічною реакцією тощо.
ВСТУП
Складний етіопатогенез ХСК полягає в крос-лінкінгу імуноглобуліну E (IgE), зв’язаного з високоафінними рецепторами на поверхні опасистих клітин шкіри або базофілів, що призводить до вивільнення прозапальних медіаторів (гістаміну, фактора активації тромбоцитів, цитокінів). Ці медіатори спричиняють активацію чутливих нервових закінчень, вазодилатацію, екстравазацію плазми та залучення клітин до ділянок висипу. Симптоми ХСК переважно зумовлені дією гістаміну на H1-рецептори, розташовані на ендотеліальних клітинах, що призводить до утворення уртикарних висипів, а також впливом на чутливі нервові закінчення, що зумовлює нейрогенний свербіж. У більшості випадків ХСК триває протягом 2-5 років, а у 20% пацієнтів – понад 5 років. Згідно з міжнародними рекомендаціями метою лікування ХСК є повний контроль симптомів і нормалізація якості життя пацієнтів.
Стандартним методом лікування ХСК є безперервне застосування H1-антигістамінних препаратів (H1-АГП), проте повного усунення симптомів досягають менш ніж у 50% випадків. Залежно від хімічної структури H1-АГП поділяють на трициклічні та піперазинові/піперидинові препарати. Порівняно з АГП першого покоління неседативним Н1-АГП другого покоління властивий кращий профіль безпеки (навіть у разі застосування вищих доз), тому ці препарати дедалі частіше розглядають як терапію першої лінії для полегшення симптомів ХСК. Для пацієнтів з недостатньою відповіддю на стандартну дозу Н1-АГП другого покоління міжнародні рекомендації передбачають підвищення дози до чотириразової та/або додавання блокатора IgE омалізумабу або циклоспорину. Слід зауважити, що збільшення дози H1-АГП підвищує ризик побічних ефектів. Навіть Н1-АГП другого покоління, незважаючи на кращий профіль безпеки завдяки меншій проникності крізь гематоенцефалічний бар’єр порівняно з першим поколінням, можуть спричиняти сонливість, седацію, втомлюваність і головний біль, значно знижуючи працездатність та якість життя пацієнтів з ХСК. У зв’язку з цим пошук оптимальної терапії для ефективного контролю симптомів ХСК без негативного впливу на якість життя є надзвичайно важливим.
Біластин являє собою неседативний піперазиновий Н1-АГП другого покоління, схвалений у 90 країнах світу для лікування кропив’янки й алергічного риніту. Для дорослих рекомендована доза становить 20 мг 1 р/добу. Порівняно з плацебо застосування біластину значно покращує симптоми вже на ранніх етапах лікування (через 1-3 дні). Застосування біластину забезпечує кращий контроль симптомів на початкових стадіях лікування та низьку частоту побічних ефектів, тому перехід на біластин може бути ефективною альтернативою для ведення пацієнтів з ХСК, які не відповідають на стандартні дози Н1-АГП другого покоління.
Матеріали і методи
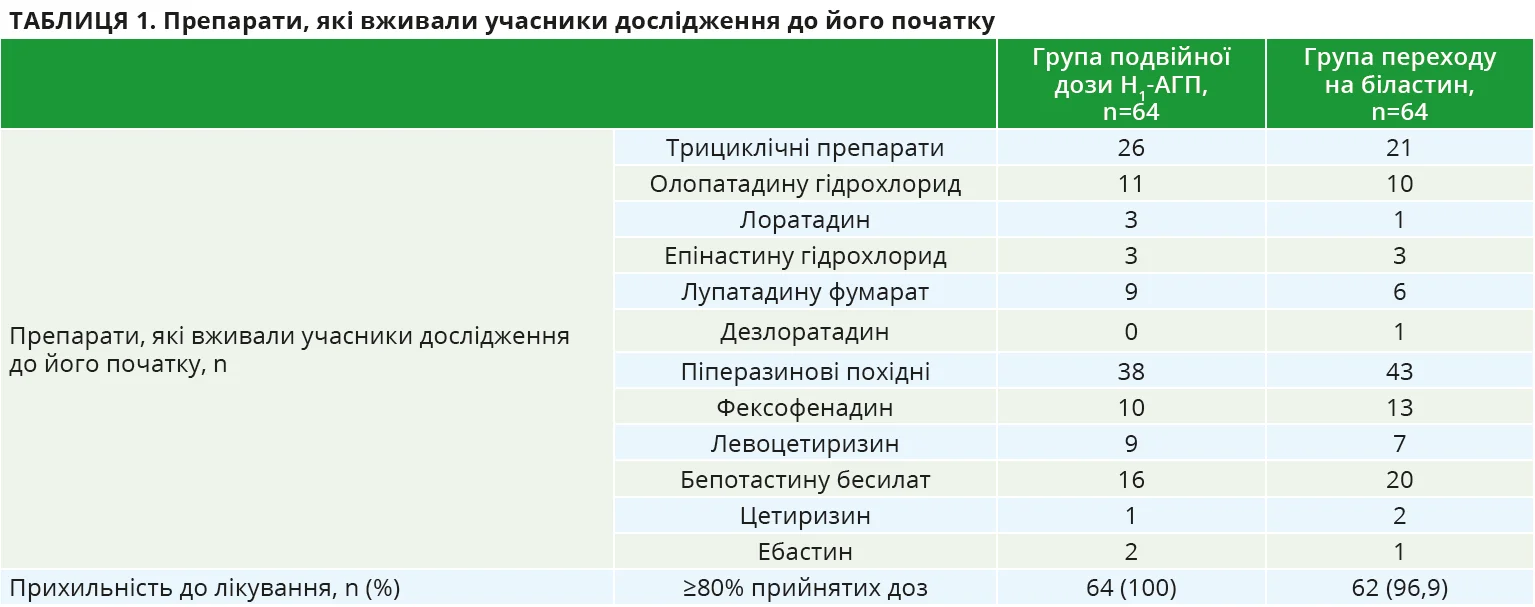
У цьому матеріалі описано багатоцентрове рандомізоване клінічне дослідження IV фази за участю пацієнтів з ХСК, які не відповідали на лікування стандартними дозами Н1-АГП другого покоління, крім біластину. Учасників було рандомізовано в групи переходу на біластин (20 мг/добу) або подвоєння дози попереднього Н1-АГП протягом 7 днів. Первинною кінцевою точкою вважали середню загальну оцінку симптомів (TSS) на 5-7-й день лікування, вторинними кінцевими точками – зміну оцінки за Епвортською шкалою сонливості порівняно з вихідним рівнем, оцінку за шкалою активності кропив’янки (UAS), зміну якості життя тощо. Середній вік учасників групи подвійної дози Н1-АГП становив 52,3±18,4 року, учасників групи біластину – 49,4±18,0 року. До Н1-АГП, які найчастіше приймали пацієнти дослідження, належали олопатадину гідрохлорид, лоратадин, епінастину гідрохлорид, лупатадину фумарат, дезлоратадин, фексофенадин, левоцетиризин, бепотастину бесилат, цетиризин, ебастин (табл. 1).
РЕЗУЛЬТАТИ
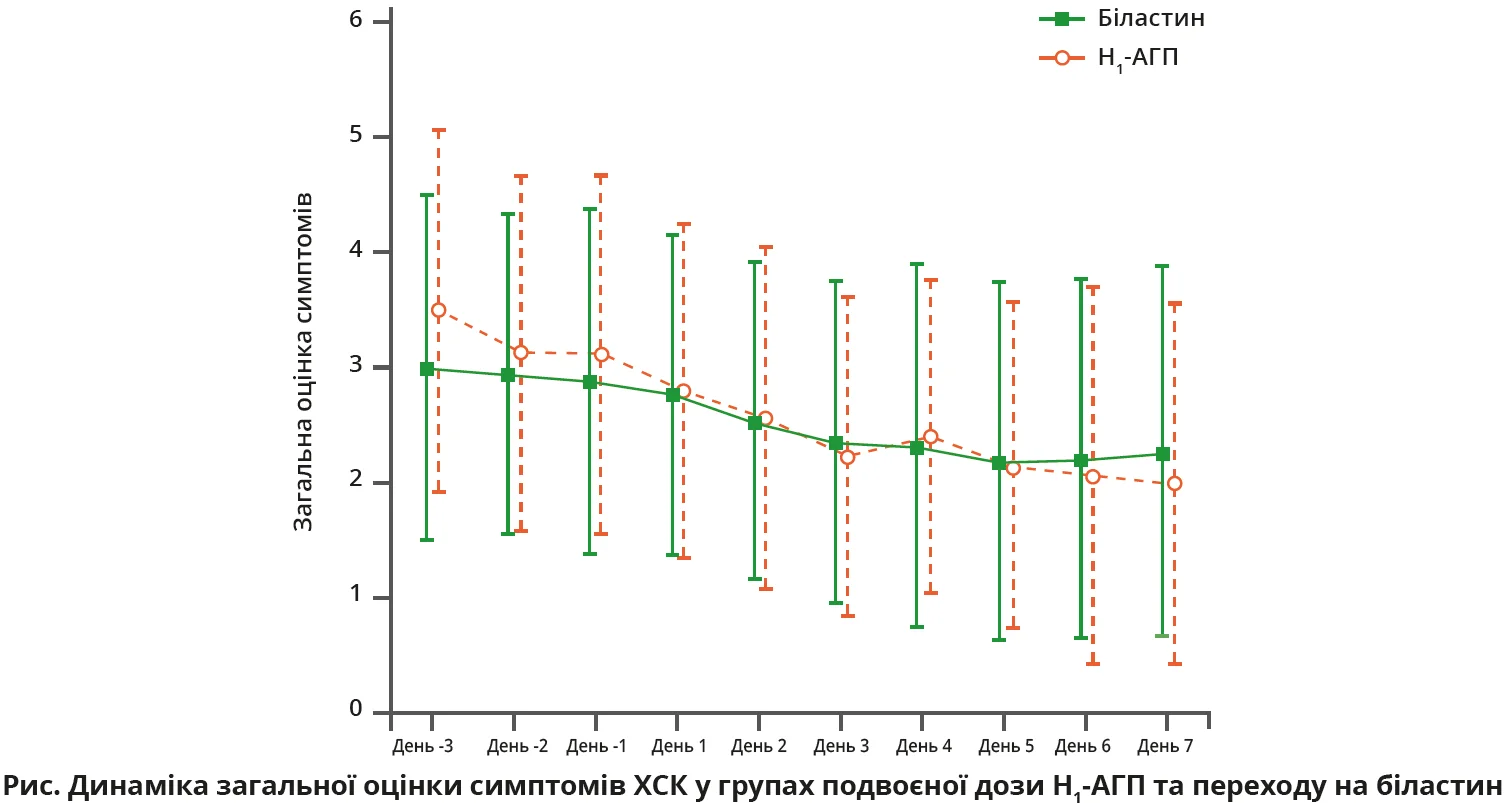
Зміни загальної оцінки симптомів продемонстрували, що перехід на біластин був не менш ефективним, аніж подвоєння дози стартового Н1-АГП. Через 5-7 днів після початку лікування загальна оцінка симптомів знизилася до 0 в 11,3% пацієнтів групи переходу на біластин і в 7,8% пацієнтів групи подвійної дози H1-AГП (рис.). Додатковий аналіз показав, що отримані результати не залежали від статі пацієнтів.
Оскільки було продемонстровано не меншу ефективність біластину порівняно з подвоєнням дози іншого Н1-АГП за середньою загальною оцінкою симптомів через 5-7 днів після початку лікування, було проаналізовано зміни оцінки за Епвортською шкалою сонливості. Хоча обидві тактики продемонстрували зіставний результат, було з’ясовано, що для пацієнтів з оцінкою ≥8 за тестом контролю кропив’янки перехід на біластин може бути доцільнішим у контексті зменшення сонливості.
Для біластину й подвійних доз Н1-АГП другого покоління не було виявлено різниці за динамікою оцінки за шкалою кропив’янки та якістю життя.
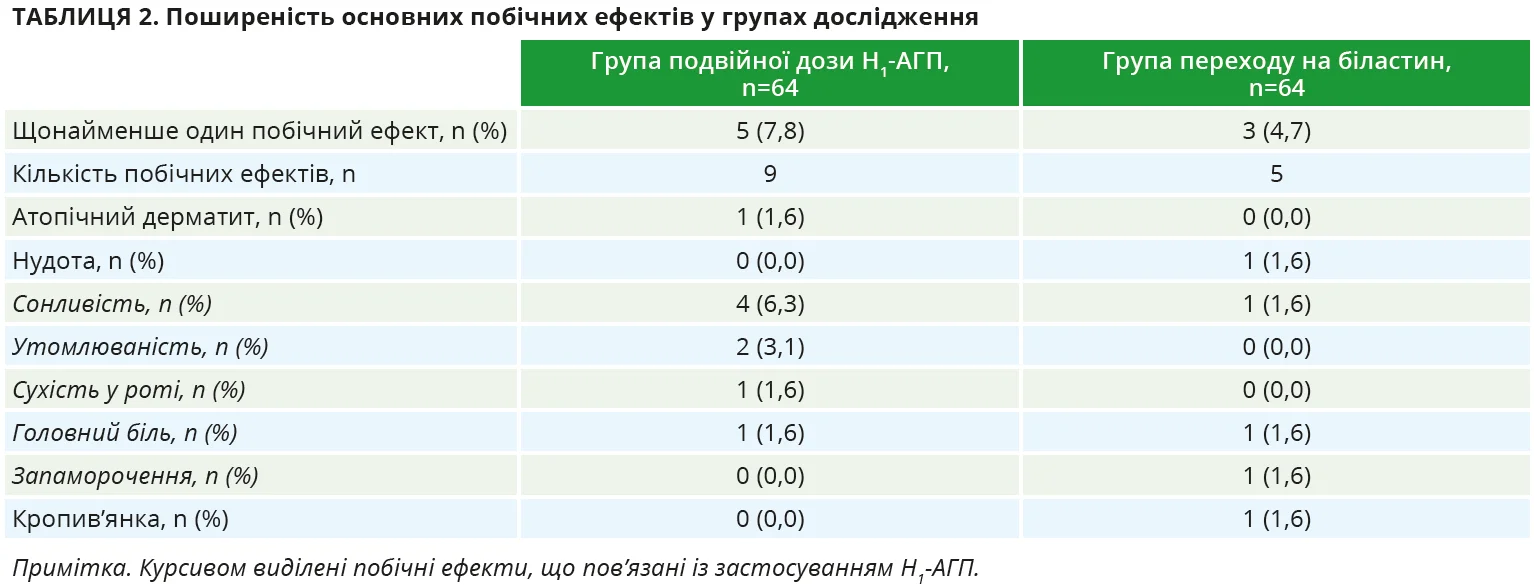
Що стосується безпеки, то тяжких побічних явищ будь-якого виду лікування зафіксовано не було. У групі подвійних доз H1-АГП побічні реакції виникли в 7,8% учасників, а в групі переходу на біластин – у 4,7% учасників. Сонливість, слабкість, сухість у роті, головний біль і запаморочення, потенційно пов’язані з H1-АГП, спостерігалися в 5 осіб групи подвоєння доз (8 проявів) та у 2 осіб групи переходу на біластин (3 прояви) (табл. 2).
Отже, це клінічне дослідження надало переконливі докази безпеки та не меншої ефективності переходу з одного H1-АГП на інший (біластин) порівняно з подвоєнням дози H1-АГП другого покоління в пацієнтів з ХСК, рефрактерних до стандартної дози H1-АГП.
Обговорення
Загалом для пацієнтів з рефрактерною ХСК першим кроком у рекомендованому алгоритмі лікування є підвищення дози Н1-АГП, але як альтернативна терапевтична стратегія розглядається перехід на інший H1-АГП. У цьому багатоцентровому відкритому рандомізованому порівняльному дослідженні з паралельними групами (H1-SWITCH) пацієнтів з ХСК, рефрактерних до H1-АГП (окрім біластину), було рандомізовано у дві групи: групу подвоєння дози вихідного препарату та групу переходу на біластин, по 64 пацієнти в кожній. Як основну кінцеву точку було обрано загальну оцінку симптомів, а як найважливішу вторинну кінцеву точку – оцінку за Епвортською шкалою сонливості. Отримані дані свідчать, що в контексті загальної оцінки симптомів ХСК ефективність переходу на біластин є не меншою, ніж подвоєння дози H1-АГП. За Епвортською шкалою сонливості статистично значущої переваги біластину продемонстровано не було, але показники в обох групах були майже однаковими, що свідчить про порівнянну ефективність обох підходів до терапії. Відмінностей за статтю в ефективності біластину виявлено не було.
Біластин, ключовий препарат у цьому дослідженні, є похідним піперазину, неседативним Н1-АГП другого покоління, схваленим для лікування кропив’янки й алергічного риніту. Клініко-фармакологічне дослідження із застосуванням позитронно-емісійної томографії показало, що одноразове пероральне вживання біластину в дозі 20 мг не призводило до зв’язування цього препарату з H1-рецепторами в головному мозку.
Дослідження ORBIT (Original Real-world cases of Bilastine In Treatment), яке вивчало питання складних для лікування випадків ХСК, показало, що щоденний прийом біластину (10 мг для дітей, 20 мг для дорослих/підлітків) добре переноситься та є ефективним у довготривалому контролі ХСК й індукованої кропив’янки. У разі рефрактерної ХСК рішення щодо використання біластину ґрунтувалося на його неседативних властивостях, економічній доцільності, відмінному профілі безпеки та відсутності імуносупресивних ефектів.
Додатковий аналіз виявив тенденцію до вираженішого зниження загальної оцінки симптомів у групі подвійної дози H1-АГП у пацієнтів з оцінкою за тестом контролю кропив’янки <8 балів, тобто в пацієнтів з гіршим контролем симптомів перевагу може мати подвоєння дози H1-АГП, а не перехід на біластин. Водночас у ході порівняння двох груп за шкалою активності кропив’янки за останні 7 днів істотних відмінностей між групою переходу на біластин і групою подвоєної дози H1-АГП виявлено не було. Ці дані дають змогу зробити висновок, що перехід на біластин є не менш ефективним, аніж терапія подвійною дозою H1-АГП у пацієнтів з рефрактерною ХСК, навіть якщо оцінювати ефективність за іншими показниками, крім загальної оцінки симптомів.
В обох групах відзначалося зіставне покращення якості життя (зниження оцінки за опитувальником DLQI приблизно на 2,5 бали від початкового рівня). При оцінюванні якості життя, пов’язаної зі здоров’ям, було виявлено, що біластин (20 мг) продемонстрував ефективність, подібну до такої левоцетиризину (5 мг), в аспекті зменшення загального дискомфорту та порушень сну, пов’язаних з ХСК. Схожі дані було отримано в ретроспективному дослідженні за участю пацієнтів з ХСК, у якому через 24 тижні лікування біластином було зафіксовано значне покращення якості життя порівняно з початковим показником.
Згідно з попередніми дослідженнями в пацієнтів з ХСК довготривале (протягом 52 тижнів) лікування біластином у дозі 20 мг 1 р/добу виявилося безпечним і добре переносилося. У цьому дослідженні теж не було зафіксовано жодного випадку серйозних небажаних явищ, пов’язаних із впливом на центральну нервову систему. Оцінка за Епвортською шкалою сонливості не продемонструвала переваг переходу на біластин над подвоєнням дози Н1-АГП. Імовірно, ця шкала може не бути належним інструментом для оцінювання сонливості внаслідок застосування H1-АГП і в цій ситуації потрібний специфічніший показник. Однак варто зазначити, що в групі переходу на біластин спостерігалося менше випадків сонливості та загалом менше побічних реакцій, пов’язаних з підвищенням дози H1-АГП. Крім того, при стратифікації за результатом тесту контролю кропив’янки чисельне зменшення оцінки за Епвортською шкалою сонливості в групі біластину було вираженішим у випадках із кращим контролем симптомів (≥8 балів). Це свідчить про те, що перехід на біластин – менш седативну альтернативу – може мати більше переваг стосовно безпеки для пацієнтів з помірно контрольованими симптомами.
Типові для Н1-АГП побічні ефекти – сонливість і втома – відзначалися в 7,8% пацієнтів групи подвійної дози Н1-АГП та в 3,1% учасників групи переходу на біластин. Це узгоджується з результатами попереднього дослідження тих самих авторів, у якому сонливість при застосуванні біластину була зафіксована лише у 2 зі 197 пацієнтів з ХСК (1,0%), що значно нижче, ніж у клінічних дослідженнях інших Н1-АГП другого покоління.
Висновки
Досвід цього дослідження підкреслює важливість урахування всіх можливих побічних реакцій при призначенні терапії H1-АГП, а також необхідність формування клінічних рекомендацій щодо відповідної стратегії їх лікування та профілактики.
Загалом це було перше рандомізоване контрольоване дослідження, котре оцінювало ефективність і безпеку переходу на біластин порівняно з подвоєнням дози H1-АГП у пацієнтів з ХСК, у яких симптоматика зберігалася після приймання звичайних доз Н1-АГП другого покоління, крім біластину. Оскільки ефективність біластину не поступалася ефективності подвоєної дози H1-АГП, а в жодній із груп дослідження не спостерігалося серйозних небажаних реакцій, варто вважати, що перехід на біластин забезпечує такі самі ефективність і безпеку, як і терапія подвоєною дозою H1-АГП. Для оцінювання довгострокових клінічних результатів потрібні подальші дослідження.
Література
Fukunaga A., Kakei Y., Murakami S., et al. Efficacy and safety of switching to bilastine, an H1-antihistamine, in patients with refractory chronic spontaneous urticaria (H1-SWITCH): a multicenter, open-label, randomized, parallel-group comparative study. Front. Immunol. 2024; 15: 1441478. doi: 10.3389/fimmu.2024.1441478.