Новий погляд на механізми патогенезу харчової алергії в дітей. Частина 1.
Імунні сигнатури, пов’язані з розвитком і тяжкістю алергічних реакцій
Переклала й адаптувала Ганна Гаврюшенко
IgE-опосередкована харчова алергія є одним з найпоширеніших алергічних захворювань у дітей і може призводити до небезпечних для життя ускладнень. Пероральна імунотерапія демонструє перспективність як у дослідах, так і на практиці, однак її застосування потребує спеціалізованих умов і кваліфікованого медичного супроводу. Тож наразі сувора елімінаційна дієта залишається основним підходом до лікування більшості дітей з харчовою алергією. Інтенсивний розвиток сучасних методів імунологічних і генетичних досліджень дає змогу глибше вивчати імунні процеси, що лежать в основі алергії, а також зміни імунних реакцій, що відбуваються в процесі пероральної імунотерапії. У цьому матеріалі викладено першу частину ґрунтовного огляду літератури, метою якого була систематизація свіжих наукових даних про нові механізми патогенезу харчової алергії в дітей з акцентом на особливості імунітету, пов’язані з розвитком і тяжкістю алергічних реакцій.
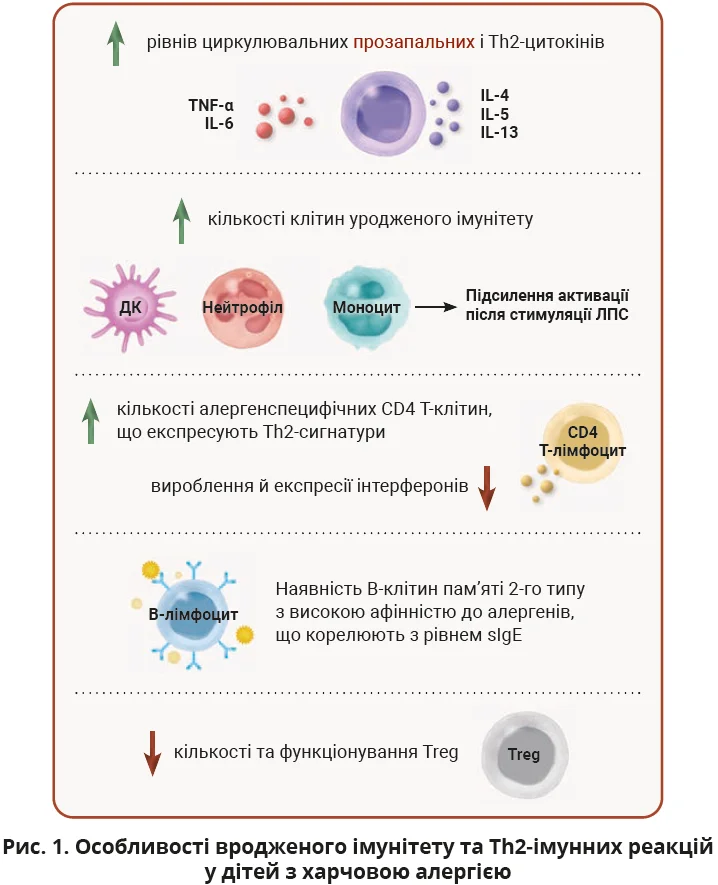
Особливості вродженого імунітету та Тh2-імунних реакцій у дітей з IgE-опосередкованою харчовою алергією
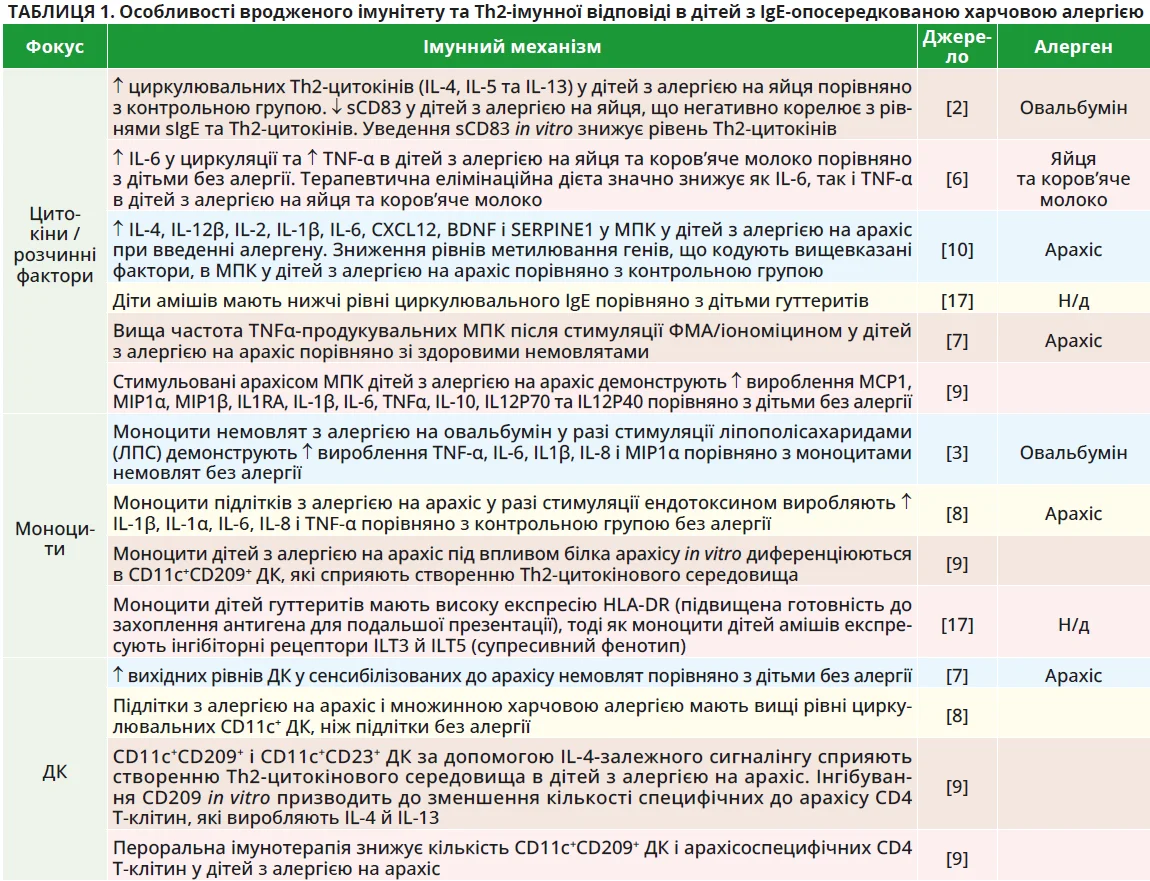
Ціла низка нещодавніх досліджень була спрямована на вивчення імунологічних особливостей дітей з IgE-опосередкованою харчовою алергією, зокрема при алергії на яйця, коров’яче молоко й арахіс (табл. 1). Досліджувалися кількісні характеристики імунних клітин, рівні розчинних медіаторів запалення, а також функціональні властивості клітин in vitro. Особлива увага приділялася вивченню ролі вродженого імунітету й імунним реакціям, опосередкованим Т-хелперами 2-го типу (Тh2), які відіграють ключову роль у формуванні та підтриманні алергічного запалення.
У дослідженні Song і співавт. було виявлено, що діти віком 10-15 років з алергією на яйця (n=20) мали вищі рівні циркулювальних Th2-цитокінів (IL-4, IL-5 та IL-13) і нижчі рівні розчинного імунорегуляторного білка CD83 (sCD83) порівняно з дітьми без алергії. Встановлено негативну кореляцію між умістом sCD83 у плазмі та рівнями Th2-цитокінів і специфічних IgE (sIgE). У дослідженнях in vitro введення sCD83 зменшувало кількість IL-4+CD4+ Т-клітин і знижувало секрецію IL-4, IL-5 та IL-13. На мишачій моделі алергії на яйця було продемонстровано, що sCD83 пригнічує розвиток експериментальної харчової алергії [2].
Дослідження Neeland і співавт. виявило змінений запальний імунний профіль у 1-річних дітей з алергією на яйця (алергічна група: n=16; контрольна група: n=11). Зокрема, в дітей з алергією спостерігалися нижчий уміст циркулювальних T-регуляторних клітин (Treg) CD4+CD25+ і вищий уміст моноцитів. При стимуляції очищених CD14+ моноцитів ліпополісахаридом (ЛПС) in vitro в алергічній групі відзначалося посилення запального фенотипу (а саме підвищення вироблення TNF-α, IL-6, IL-1β, IL-8 і MIP1α) порівняно з моноцитами дітей без алергії [3].
За даними дослідження Lai та співавт., немовлята з алергією (n=21) мали пригнічений розвиток овальбуміноспецифічних Treg і знижену частоту овальбуміноспецифічних В-регуляторних клітин (Breg) порівняно з дітьми без алергії (n=92). Також було виявлено значущу кореляцію між умістом овальбуміноспецифічних CD137+IL-10+ Treg і специфічних до яєць IgG4 у немовлят, у дієту яких були введені яйця у віці 5-10 місяців і які не мали алергії у 12 місяців. Отже, раннє введення яєчного білка може сприяти формуванню толерантності [4].
Два інші дослідження вивчали імунну відповідь у дітей з алергією на коров’яче молоко. У першому, проведеному Lewis і співавт., вивчався вплив епітопів білків коров’ячого молока на мононуклеари периферичної крові (МПК) у дітей з алергією (n=89) порівняно з контрольною групою (n=66). У дітей з алергією було відзначено підвищену частоту реактивних до молока клональних FOXP3+ Treg, які мали підсилену експресію інтерферон-стимульованих генів і дисрегульовану експресію хемокінів (дисфункціональний фенотип Treg) [5]. Окрім того, в дітей з алергією на коров’яче молоко було виявлено невелику популяцію специфічних до молока CD4+ Т-клітин, які експресували гени, пов’язані з патологічними імунними реакціями, опосередкованими Th2 та фолікулярними Т-хелперами.
У дослідженні Kara та співавт. було показано, що діти віком від 1 до 33 місяців (n=37) з алергією на коров’яче молоко та/або яйця мали підвищені рівні циркулювальних IL-6 і TNF-α, а також вищу кількість нейтрофілів порівняно з контрольною групою (n=24). Виключення молока та яєць з раціону сприяло зниженню рівнів IL-6 і TNF-α в дітей з алергією [6].
У низці нещодавніх публікацій досліджуються особливості імунітету дітей з алергією на арахіс.
Зокрема, Neeland і співавт. описали особливості імунних профілів МПК (у спокої та після стимуляції ФMA/іономіцином) у трьох груп 1-річних дітей: з алергією на арахіс (n=12), сенситивізованих, але толерантних до арахісу (n=12) і здорових (n=12) [7]. Сенситивізовані діти мали нижчий початковий рівень наївних CD4+ Т-клітин і CD19highHLA-DRhigh В-клітин, але вищу кількість плазмоцитоїдних дендритних клітин (ДК), тоді як діти з алергією на арахіс мали високу початкову кількість CD19highHLA-DRhigh В-клітин і значне вироблення TNF-α після стимуляції. У групі сенситивізації спостерігався вищий рівень IL-2 у наївних CD4+ Т-клітинах після стимуляції; в групах сенситивізації й алергії на арахіс було виявлено знижену експресію IFN-γ в ефекторних CD4+HLA-DR+ Т-клітинах пам’яті порівняно з контрольною групою. Стимуляція білком арахісу зумовлювала появу більшої кількості арахісореактивних CD4+ Т-клітин з фенотипом пам’яті в дітей з алергією порівняно із сенсибілізованими та здоровими дітьми.
У подальшому дослідженні ці автори виявили, що підлітки з алергією на арахіс (n=20) і з множинною харчовою алергією (n=20) віком 10-14 років мали вищу частку звичайних CD11c+ ДК й активованих Treg з фенотипом пам’яті, ніж підлітки без алергії (n=19). Стимульовані CD4+ Т-клітини в підлітків з алергією виробляли нижчі рівні IL-6, TNF-α й IFN-γ порівняно з контролем. Окрім того, CD14+ моноцити з харчовою алергією демонстрували тенденцію до вищого вироблення IL-1β, IL-1α, IL-6, IL-8 і TNF-α у відповідь на ендотоксин [8].
У дослідженні Zhou та співавт. МПК дітей віком 5-10 років з алергією на арахіс (n=22), стимульовані арахісовим білком, виробляли більше прозапальних цитокінів (MCP1, MIP1α, MIP1β, IL-1RA, IL-1β, IL-6, TNF-α, IL-10, IL-12p70 та IL-12p40) порівняно з контролем (n=26; вік – 4-13 років). Стимуляція алергеном також зменшувала частку моноцитів у дітей з алергією на арахіс, оскільки вони диференціювалися в CD11c+CD209+ ДК, здатні захоплювати арахісовий антиген. Процес диференціації був залежним від сигналінгу через рецептор IL-4 та наявності CD4+ Т-клітин, що виробляють IL-4 й IL-13. Зворотний зв’язок між CD11c+CD209+ ДК і специфічними CD4+ Т-клітинами свідчив про їхню взаємодію в індукції алергії [9].
В іншій публікації Zhou та співавт. описали епігенетичні відмінності між парами ідентичних близнюків, де один з них мав алергію на арахіс. У дітей з алергією відзначалися знижене метилювання ДНК у локусах генів IL4, IL2, IL17F, IL1B, IL6, BDNF, CCR7, CD3E та SERPINE1, а також підвищене метилювання в ділянках IL12B, CXCL12 і RUNX. Стимулювання МПК арахісовим білком спричиняло збільшення вироблення відповідних прозапальних білків (IL-4, IL-12β, IL-2, IL-1β, IL-6, CXCL12, BDNF, SERPINE1) у дітей з алергією [10]. Подальші епігенетичні та транскриптомні дослідження виявили унікальні, асоційовані з алергією патерни метилювання й експресії ДНК у генах, що регулюють розвиток В- і Т-клітин, Th1/Th2-диференціацію, сигналінг інтерферону та вироблення цитокінів [11-13].
Дослідження Wang і співавт. показало, що анти-CD3/CD28-стимульовані МПК осіб віком від 2 до 20 років (n=33) з алергією на арахіс характеризуються високою експресією стероїдогенного ферменту CYP11A1, підвищеним рівнем мРНК IL-13 та IL-4, а також вищою частотою CD4+IL-13+ Т-лімфоцитів порівняно з контрольною групою (n=11). Роль CYP11A1 в індукції Th2-відповіді була підтверджена за допомогою експериментального інгібування та CRISPR-нокауту CYP11A1 in vitro, що призводили до зниження кількості CD4+IL-13+ Т-клітин [14].
Нещодавно було показано, що В-клітини пам’яті також модулюють алергічне середовище, стимулюючи Th2-імунітет у дітей з харчовою алергією на арахіс [15]. Популяція В-клітин пам’яті, що характеризується експресією CD23 й IgG1, містить високоафінні клони В-клітин, які здатні перемикатися на синтез IgE при активації та корелюють з рівнем циркулювального IgE в дітей з алергією на арахіс [16]. За даними scRNA-Seq і парного секвенування рецепторів В-лімфоцитів (BCR-Seq) цієї популяції клітин було виявлено високу експресію регуляторних генів IL-4 й IL-13, а також високу афінність BCR до основного алергенного білка арахісу Ara h 2.
Це свідчить про те, що вказана підгрупа В-клітин готова до активації та перемикання класу антитіл у разі контакту з арахісовим антигеном, що потенційно сприяє тривалій персистенції алергії на арахіс.
Останні дослідження також аналізували вплив довкілля на розвиток алергічних захворювань. Зокрема, в публікації Hrusch і співавт. продемонстровано, що діти з релігійної спільноти гуттеритів віком 6-14 років (n=30), які зростали в сучасному сільськогосподарському середовищі, мають більш реактивну та попередньо активовану імунну систему, а також підвищений ризик розвитку атопії й астми порівняно з дітьми зі спільноти амішів аналогічного віку (n=30), що проживають у традиційному аграрному середовищі [17]. Реактивніший імунний фенотип дітей гуттеритів характеризується моноцитами з підвищеною готовністю до розпізнавання антигенів (висока експресія HLA-DR), активованими популяціями Т-лімфоцитів (CD4+, що експресують CD127, CD28 або ICOS) і нижчою частотою активованих ICOS+ Treg. Натомість діти амішів мали нижчі рівні циркулювального IgE, більш «супресивні» моноцити з високою експресією інгібіторних рецепторів ILT3 й ILT5, вищу частку CD4+ Т- і Treg-клітин, що експресують інгібіторну молекулу PD-1, а також більшу кількість CD28-негативних CD8+ Т-клітин і підсилене вироблення IFN-γ Т-клітинами. Такий менш реактивний імунний фенотип, імовірно, сприяє нижчій захворюваності на алергію серед дітей амішів.
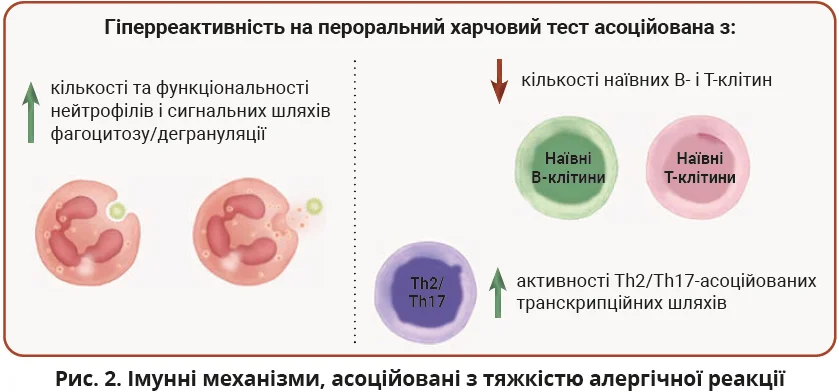
Імунні механізми, асоційовані з тяжкістю алергічної реакції
У трьох свіжих публікаціях вивчався взаємозв’язок особливостей імунної системи та тяжкості перебігу харчової алергії на арахіс у дітей (табл. 2). Зокрема, в дослідженні Do та співавт. визначалася тяжкість алергічних реакцій у дітей під час пероральної провокаційної проби з арахісом. Оцінка проводилася за шкалою, що охоплювала респіраторні, шлунково-кишкові, шкірні, серцево-судинні та кон’юнктивальні симптоми. Транскриптомний аналіз зразків цільної крові, зібраних під час харчової провокаційної проби в дітей віком 7-17 років (основна когорта: n=21, реплікаційна когорта: n=19), виявив 318 генів, пов’язаних з тяжкістю реакції, які були спільними для обох когорт. Аналіз сигнальних шляхів показав, що ці гени переважно асоційовані з функціями нейтрофілів, зокрема фагоцитозом, активацією та дегрануляцією. Аналіз транскриптомних даних продемонстрував позитивну кореляцію між тяжкістю реакції та підвищеною часткою нейтрофілів, а також зниженням кількості наївних В-клітин і наївних CD4+ Т-клітин. Окрім того, аналіз метилювання ДНК у CD4+ Т-клітинах виявив 203 CpG-сайти (що охоплюють 197 унікальних генів), які пов’язані з тяжкістю алергічних реакцій [18].
У другому дослідженні Zhang і співавт. виявили сильну кореляцію між кількістю нейтрофілів у зразках цільної крові та тяжкістю реакцій на харчовий провокаційний тест з арахісом у дітей віком 4-14 років (n=105). Транскриптомний аналіз показав, що вищі рівні нейтрофілів були пов’язані зі збагаченням сигнальних модулів, пов’язаних з FCγR-опосередкованим фагоцитозом і TLR- сигналізацією. Було ідентифіковано п’ять ключових генів-драйверів цих модулів: AP5B1, KLHL21, VASP, TPD52L2 та IGF2R [19].
Третє дослідження, проведене Ruiter і співавт., охоплювало як дорослих, так і дітей (n=62; середній вік – 17 років) і також використовувало провокаційну пробу з поступовим підвищенням дози арахісу для оцінювання тяжкості реакцій. Стимуляція МПК арахісовим білком у реактивних учасників призводила до збільшення вироблення Th2-цитокінів (IL-4, IL-5, IL-9, IL-13), підвищення частоти арахісоспецифічних CD154+CD4+ Т-клітин, а також зростання числа клонів Т-клітин з носійством специфічних до арахісу CDR3. У CD154+CD4 Т-клітинах реактивних учасників відзначалася вища експресія генів, асоційованих з Th2-ланкою (IL-5, IL-9) і Th17-ланкою (IL-22, IL-26), порівняно з гіпореактивними учасниками. Водночас у гіпореактивних учасників виявляли нижчий рівень експресії генів, пов’язаних з функцією Т-регуляторів (TNFRSF9, CD137) та імунною регуляцією (NFKBID, IL1RN, BDR).
За даними дослідження розподілу арахісоспецифічних CDR3 у популяціях CD25+CD127+ Т-ефекторних і CD25+CD127− Т-регуляторних клітин, у реактивних учасників частка специфічних CDR3 була зміщена в бік Т-ефекторної, а не Т-регуляторної популяції, що може свідчити про імунний дисбаланс, пов’язаний з тяжкістю алергічної реакції [20].
Література
Gubbels L., Saffery R., Neeland M.R. New insights into the mechanisms of childhood food allergies. Pediatr. Allergy Immunol. 2025; 36: e70069. doi: 10.1111/pai.70069.