Результати дослідження OMRIA RWE: пероральний бактеріальний лізат OM-85 запобігає інфекціям дихальних шляхів при астмі
Переклала й адаптувала канд. мед. наук Ольга Королюк
Респіраторні інфекції (РІ) є важливою проблемою охорони здоров’я із серйозними клінічними й економічними наслідками. Бронхіальна астма вражає понад 300 мільйонів людей у світі й асоціюється з підвищеною схильністю до рецидивних РІ. Переважна більшість РІ в цій когорті зумовлена різними підтипами риновірусів людини (HRV), аденовірусів (HAdV), коронавірусів (наприклад, SARS-CoV-2), вірусів грипу (IFV) та респіраторно-синцитіальних вірусів (RSV). Бактеріальні патогени, особливо в разі синуситу або пневмонії, також відіграють вирішальну роль у загостренні РІ.
Рецидиви РІ спричиняють зниження функції легень і погіршення якості життя пацієнтів, будучи тригерами загострень астми; їх лікування становить ≈80% загальних витрат на лікування астми. Надмірне використання антибіотиків асоціюється з антибіотикорезистентністю, дисбактеріозом, що погіршує імунний захист і посилює ризик атопії. Крім того, РІ часто є причиною ескалації терапії астми, зокрема призначення пероральних кортикостероїдів (КС), які мають широкий спектр побічних ефектів. Отже, профілактика РІ має значення для покращення лікування астми та зменшення витрат на охорону здоров’я.
Сучасні стратегії боротьби з РІ насамперед передбачають вакцинацію. Проте неповне охоплення вакцинацією, нестабільна ефективність і відсутність вакцин проти багатьох респіраторних вірусів підкреслюють потребу в альтернативних підходах. Згідно з «гігієнічною гіпотезою» вплив мікробних продуктів, зокрема бактеріальних лізатів, може зміцнити імунний захист і зменшити частоту РІ.
OM-85 – це пероральний препарат ліофілізованих бактеріальних лізатів 8 поширених респіраторних патогенів: Haemophilus influenzae, Diplococcus pneumoniae, Klebsiella pneumoniae, Klebsiella ozaenae, Staphylococcus aureus, Streptococcus pyogenes, Streptococcus viridans і Neisseria catarrhalis. У дослідженнях in vitro, на тваринних моделях і в клінічних випробуваннях OM-85 продемонстрував противірусні й імуномодулювальні властивості. Отже, OM-85 здатний убезпечити від широкого спектра респіраторних вірусів, включно з HRV, IFV, RSV та SARS-CoV-2. Препарат продемонстрував ефективність у профілактиці РІ в дітей і вразливих групах дорослих, зокрема в пацієнтів із хронічним бронхітом, хронічним обструктивним захворюванням легень і пацієнтів на гемодіалізі. Проте дані щодо ефективності OM-85 у профілактиці рецидивів РІ в дорослих з астмою обмежені.
Реальну ефективність OM-85 як додаткової терапії в дорослих з алергічною астмою фенотипу T2-high оцінювало дослідження OMRIA RWE.
Методи
Дизайн дослідження
OMRIA RWE – багатоцентрове обсерваційне контрольоване когортне дослідження з реальної клінічної практики IV фази, проведене в 3 різних алергологічних відділеннях у Греції. Учасниками були пацієнти з алергічною астмою середнього-тяжкого ступенів з документованими регулярними спостереженнями що 3 місяці впродовж ≥12 місяців до початку дослідження (дані від серпня 2021 р. до липня 2023 р. були зібрані ретроспективно) та впродовж дослідження. Метою було оцінити, чи додавання OM-85 до стандартної терапії (СТ) астми здатне зменшити кількість і тяжкість клінічних епізодів, що свідчать про РІ в цій когорті. Для забезпечення конфіденційності всі дані пацієнтів були анонімними, кожен учасник підписував інформовану згоду.
Пацієнти
До участі в дослідженні допускали дорослих віком 18-80 років зі встановленим діагнозом алергічної астми середнього або тяжкого ступеня («тяжка для лікування астма»). Пацієнти отримували СТ 4-го кроку GINA та мали добрий контроль симптомів – бал >19 за тестом контролю астми (ACT – Asthma Control Test). Незважаючи на добрий контроль, у них спостерігалися часті загострення за попередні 12 місяців – принаймні 2 легких-помірних або ≥1 тяжке документоване загострення, що потребувало госпіталізації.
СТ включала:
1) терапію 4-го кроку за GINA: будесонід 200 мкг + формотерол 6 мкг на інгаляцію як підтримувальна терапія (2 інгаляції двічі на день), а також за потреби для полегшення симптомів (стратегія MART);
2) профілактичні щеплення, зокрема щорічну вакцинацію проти грипу (анти-IFV), пневмококову кон’юговану вакцину (PCV13) та 3 дози вакцини проти COVID-19 (Pfizer-BioNTech);
3) лікування супутніх захворювань і модифікованих чинників ризику для зменшення загострень.
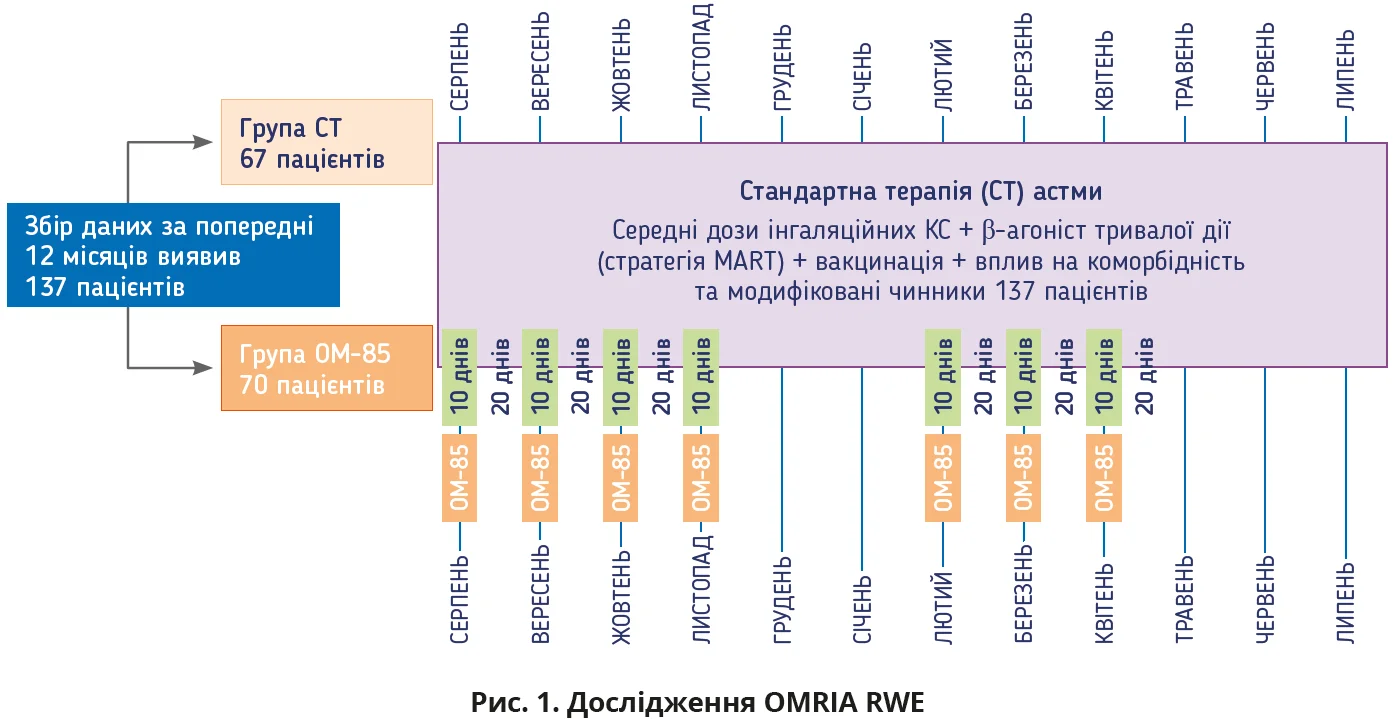
За рекомендаціями лікаря частина пацієнтів додатково отримувала OM-85, щоб запобігти рецидивам РІ й уникнути загострень астми. Терапія OM-85 передбачала пероральне приймання 1 капсули 7 мг на день протягом 10 днів щомісяця; загалом було 2 тримісячні курси (серпень – жовтень і лютий – квітень) із 2 тримісячними перервами (листопад – січень і травень – липень).
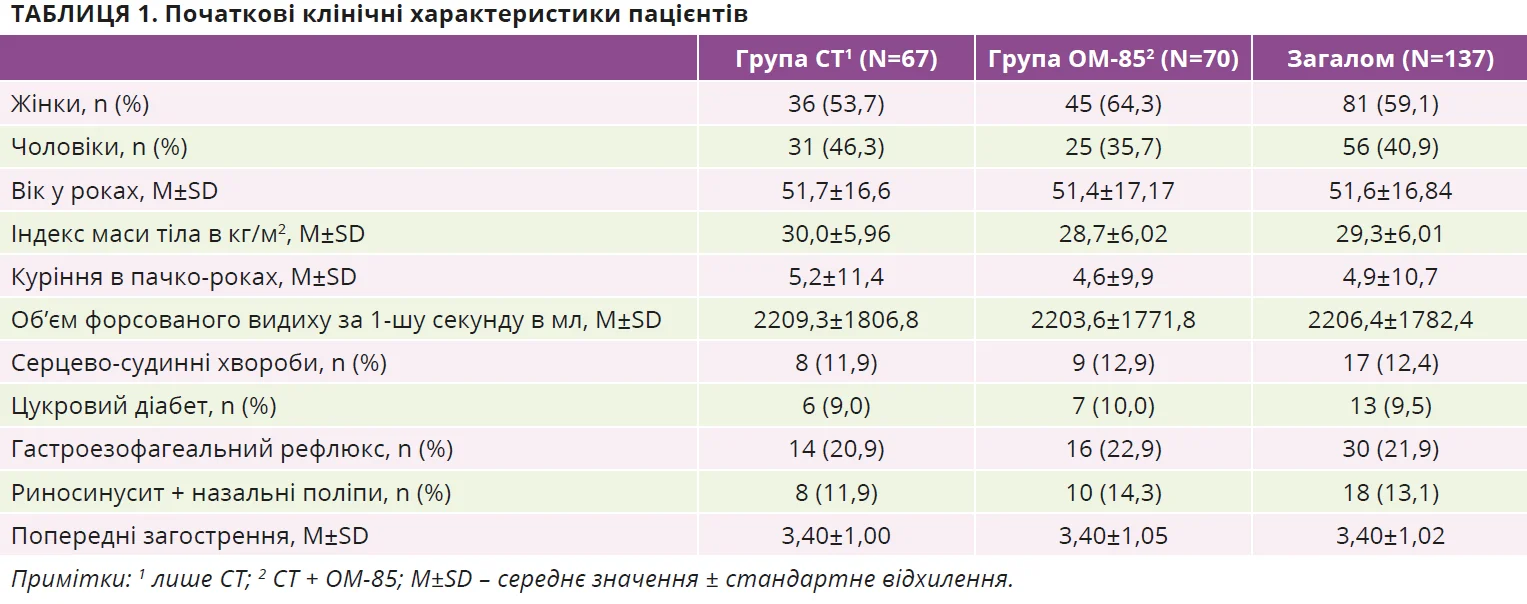
Початкові клінічні характеристики пацієнтів представлено в таблиці 1. Основним критерієм вилучення було застосування пероральних КС або інших імуносупресантів.
Процедури
Для визначення пацієнтів, які відповідають критеріям залучення, використовували аналітичну систему MedExpress. Усі зареєстровані клінічні епізоди респіраторних симптомів (табл. 2) зі встановленим лікарем діагнозом РІ впродовж 12 місяців (від серпня 2022 р. до липня 2023 р.) отримано з медичних карток пацієнтів. Тяжкість клінічних епізодів оцінювали за 3-бальною шкалою, вказуючи середній індекс тяжкості (mSI): 1 – легкий епізод (легка закладеність носа чи нежить, які не впливають на повсякденну діяльність); 2 – помірний епізод (симптоми, що впливають на повсякденну діяльність, але не порушують сон); 3 – тяжкий епізод (труднощі зі сном і диханням).
Оскільки анамнез попередніх загострень є важливим чинником, що збільшує ризик майбутніх загострень, реєструвалися всі загострення астми за 12 місяців до початку застосування OM-85 і через 12 місяців після цієї дати. Клінічно значуще загострення астми визначалося як початок та/або погіршення хронічних симптомів з боку дихальних шляхів, що спричиняло клінічно значущий дистрес або порушення в соціальних, професійних чи інших важливих сферах функціонування та потребувало будь-якої з таких дій: а) застосування системних КС протягом ≥3 днів; б) збільшення підтримувальної дози пероральних КС протягом ≥3 днів або одноразова депо-ін’єкційна доза КС; в) візит до відділення невідкладної допомоги, що потребував застосування системних КС; г) госпіталізація. Інформацію щодо призначення антибіотиків та/або циклів пероральних КС, загострень астми, позапланових візитів і госпіталізації також отримували з медичних записів. Окрім того, в системі електронних рецептів Національної системи охорони здоров’я проводився пошук рецептів на антибіотики та/або системні КС, а також будь-яких візитів до відділення невідкладної допомоги чи госпіталізацій, не зазначених у медичних картках учасників дослідження. Знайдені дані додавалися до медичних карток і використовувалися для аналізу результатів. Потім пацієнтів розподілили на дві групи: СТ й OM-85, до якої увійшли пацієнти, котрі додатково отримували OM-85 (рис. 1).
Первинними кінцевими точками дослідження були:
1) загальна кількість клінічних епізодів, що вказують на РІ;
2) тяжкість клінічних епізодів у кожній групі впродовж 12 місяців.
Вторинні кінцеві точки включали загальну кількість загострень астми, циклів пероральних КС і антибіотиків, а також кількість позапланових візитів і госпіталізацій у кожній із груп.
Статистичний аналіз
Для оцінювання впливу лікування препаратом OM-85 на всі первинні та вторинні кінцеві точки використовувався аналіз регресії Пуассона. Для оцінювання параметра надмірної дисперсії застосовувався аналіз негативної біноміальної регресії. Великі значення параметра надмірної дисперсії вказують на відсутність значної дисперсії; в такому разі регресія Пуассона є адекватною для оцінювання ефекту лікування. Для безперервних даних використовувалася лінійна регресія.
Моделі Пуассона та негативної біноміальної регресії були зваженими. Ваги були отримані з балів схильності, оцінених методом логістичної регресії з урахуванням віку, індексу маси тіла, тривалості куріння, об’єму форсованого видиху за 1-шу секунду, попередній 12-місячний анамнез загострень астми й анамнез супутніх захворювань (серцево-судинних, діабету, гастроезофагеального рефлюксу, риносинуситу з назальними поліпами). Ефект лікування відображав середній ефект лікування в популяції.
Результати
За період від серпня 2022 р. до липня 2023 р. критеріям залучення відповідали 137 дорослих. Оскільки це було дослідження даних з реальної клінічної практики, пацієнти мали чинники, які підвищують ризик загострень, навіть за умови належного контролю симптомів астми: куріння, хронічний риносинусит з назальними поліпами та гастроезофагеальний рефлюкс (табл. 1). Крім того, всі пацієнти були сенсибілізовані до цілорічних або сезонних алергенів. Згідно з медичними записами 67 пацієнтів отримували лише СТ (група СТ), 70 пацієнтів додатково отримували препарат OM-85 (група OM-85). Дотримання графіка лікування, про яке повідомляли пацієнти, з відповідним підтвердженням у системі електронних рецептів було подібним в обох групах. Повідомлень про серйозні побічні ефекти не було; жоден з побічних ефектів не призвів до припинення терапії. Найчастішими побічними ефектами в групі OM-85 буди легкі шлунково-кишкові розлади (2,3%).
Первинні результати
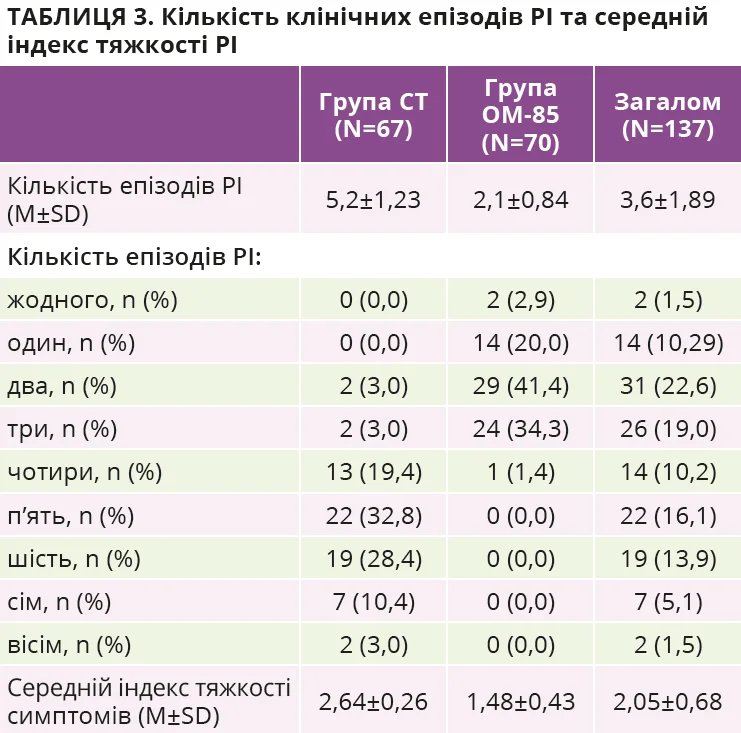
Упродовж 12 місяців дослідження в усіх пацієнтів часто виявляли клінічні епізоди РІ (в середньому 3,6±1,89). Проте в пацієнтів із групи СТ їх кількість була вищою, ніж у групі OM-85 (5,2±1,23 проти 2,1±0,84). У групі OM-85 спостерігалося статистично значуще зниження середньої кількості РІ на 60,1% (P <0,0001) протягом 12-місячного періоду (табл. 3).
Тяжкість клінічних епізодів РІ
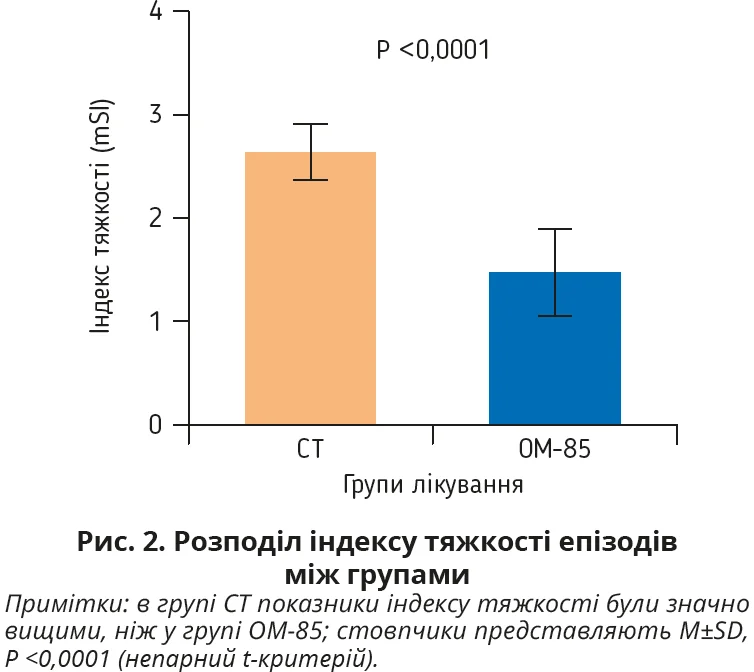
У досліджуваній популяції відзначено коливання тяжкості респіраторних симптомів. У пацієнтів із групи СТ респіраторні симптоми були тяжчими: mSI становив 2,64±0,26 порівняно з 1,48±0,43 у групі OM-85 (табл. 3). У пацієнтів, які отримували OM-85, спостерігалося статистично значуще (P <0,0001) зниження mSI на 1,17 одиниці (рис. 2).
Вторинні кінцеві точки
Загострення астми
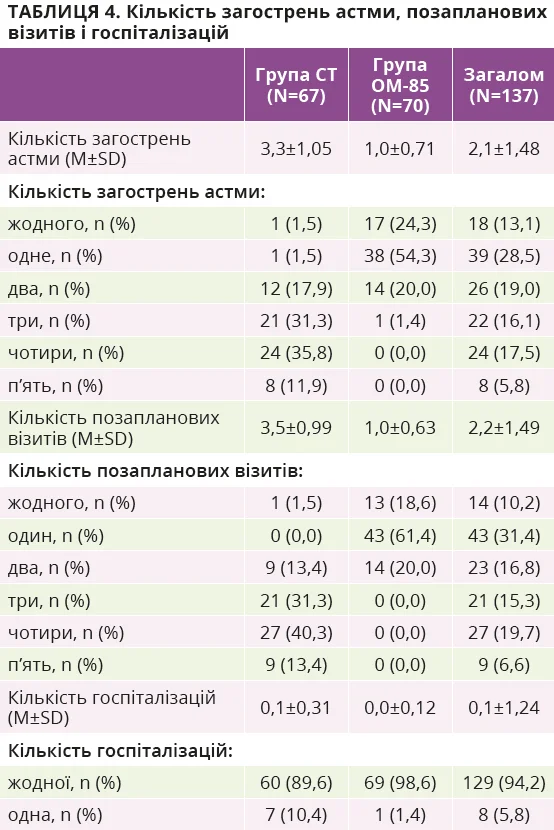
В учасників спостерігалися часті загострення: 2,1±1,48 на пацієнта (табл. 4). Проте в групі OM-85 загострень було менше, ніж у групі СТ (1,0±0,71 проти 3,3±1,05). Упродовж 12 місяців у групі ОМ-85 спостерігалося статистично значуще зниження середньої кількості загострень астми на 71% (P <0,0001), незважаючи на відсутність істотної різниці в попередньому анамнезі загострень астми між групами (табл. 1).
Незаплановані візити та госпіталізації
Пацієнти групи OM-85 мали менше позапланових візитів, аніж у групі СТ (1,0±0,63 проти 3,5±0,99), тобто статистично значуще зниження середньої кількості позапланових візитів на 72,4% (P <0,0001) впродовж дослідження (табл. 4). В обох групах лікування зареєстровано лише 8 госпіталізацій (5,8%), але в групі OM-85 не потребували госпіталізації 98,6% пацієнтів, а в групі СТ – 89,6% (табл. 4). Отже, в групі OM-85 спостерігалося статистично незначуще зниження середньої кількості госпіталізацій на 91,6% (P=0,058).
Цикли пероральних КС і антибіотиків
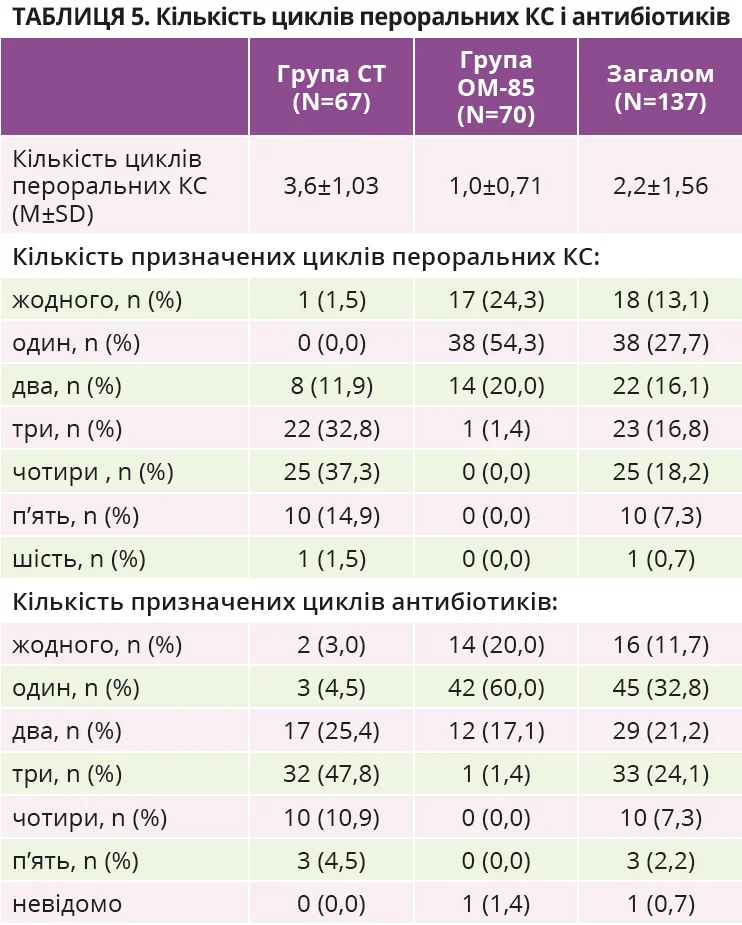
Пацієнтам із групи OM-85 виписано менше рецептів на пероральні КС і антибіотики (1,0±0,71та 1,0±0,66 відповідно проти 3,6±1,03 та 2,8±1,00 у групі СТ). Отже, в групі OM-85 спостерігалося статистично значуще (обидва P <0,0001) зниження середньої кількості циклів пероральних КС і антибіотиків на 73 та 66,6% відповідно (табл. 5).
Обговорення
Хоча всі учасники дослідження були вакциновані проти грипу, пневмококової інфекції та SARS-CoV-2, часто повідомлялося про клінічні епізоди, що вказують на РІ; лише 2 пацієнти (1,5%) не мали жодного епізоду РІ впродовж дослідження (табл. 3).
Запальні зміни в дихальних шляхах пацієнтів з алергічною астмою підвищують схильність до повітряно-крапельних інфекцій, оскільки патогени знаходять сприятливе мікросередовище в набряклих і вузьких бронхах. Існують численні докази аномальної вродженої імунної відповіді в пацієнтів з астмою, що зумовлює повільніший кліренс патогенів і більшу схильність до РІ. Ймовірно, первинний дефект є на першому етапі індукції противірусних захисних цитокінів (інтерферонів β та λ) після виявлення вірусних компонентів рецепторами розпізнавання образів (PAMP). Окрім того, дихальні шляхи пацієнтів з астмою демонструють вищу схильність до пошкоджень і повільніше відновлення після зовнішніх впливів.
Також у пацієнтів з астмою спостерігається недостатнє формування щільних контактів епітелію. Взаємодія Т-клітин в епітелії та дія алергенів (наприклад, протеаз), забруднювачів, вірусів, які порушують функції щільних контактів, іще більше посилюють підвищену проникність.
Більшість дослідників погоджуються, що в пацієнтів з астмою РІ спричиняють довшу тривалість хвороби та посилюють тяжкість симптомів з боку нижніх дихальних шляхів. У цьому дослідженні середні показники mSI становили 2,05±0,68, тобто помірні-тяжкі симптоми, які спричиняли значні денні та нічні порушення (табл. 3).
Після РІ перебіг алергічної астми зазвичай тяжчий, аніж неалергічної астми. Оцінювання реакції на HRV-інфекцію в пацієнтів з астмою виявило, що вірусологічні та клінічні наслідки тісно пов’язані з дефіцитом інтерферону-γ й інтерлейкіну-10 (ІЛ-10), а також зі збільшенням генерації цитокінів Th2 – ІЛ-4, IЛ-5 та ІЛ-13. Це свідчить про зв’язок між алергічною сенсибілізацією, запаленням з високим рівнем T2 і схильністю до вірусних інфекцій.
Обґрунтування перорального застосування імуномодуляторів для профілактики рецидивів РІ базується на концепції кишково-легеневої імунної осі. Зокрема, OM-85 впливає на численні компоненти вроджених і адаптивних імунних відповідей, що сприяє зниженню частоти та тяжкості РІ.
В експерименті на дендритних клітинах кісткового мозку мишей дикого типу встановлено, що OM-85 діє як PAMP, посилюючи противірусну сигналізацію 1-го типу й індукуючи секрецію інтерферону-β. Крім того, OM-85 діяв як праймінг-сигнал для інфламасом NLRP3 й AIM2, які є ключовими платформами для виявлення та захисту від вірусних інфекцій.
Ці інфламасоми допомагають підтримувати вроджені імунні клітини в стані готовності, що характеризується здатністю вивільняти велику кількість IЛ-1β при виявленні запальних тригерів, тим самим зменшуючи інфекції. Проте OM-85 не призводить безпосередньо до вивільнення IЛ-1, що важливо, зважаючи на негативний вплив осі NLRP3/IL-1 за хронічних запальних захворювань.
Після інтраназального введення OM-85 піддослідним мишам виявлено підвищення експресії гена, який кодує клаудин-1 – білок щільних контактів, критично важливий для функції епітеліального бар’єра, що свідчить про прямий бар’єрозміцнювальний ефект. Окрім того, є дані, що OM-85 формує в легенях середовище, сприятливе для розвитку толерантності, що асоціюється з пригніченням експериментальної астми.
У дослідженні OMRIA RWE додавання OM-85 до СТ асоціювалося зі значним зниженням загальної кількості клінічних епізодів РІ, а також з легшим перебігом хвороби (значно нижчий mSI).
Спільне введення OM-85 і вакцин проти поширених респіраторних патогенів добре переносилося, без документованих доказів збільшення місцевих або системних побічних ефектів або виникнення тяжких побічних ефектів. Одночасне введення OM-85 і вакцини проти грипу для оптимізації ефективності стратегій профілактики вже було оцінено та рекомендовано. Проте необхідні спеціальні дослідження, щоб поширити таку рекомендацію на вакцини проти COVID-19 і пневмококової інфекції.
Дослідження OMRIA RWE вперше в реальних умовах оцінило ефективність OM-85 щодо зменшення кількості РІ в дорослих з алергічною астмою фенотипу T2-high, що важко піддається лікуванню. Одним з найпослідовніших висновків клінічних досліджень є те, що алергія та вірусні інфекції синергічно збільшують ризик загострень. У дослідженні OMRIA RWE імунні модифікації, спричинені OM-85, пригнічували провокування загострень, що сприяло зменшенню кількості незапланованих візитів, госпіталізацій, використання курсів пероральних КС і антибіотиків.
Висновки OMRIA RWE узгоджуються з результатами іншого відкритого проспективного дослідження з послідовним дизайном за участю 84 пацієнтів віком 16-65 років з алергічним ринітом, астмою та хронічним обструктивним захворюванням легень, які перенесли ≥3 РІ впродовж року до початку дослідження. Призначення OM-85 як доповнення до СТ супроводжувалося значущим зниженням загальної кількості РІ та загострень (Koatz A. et al., 2016).
Пікові сезони загострень астми фіксуються восени й навесні. Восени РІ найчастіше виявляються у вересні. «Вереснева епідемія» насамперед пов’язана з поверненням дітей до школи та впливом вірусів і алергенів, що передаються повітряно-крапельним шляхом. Потім РІ поширюються на інших членів родини, особливо людей похилого віку та вразливих осіб. Весняне загострення зумовлене високою захворюваністю на РІ, що підсилюється дією пилку.
У дослідженні OMRIA RWE препарат OM-85 призначався двічі на рік за кілька тижнів до пікових сезонів РІ з метою стимуляції імунної системи для зменшення частоти та тяжкості РІ. Такий підхід продемонстрував ефективність у пацієнтів, сенсибілізованих до цілорічних алергенів. Позитивні наслідки такої практики пояснюються висновками експериментального дослідження, котре вивчало вплив OM-85 на ізольовані клітини епітелію дихальних шляхів людини від пацієнтів з астмою. Виявлено, що OM-85 активує два сигнальні шляхи – Erk1/2MAPK та цАМФ, покращуючи виживання епітеліальних клітин, інфікованих HRV. Проте профілактичний ефект OM-85 був значущим лише після попередньої інкубації клітин з OM-85 протягом 48 годин, що вказує на залежність захисного ефекту від часу (Roth M. et al., 2017). Отже, профілактичне лікування препаратом OM-85 є ефективним проти інфекційних і алерген-індукованих уражень за умови призначення за кілька тижнів до сезону піку РІ та/або впливу алергенів.
Дослідження OMRIA RWE має декілька обмежень. Хоча результати вказують на сильний зв’язок між OM-85 і зниженням частоти РІ та загострень, ретроспективний характер дослідження обмежує можливість робити причинно-наслідкові висновки. Для їх підтвердження й оцінювання довгострокової ефективності OM-85 потрібні подальші проспективні випробування. Крім того, дослідження не включало лабораторних даних, але ідентифікація РІ ґрунтувалася на суворій клінічній оцінці, відображаючи повсякденну практику в первинній ланці медичної допомоги.
Зазначені обмеження компенсуються наданням доказів з реальної клінічної практики, що забезпечує більшу репрезентативність цільової клінічної популяції.
Висновки
Результати дослідження OMRIA RWE демонструють значні клінічні переваги OM-85 у разі додавання до СТ у пацієнтів з алергічною астмою середнього-тяжкого ступенів, зокрема меншу кількість і легший перебіг РІ; менше загострень астми, незапланованих візитів до лікаря; зниження потреби в курсах антибіотиків або пероральних КС. Додаткове призначення OM-85 доповнювало ефекти вакцинації, оптимізуючи ефективність профілактики. Для вивчення потенційних клінічних переваг OM-85 за неалергічних фенотипів астми потрібні подальші дослідження.
На вітчизняному ринку бактеріальний лізат OM-85 представлений препаратом Бронхо-Ваксом® (виробник – «ОМ Фарма СА» (Швейцарія), офіційний дистриб’ютор – ТОВ «Такеда Україна», маркетинговий партнер – компанія Delta Medical). Препарат є у двох формах: Бронхо-Ваксом® дорослі – капсули по 7 мг OM-85 для пацієнтів віком ≥12 років і Бронхо-Ваксом® діти – капсули по 3,5 мг OM-85 для дітей віком 6-12 років. Режим дозування: 1 капсула щоденно натще протягом 10 днів поспіль щомісяця курсом 3 місяці; за потреби – повторний курс через 6 місяців або індивідуальна корекція. Показаннями до застосування препарату є профілактика рецидивних інфекцій дихальних шляхів (фарингіт, бронхіт, синусит); допоміжна терапія при хронічному бронхіті, тонзиліті, синуситі; зниження ризику загострень при астмі, особливо фенотипі T2-high.
Література
Christopoulou M.E., Panteli L.S., Moisidis J.A., et al. Oral bacterial lysate OM-85 prevents respiratory tract infections in asthma: the OMRIA RWE study. J. Asthma Allergy. 2025 Jun 2; 18: 891-902. doi: 10.2147/JAA.S517194.