Використання антигістамінних препаратів за дерматологічної патології
Автор: Сергій Вікторович ЗАЙКОВ, доктор медичних наук, професор кафедри фтизіатрії і пульмонології Національного університету охорони здоров’я України ім. П.Л. Шупика (м. Київ), президент ВГО «Асоціація алергологів України»
Для лікування станів, асоційованих зі свербежем, лікарі-дерматологи зазвичай застосовують топічні засоби, а як ліки другої лінії додають антигістамінні препарати (АГП). Саме вони є однією з найчастіше призначуваних у дерматологічній практиці груп фармакопрепаратів, що пов’язано з численними та різноманітними ефектами гістаміну [1].
Гістамін є гетероциклічним аміном, що утворюється в ході декарбоксилювання L-гістидину – синтезується в тучних клітинах і базофілах. Гістаміну притаманні прозапальна та протизапальна дії водночас, і ці ефекти залежать як від підтипу рецепторів, так і від клітин, які стимулюються. Існує чотири підтипи рецепторів: H1, H2, H3 та H4. Рецептори типу H1 відповідають за імунорегуляторний ефект гістаміну, а також за гостре та хронічне алергічне запалення. При зв’язуванні гістаміну з Н1-рецепторами на венозних капілярах утворюються пухирі або ділянки ангіонабряку. Це відбувається в результаті вазодилатації та підвищеної проникності судин, що призводить до випотівання плазми разом з високомолекулярними білками, зокрема імуноглобулінами, в інтерстицій. Гістамін також індукує стимуляцію чутливих нервів, спричиняючи свербіж, і зумовлює формування змішаного клітинного інфільтрату пухирів. При цьому антигістамінними називають лише ті препарати, які взаємодіють з Н1-рецепторами. АГП є зворотними агоністами конституційно активних Н1-рецепторів, тобто вони протидіють ефектам гістаміну, стабілізуючи ці рецептори в неактивній конформації. Саме тому їх називають H1-АГП, а не антагоністами гістаміну.
АГП зумовлюють зворотний розвиток локальної вазодилатації та зменшують індуковану гістаміном підвищену проникність судин, таким чином зменшуючи місцевий набряк. Окрім блокування впливу гістаміну на рецептори малих кровоносних судин і чутливих нейронів, АГП опосередковано протидіють алергічному запаленню, пригнічуючи накопичення запальних клітин у тканинах організму та гальмуючи імунну відповідь на антигени [2].
Кропив’янка
Кропив’янка являє собою поширене запальне захворювання шкіри, яке характеризується активацією та вивільненням гістаміну й інших медіаторів з тучних клітин шкіри, що призводить до появи минущого висипу у вигляді пухирів та/або ангіонабряку.
Кропив’янка може виникати спонтанно або під впливом різних чинників і поділяється на гостру (триває до 6 тижнів) і хронічну (триває понад 6 тижнів). Хронічна кропив’янка, яка значно погіршує якість життя, частіше трапляється в дорослих жінок [3].
У разі хронічної спонтанної кропив’янки міжнародні рекомендації (EAACI/GA²LEN/EuroGuiDerm/APAAACI, 2022) радять виключити альтернативні діагнози, вивчити причини процесу за допомогою аналізу маркерів автоімунної кропив’янки, з’ясувати потенційні тригери (наприклад, стрес, приймання нестероїдних протизапальних препаратів), виявити коморбідні стани та наслідки кропив’янки (тривожність, депресія, втомлюваність, сексуальна чи когнітивна дисфункція, розлади сну), оцінити біомаркери хвороби та предиктори відповіді на лікування. Активність хвороби та її контроль доцільно моніторувати за допомогою шкали активності кропив’янки (Urticaria Activity Score, UAS), шкали активності ангіонабряку (Angioedema Activity Score, AAS), тесту контролю кропив’янки (Urticaria Control Test, UCT) і тесту контролю ангіонабряку (Angioedema Control Test, AECT), паралельно визначаючи якість життя за допомогою спеціальних опитувальників [2, 4].
Першою лінією лікування пацієнта з кропив’янкою виступають АГП другого покоління, а альтернативою – омалізумаб і циклоспорин А. Останніми роками було запропоновано інноваційні режими лікування, як-от підвищення дози АГП учетверо порівняно зі стандартом [3, 5]. Така високодозова терапія забезпечує успіх лікування в 63% осіб, які не відповіли на стандартні дози АГП [6]. Ефективність їх зазвичай є індивідуальною, тому в разі невдачі однієї активної речовини доцільно спробувати призначити іншу. Слід зауважити, що АГП є дієвішими за щоденного приймання, а не при застосуванні на вимогу. Якщо стандартна доза АГП дає змогу контролювати симптоми, доцільно продовжити лікування протягом кількох тижнів – кількох місяців, періодично перериваючи його, щоб з’ясувати, чи не припинилася кропив’янка спонтанно. Якщо застосування стандартних доз протягом 2-4 тижнів не забезпечило контролю симптомів, доцільно підвищити дозу АГП [7].
Загалом АГП є наріжним каменем лікування осіб із хронічною кропив’янкою. Оскільки існує велика кількість різних АГП, обирати препарат слід на підставі індивідуальних характеристик і вподобань пацієнта, зважаючи на вік, стать і потенційні міжлікарські взаємодії [2].
Атопічний дерматит
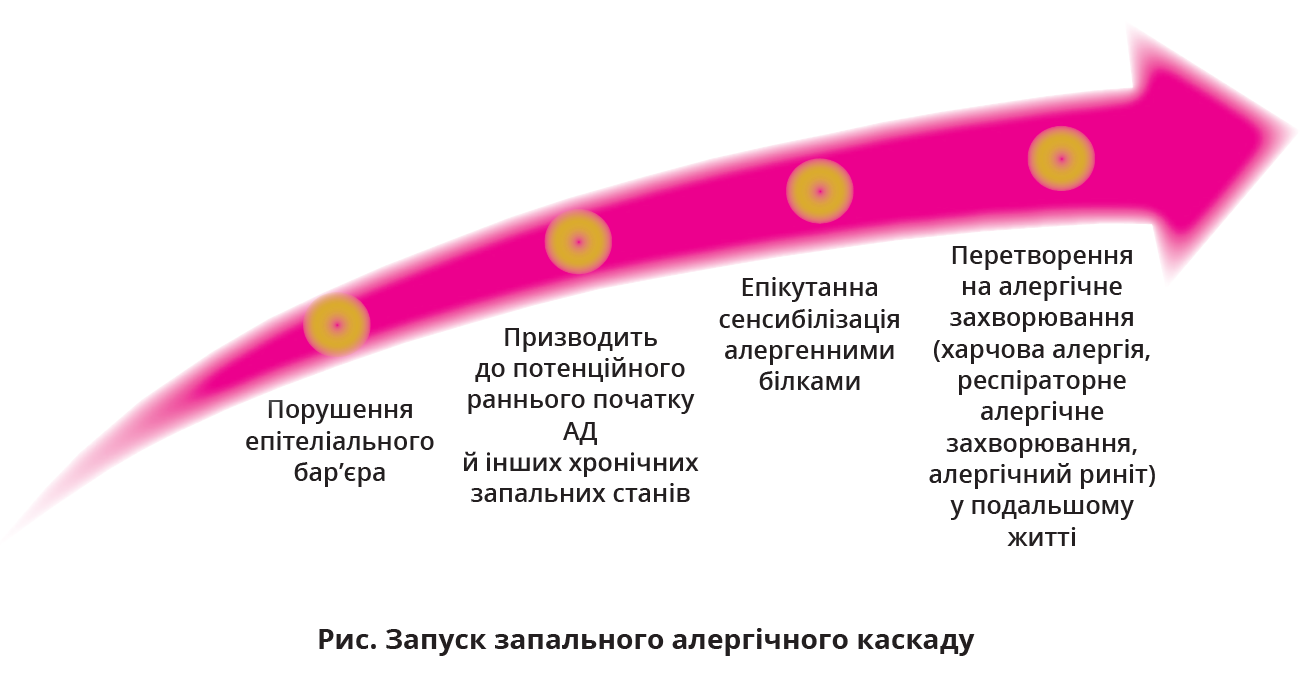
Поширеність атопічних хвороб стабільно зростає, що зумовлює потребу в глибокому їх вивченні з метою формування оптимальних діагностично-лікувальних алгоритмів. Нерідко першим проявом атопічних захворювань виступає саме атопічний дерматит (АД), з яким часто асоційовані харчова алергія, алергічний риніт або алергічна астма, що підтверджує їхній спільний патогенетичний механізм. Цей процес має назву атопічного маршу. Вважається, що першим кроком у запуску запального алергічного каскаду є ушкодження епітеліального бар’єра (рис.) [8].
АД, або атопічна екзема, характеризується почервонінням і свербежем шкіри, її сухістю, іхтіозом і навіть больовими відчуттями. АД притаманні також несприятливі психосоціальні впливи: стигматизація, порушення особистих стосунків, розлади сну, тривожність, гіперактивність, депресія. Хоча патогенез АД дотепер вивчений недосконало, в його основі лежать порушення епідермального бар’єра й імунна дисрегуляція [9].
Зазвичай АД має типовий хронічний перебіг, який характеризується чергуванням ремісій і загострень, причому під час останніх пацієнти можуть потребувати більших доз фармакопрепаратів. Існує два підходи до довготривалого лікування АД: реактивний і проактивний. Реактивний підхід передбачає щоденне зволожування та наводнення шкіри в поєднанні з протизапальним засобом (за потреби), натомість проактивний – періодичне нанесення протизапальних і пом’якшувальних засобів на уражені, а іноді навіть на неуражені ділянки. У разі помірно тяжкого або тяжкого АД зі значно погіршеною якістю життя рекомендовано застосовувати проактивний підхід [9].
Для лікування АД призначаються різнопланові топічні засоби: зволожувальні та пом’якшувальні креми, глюкокортикоїди (ГК), інгібітори кальциневрину – ІКН (такролімус, пімекролімус). Проактивна топічна протизапальна терапія зазвичай передбачає тривале застосування комбінації ГК та/або ІКН з пом’якшувальними засобами. На початку лікування ГК/ІКН застосовуються щодня до досягнення контролю, а потім частота використання поступово знижується до 2-3 разів на тиждень протягом 16 тижнів [8]. ГК гальмують взаємодію дендритних клітин і клітин Ланґерганса з антигенами та зменшують вироблення прозапальних цитокінів. Найчастіше призначуваними ГК виступають гідрокортизон, тріамцинолон і бетаметазон, представлені у формі кремів, мазей і лосьйонів. Для нанесення на обличчя та шию доцільно застосовувати менш потужні ГК, наприклад гідрокортизон (1%), натомість для інших ділянок тіла призначають потужніші варіанти цих препаратів (клобетазол). ГК слід наносити тонким шаром, після чого змазувати шкіру зволожувальним засобом. Поступове скасування ГК у міру зниження інтенсивності симптомів покликане мінімізувати такі їхні потенційні побічні ефекти, як стрії, атрофія та витоншення шкіри [9].
Хоча асоційований з АД свербіж має переважно «негістамінний» характер, АГП першого та другого поколінь можуть призначатися пацієнтам, які мають розлади сну або сильно розчухують шкіру під час сну [9]. АГП першого покоління мають додаткові седативні характеристики; хоча вони безпосередньо не усувають свербіж, ця седативна дія дає змогу покращувати сон у пацієнтів з АД. Натомість неседативні АГП другого покоління успішно застосовуються в осіб з алергічними тригерами АД, наприклад з IgE-залежною його формою, поєднанням АД з кропив’янкою, алергічним ринокон’юнктивітом, харчовою, медикаментозною, інсектною алергією тощо й не мають несприятливих побічних ефектів у формі надмірної седації, погіршення навчання та працездатності [10].
Алергічний контактний дерматит
Контактний дерматит, зумовлений побутовими хімічними речовинами чи професійним контактом, є поширеною причиною звернень до лікаря.
З огляду на патофізіологічне підґрунтя виокремлюють два типи контактного дерматиту: пов’язаний з подразненням шкіри (простий або іритативний) і пов’язаний з алергопатологією (власне алергічний контактний дерматит – АКД). На частку АКД припадає 20% випадків контактного дерматиту, що зумовлює актуальність цього захворювання. Цей вид дерматиту проявляється сверблячим висипом, що виникає через кілька днів – кілька годин після контакту з алергеном. У хронічній фазі хвороби спостерігаються еритема, лущення та ліхеніфікація шкіри.
Домінувальним симптомом при АКД виступає сильний свербіж, який значно погіршує якість життя пацієнтів. Слід зауважити, що цей свербіж може мати гістамінергічний і негістамінергічний характер. Гістамінергічний свербіж опосередковують тучні клітини, вивільняючи гістамін, який, своєю чергою, активує рецептори на чутливих нейронах задніх корінців спинного мозку.
Основним методом лікування пацієнтів з АКД є уникнення контакту з алергеном, але в реальному житті це досить складно здійснити, оскільки алергени присутні в усіх можливих середовищах, а для розвитку реакції з боку шкіри достатньо надзвичайно малої кількості причинного алергену, який далеко не завжди можливо ідентифікувати [11]. Першою лінією фармакотерапії пацієнтів виступають топічні ГК (якщо уражено <20% поверхні тіла) чи системні пероральні ГК (якщо уражено >20% поверхні тіла). Якщо АКД розвинувся в таких делікатних ділянках, як складки шкіри або повіки, можуть застосовуватися топічні ІКН або інгібітори фосфодіестерази-4. Симптоматичне лікування передбачає пероральні АГП, прохолодні ванночки та зволожувальні засоби. У деяких випадках доцільною може бути фототерапія ультрафіолетовими променями типу А в поєднанні з псораленом, а в разі найтяжчого перебігу – імуносупресивні засоби на кшталт мікофенолату мофетилу [12].
При тяжкому АКД, який супроводжується значним свербежем, можуть застосовуватися пероральні АГП [13], причому нерідко – АГП першого покоління з певною седативною/снодійною дією [14]. Важливо, що АГП у цьому випадку є не лише ефективними, а й безпечними препаратами [15].
Отже, АГП відіграють значну роль у лікуванні пацієнтів з дерматологічною патологією. В одних ситуаціях (у разі кропив’янки) вони є препаратами першої лінії, в інших (при АД або АКД) – допоміжними, але також важливими лікарськими засобами, які дають змогу підвищити ефективність лікування та якість життя відповідної категорії пацієнтів. Обираючи оптимальний АГП, слід оцінити потребу пацієнта в додатковій седативній/снодійній дії засобу. Якщо в клінічній картині дерматологічної хвороби домінує свербіж, який є настільки вираженим, що значно турбує пацієнта й перешкоджає сну, доцільним є застосування АГП першого покоління. Якщо ж провідну роль відіграє уртикарний висип або ураження шкіри поєднується з алергічним ринітом чи кон’юнктивітом, перевагу варто віддати АГП другого покоління, котрі не спричиняють седації та не мають снодійної дії.
Список літератури – в редакції.
