Клінічно значущі характеристики препарату Ріалтріс і порівняння з іншими протиалергічними назальними спреями
Переклала й адаптувала канд. біол. наук Олександра Демецька
Останніми роками було розроблено та комерціалізовано низку назальних препаратів, призначених для лікування алергічних захворювань [1, 2]. Поєднання інноваційних методів тестування з традиційними підходами для дослідження протиалергічних назальних спреїв дає змогу отримати глибше розуміння таких важливих аспектів, як розчинення й осадження, та зрештою передбачити їхню ефективність in vivo.
Характеристики протиалергічних назальних продуктів, що впливають на ефективність
Носові симптоми серйозно впливають на якість життя пацієнтів: лише в США алергічний риніт є відповідальним за приблизно 800 000 днів відпустки та 825 000 днів поза навчанням, а також за зниження продуктивності, оцінене в 4 250 000 днів на рік [3].
Назальні засоби, схвалені для місцевого лікування сезонного або цілорічного алергічного риніту, переважно представлені у вигляді суспензій, що містять кортикостероїди або розчини антигістамінних препаратів (у деяких випадках пропонується поєднання двох терапевтичних класів) [4]. Установлено, що ефективність цих назальних продуктів ґрунтується на розчинності препарату, стабільності, відкладенні в носовій порожнині, часі перебування (обмеженому елімінацією препарату внаслідок мукоциліарного кліренсу) й ефекті допоміжних речовин, які разом у підсумку впливають на місцеве всмоктування та визначають поведінку препаратів in vivo [7-9].
Натепер існує ціла низка методів для визначення характеристик інгаляційних продуктів, які зазвичай застосовують окремо. Тому певний інтерес становило застосування сучасних методик, зосереджених на розчиненні, осадженні й адгезії, для характеристики технологічних аспектів, які визначають клінічну ефективність назального спрею Ріалтріс (мометазону фуроат і олопатадину гідрохлорид) порівняно з іншими комерційними назальними препаратами, що показані при алергічному риніті, а саме комбінації азеластину гідрохлориду та флутиказону пропіонату (Диміста), мометазону фуроату (Назонекс) і флутиказону фуроату (Аваміс).
Аспекти, пов’язані з рецептурою
Тест ANOVA показав, що показники в’язкості препаратів мали статистично значущі відмінності (p=0,0001). Зокрема, Ріалтріс продемонстрував найвищу в’язкість порівняно з іншими продуктами (рис. 1).

Як додатковий тест на в’язкість було виконано простий експеримент для оцінювання потоку складу на похилій площині. Це дало додаткову інформацію про тенденцію назального продукту витікати після введення. Схеми потоку, створені для досліджуваних продуктів, представлено на рисунку 2.

Цікаво, що результати лише частково визначалися в’язкістю рецептури. Показано, що Диміста забезпечує найшвидший потік, оскільки він не дуже в’язкий. Водночас Ріалтріс, найбільш в’язка суспензія, не продемонстрував помітної течії та залишився прикріпленим до похилої площини напівтвердого покриття. Аваміс продемонстрував проміжну поведінку з помірним потоком, тоді як Назонекс, усупереч очікуванням, забезпечив структуру потоку, подібну до такої Диміста.
Аспекти, пов’язані з пристроєм
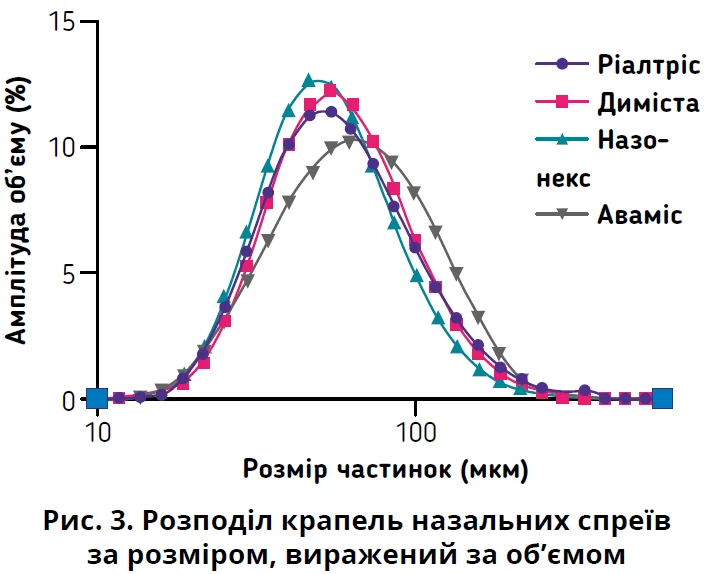
Усі комерційні продукти були піддані аналізу розміру крапель спрею (рис. 3). Було виявлено, що розподіл крапель за розміром має середній пік близько 50-60 мкм, причому Аваміс представлений найбільшими краплями. Назонекс мав вужчий розподіл крапель за розміром, тоді як Аваміс і Ріалтріс продемонстрували ширший розподіл розпилення, але ці відмінності не були статистично значущими.
Відкладення зліпка
Аналіз відкладення зліпка в носі проводили для всіх чотирьох композицій. Схеми відкладення Ріалтріс, Диміста, Назонекс і Аваміс були досліджені при введенні продукту в силіконовій назальній пов’язці, покритій пастою для виявлення води. Пристрій вставляли в ніздрю під кутом 45° від горизонталі до «нормального» поводження пацієнта з пристроєм.
Загальне відкладення для Аваміс становило 27,42±1,72%, для Диміста – 28,96±2,86%, для Назонекс – 27,74±1,59%, для Ріалтріс – 28,69±2,41% (p=0,28). Цікаво, що аналіз регіональних відкладень показав деякі незначні, але статистично значущі відмінності; це означає для Ріалтріс менші відкладення в передній частині носа та більші – в середній і верхній ділянках раковини.
Назальний спрей Ріалтріс також було проаналізовано, щоб дослідити потенційні відмінності в картині осадження та регіональному осадженні в носовій порожнині при зміні нахилу виробу під час активації з 45° до 30° або 60° від горизонтальної площини, тобто імітуючи неправильне використання пристрою.
Аналіз відкладень продемонстрував, що активація під кутом 60° призвела до значно більшого відкладення в присінку носа (p=0,0049) та значно меншого відкладення в середній і верхній ділянках носової раковини (p=0,0190). Незважаючи на це, не було суттєвої різниці в загальній площі, охопленій випробуваннями під кутом 45° і 30° (p<0,0001).
Аспекти, пов’язані з активним інгредієнтом
Дослідження розчинення назальних продуктів проводили з використанням Respicell – апарату, призначеного для розчинення продуктів інгаляції, який дає змогу змочувати продукт, а отже, процес розчинення відбувається на вологій поверхні полімерної мембрани.
Профілі розчинення для кортикостероїду показали дещо швидше розчинення для флютиказону фуроату (Аваміс), за яким слідував мометазону фуроат (Ріалтріс і Назонекс), тоді як флютиказону пропіонат (Диміста) продемонстрував повільніше розчинення: менш ніж 30% дози розчинялося протягом 240 хвилин (рис. 4).

Профілі розчинення порівнювали з використанням факторів відмінності (f1) і подібності (f2) – статистичного підходу, який добре зарекомендував себе для порівняння профілів розчинення пероральних продуктів. Аваміс, Назонекс і Ріалтріс мали подібні профілі розчинення, оскільки значення f1 були нижчими за 15, а значення f2 – вищими за 50. Навпаки, повільніший профіль розчинення свідчив, що Диміста відрізняється (f1 >15, f2 >50) від трьох інших досліджуваних продуктів.
Розподіл зважених частинок за розміром і морфологічний аналіз
Назальні продукти, що містять кортикостероїди, є суспензіями; крім того, всі продукти містили целюлозу, яка також присутня у вигляді диспергованих нерозчинних частинок. На рисунку 5 представлено розподіл зважених частинок за кількістю.

Ріалтріс і Аваміс були представлені найбільшою кількістю субмікронних частинок, за ними слідував Назонекс, тоді як Диміста був продуктом з найменшою присутністю високодисперсних частинок.
Обговорення
Серед різних фізико-хімічних характеристик рідких назальних композицій в’язкість незмінно вказується як один з тих параметрів, що є ключовими для ефективності назальних продуктів, і впливає на розмір частинок крапель, кути розпилення й осадження, а також час перебування продукту після осадження [2, 21]. Протестовані назальні продукти мають різний склад композиції та, як наслідок, демонструють суттєво різну в’язкість. Якщо взяти за еталон класичний назальний спрей Назонекс, помітно, що в’язкість комбінованого препарату Диміста становить лише малу частку його в’язкості, тоді як в’язкість Ріалтріс у 4-5 разів вища, а отже, в десятки разів перевищує в’язкість інших комбінованих препаратів.
Висока подібність у розподілі розміру крапель забезпечила майже однакове осадження в назальному зліпку для чотирьох назальних продуктів, з невеликою, але значною різницею в регіонах осадження, засвідченою лише для Ріалтріс, що сприяло глибшому проникненню спрею до середньої та верхньої ділянок носової раковини.
В’язкість мала значний вплив на течію на похилій площині з результатами, які чітко відрізняли назальні продукти (Ріалтріс < Аваміс < Диміста ~ Назонекс). Це має велике клінічне значення, оскільки, як показано на рисунку 2, новий комбінований спрей Ріалтріс залишається на місці осадження й не тече через вищу в’язкість. Останнє забезпечує інтенсивний обмін зі слизовою оболонкою носа.
Результати показали, що флутиказону пропіонат у складі Диміста розчинявся повільніше порівняно з іншими кортикостероїдами, тобто мометазону пропіонатом у складі Ріалтріс і Назонекс і флутиказону фуроатом у складі Аваміс. Частково це можна пояснити деякими відмінностями в розподілі суспендованих частинок за розміром, які показали для Диміста найнижчу кількість частинок менш ніж 1 мкм, тоді як ця кількість була найвищою для Аваміс і Ріалтріс, які продемонстрували найвищі швидкості розчинення.
Водночас фізико-хімічні властивості активного інгредієнта також відіграють вирішальну роль у кінетиці розчинення, оскільки два препарати, що містять мометазону фуроат, тобто Ріалтріс і Назонекс, продемонстрували найбільш подібні профілі розчинення.
Було повідомлено, що полегшення симптомів настає приблизно через 7 годин після прийому мометазону фуроату [27] і через 8 годин після прийому флютиказону фуроату [28, 29] у пацієнтів з алергічним ринітом.
Висновки
Назальний спрей Ріалтріс, який являє собою комбінацію фіксованих доз мометазону фуроату й олопатадину гідрохлориду, продемонстрував особливі властивості порівняно з іншими проаналізованими комерційними продуктами (Аваміс, Назонекс, Диміста).
Ріалтріс має вищу в’язкість, що сприяє тривалішому часу утримування в носовій порожнині, не впливаючи на носові відкладення. Було продемонстровано, що назальне відкладення Ріалтріс глибоко та рівномірно розподіляється на носових раковинах, особливо під кутом 30° уведення пристрою.
Профілі розчинення показали, що мометазону фуроат, який міститься в комбінованому спреї Ріалтріс, розчинявся вдвічі швидше, ніж флутиказону пропіонат у спреї Диміста, й подібно до інших препаратів порівняння, тобто мометазону фуроату та флутиказону фуроату (Назонекс і Аваміс відповідно). Це може мати позитивні клінічні наслідки, зокрема швидший початок дії та підвищення ефективності нового комбінованого спрею Ріалтріс, зважаючи також на вищу в’язкість препарату.
Зазначені аспекти є актуальними не лише для характеристики та диференціації назальних продуктів, які вже представлені на ринку, але й для розроблення нових назальних препаратів і кращого розуміння їхньої потенційної клінічної ефективності.
Література
Patterlini V., Guareschi F., D’Angelo D., et al. Clinically relevant characterization and comparison of Ryaltris and other anti-allergic nasal sprays. Pharmaceutics. 2024; 16 (8): 989. doi: 10.3390/pharmaceutics16080989.
