Антигістамінні препарати в педіатричній практиці: пошук балансу ефективності й безпеки
Автор: Світлана Миколаївна НЕДЕЛЬСЬКА, докторка медичних наук, професорка, завідувачка кафедри факультетської педіатрії Запорізького державного медичного університету, керівниця Центру сучасної дитячої алергології та пульмонології, віцепрезидентка ВГО «Асоціація алергологів України»
Огляд присвячено аналізу доступних в Україні дитячих форм антигістамінних препаратів (АГП) з акцентом на їхню безпеку. Пероральні АГП I покоління досі використовуються в педіатричній практиці, але вони спричиняють низку серйозних побічних явищ. Тому дедалі значнішого поширення набувають АГП II покоління, котрі позбавлені більшості негативних ефектів попереднього покоління. Найкращий профіль безпеки мають активні метаболіти II покоління, як-от дезлоратадин. Результати власних спостережень підтверджують цей висновок.
Нині майже половина педіатричного населення має принаймні один симптом алергії (de Las Vecillas, 2024). У лікуванні алергічних захворювань (АЗ) широко використовуються АГП (Wang, 2024). Однак існує небагато клінічних настанов, орієнтованих саме на педіатричну популяцію, переважно через недостатню кількість високоякісних досліджень для підтримки терапевтичних варіантів у дітей (Chin, 2023). Діти значною мірою були виключені з рандомізованих випробувань ліків від симптомів АЗ (Cohen, 2023) у зв’язку із жорсткішими вимогами в питаннях безпеки таких випробувань для дітей. Тому сьогодні лікування педіатричних АЗ зазвичай екстраполюється з досліджень за участю дорослих (Chin, 2023), лише з корегуваннями доз АГП залежно від віку (Cohen, 2023). Проте такий підхід при виборі АГП для застосування саме в дітей потребує прискіпливішої уваги до можливих побічних ефектів.
Мета огляду – аналіз доступних в Україні дитячих форм пероральних АГП з акцентом на їхню безпеку.
Матеріали та методи
Вивчено інструкції для медичного застосування найпоширеніших в Україні АГП, а також доступні в наукометричних базах дані щодо профілю безпеки для дітей таких молекул, як дезлоратадин, левоцетиризин, хлоропірамін, диметинден, мебгідролін. Відомо, що ризик побічних явищ АГП найчастіше пов’язаний із недостатньою селективністю до Н1-рецепторів і непотрібною здатністю проникати крізь гематоенцефалічний бар’єр, що спричиняє, в тому числі, сонливість/седацію. Враховуючи важливість уникнення такого несприятливого ефекту для нормального когнітивного, фізичного та психологічного розвитку дитини, саме показник частоти виникнення сонливості вибраний як основний для оцінки профілю безпеки тієї чи іншої молекули АГП. З огляду також на те, що високий профіль безпеки зазвичай підтверджується використанням без особливих застережень у немовлят і дітей, брали до уваги й цей показник.
Результати й обговорення
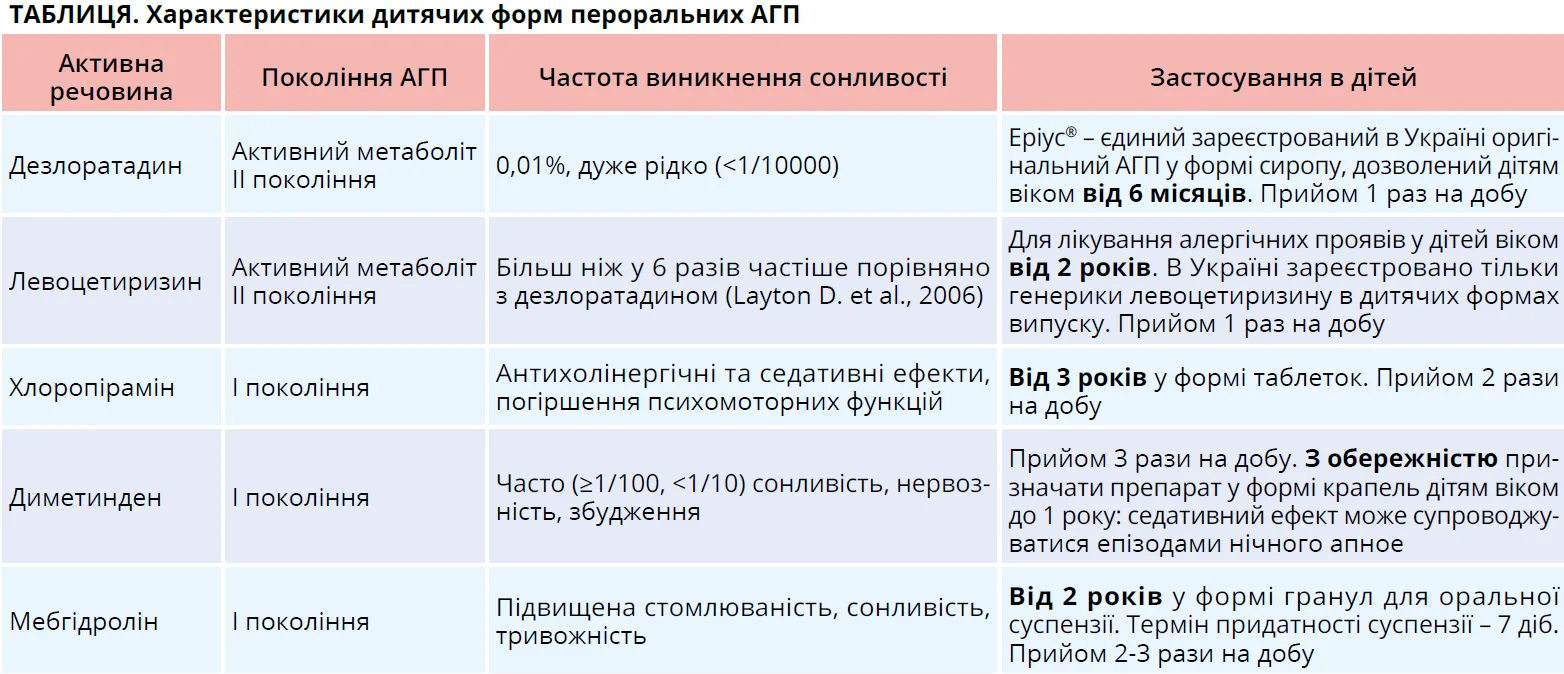
Дані для порівняння найпоширеніших дитячих форм АГП за вибраними критеріями представлено в таблиці.
Як бачимо з таблиці, АГП хлоропірамін може застосовуватися дітям тільки з 3-річного віку, часто спричиняє погіршення психомоторних функцій. Активна речовина диметинден також часто зумовлює побічні реакції, дітям до року може застосовуватися тільки із застереженням, оскільки провокує таке небезпечне явище, як епізоди нічного апное. Активна речовина мебгідролін теж проявляє нейротоксичність, тому дітям може призначатися тільки з віку 2 років, незважаючи навіть на такий тривалий час на ринку, за який могли би з’явитися докази безпечності його застосування для дітей більш раннього віку, якби це справді було так.
Варто зазначити, що хлоропірамін, диметинден, мебгідролін є представниками АГП І покоління.
Для них із часом з’являється, навпаки, чимраз більше доказів негативного профілю безпеки (Linton, 2023). Так само, як і для інших АГП І покоління (дифенгідрамін, гідроксизин тощо), котрі проникають крізь гематоенцефалічний бар’єр і спричиняють седативний ефект, знижуючи розвиток когнітивних функцій, продуктивність у школі та якість життя в пацієнтів з алергією (Cohen, 2023). Масштабне педіатричне популяційне перехресне дослідження показало, що застосування АГП І покоління пов’язане з підвищеним ризиком і серцево-судинних подій, особливо аритмій, у дітей раннього віку (Kim, 2023). Тому сьогодні такі препарати визнані застарілими та більше не рекомендуються міжнародними настановами для лікування як алергічного риніту, так і кропив’янки, причому не тільки в дітей, а й навіть у дорослих пацієнтів (Linton, 2023).
Натомість накопичується дедалі більше доказів на підтримку нового покоління АГП (Linton, 2023; Vandenberghe-Dürr, 2024; Wang, 2024), так званих неседативних. Вони настійно рекомендуються для лікування в дітей алергічного риніту (Cohen, 2023; Sato, 2023; Weaver-Agostoni, 2023; Bernstein, 2024; Tosca, 2024), кон’юнктивіту (Mahoney, 2023), кропив’янки (Chin, 2023; Podder, 2023; Yosipovitch, 2023; Wieczorek, 2024). Друге покоління АГП і з’явилося саме в результаті пошуку препаратів, котрі були б максимально позбавлені тих негативних побічних ефектів, що притаманні препаратам І покоління. Ба більше, на основі деяких АГП ІІ покоління винайдено ще безпечніші препарати, котрі мають іще нижчий ризик нейротоксичності, кардіотоксичності, гепатотоксичності завдяки тому, що вони не потребують для свого метаболізму участі цитохрому Р450.
Це – активні метаболіти ІІ покоління АГП, які називають інколи навіть ІІІ поколінням (Czech, 2023).
Із наведених у таблиці препаратів до цієї групи належать перші два. Якщо ж порівняти їх між собою, то побачимо, що дезлоратадин (активна речовина Еріус® сироп) має вищий профіль безпеки, ніж левоцетиризин, адже частота виникнення сонливості при застосуванні левоцетиризину в 6 разів більша, ніж у разі застосування дезлоратадину (Layton, 2006). Саме з міркувань безпеки препарати з активною речовиною левоцетиризин рекомендуються дітям тільки після 2 років, тоді як Еріус® сироп – із 6 місяців у разі кропив’янки та з 1 року при алергічному риніті.
До того ж в Україні зареєстровано тільки генеричні форми левоцетиризину для застосування в дітей (Довідник еквівалентності лікарських засобів).
А Еріус® сироп – оригінальний дезлоратадин, який виробляється в Європейському Союзі, а отже, він пройшов усі необхідні доклінічні та клінічні дослідження в повному обсязі – щодо як ефективності, так і безпеки, в тому числі на педіатричній популяції (Bloom, 2004; Prenner, 2006; Gupta, 2007). Дослідження дезлоратадину тривають і сьогодні (Kapadia, 2024; Zwierz, 2024), підтверджуючи його високу ефективність і сприятливий профіль безпеки. Варто зазначити, що Еріус® – єдиний зареєстрований в Україні оригінальний АГП у формі сиропу, дозволений дітям віком від 6 місяців (Державний реєстр лікарських засобів України). Тому можна говорити про найкращий баланс ефективності й безпеки цього препарату серед інших АГП.
Саме тому для лікування АЗ, з якими зверталися найменші пацієнти до Центру сучасної дитячої алергології та пульмонології протягом останніх років, було вибрано Еріус® сироп. Дозування препарату здійснювали згідно з його інструкцією: дітям віком від 6 до 11 місяців – по 2 мл сиропу (1 мг дезлоратадину), від 1 до 5 років – по 2,5 мл сиропу (1,25 мг дезлоратадину), від 6 до 11 років – по 5 мл сиропу (2,5 мг дезлоратадину), віком від 12 років – по 10 мл сиропу (5 мг дезлоратадину) 1 раз на добу.
У нашій клініці Еріус® сироп регулярно використовується для лікування алергічного риносинуситу (ринокон’юнктивіту), гострої та хронічної кропив’янки, шкірних проявів харчової, медикаментозної алергії. Цей препарат дав нам змогу отримати клінічно значущий результат і в тих випадках, коли в дитини респіраторні симптоми поєднувалися зі шкірними: алергічний риніт і кропив’янка, бронхіальна астма й екзема тощо. При тяжкому перебігу атопічного дерматиту ми застосовуємо тривалий прийом Еріус®, адже завдяки протизапальній, протинабряковій діям він дає змогу досягнути ефективного контролю над станом дитини, зменшити активність запалення, ліхеніфікацію, свербіж і поступово розширити дієтичні обмеження. У всіх випадках був досягнутий очікуваний клінічний ефект, діти переносили лікування добре.
Висновок
Отже, дані проведеного огляду та власний клінічний досвід свідчать на користь вибору серед АГП для застосування в дітей активних метаболітів
ІІ покоління, як-от дезлоратадин (Еріус® сироп). Сприятливий профіль безпеки, доведена ефективність, наявність дитячої лікарської форми випуску (сироп), можливість застосування всього 1 раз на добу та призначення вже з 6-місячного віку, а також незаперечна якість оригінального дезлоратадину Еріус® виступають найважливішими аргументами на користь саме цього АГП для використання в педіатричній практиці.
Література
- Bernstein J.A., Bernstein J.S., Makol R., Ward S. Allergic rhinitis: a review. JAMA. 2024; 331 (10): 866-877. doi: 10.1001/jama.2024.0530.
- Bloom M., Staudinger H., Herron J. Safety of desloratadine syrup in children. Curr. Med. Res. Opin. 2004; 20 (12): 1959-1965. doi: 10.1185/030079904×14148.
- Chin M.L. It comes and goes: pediatric chronic spontaneous urticaria. Cureus. 2023; 15 (6): e40006. Published 2023 Jun 5. doi: 10.7759/cureus.40006.
- Cohen B. Allergic rhinitis. Pediatr. Rev. 2023; 44 (10): 537-550. doi: 10.1542/pir.2022-005618.
- Czech E.J., Overholser A., Schultz P. Allergic rhinitis. Prim. Care. 2023; 50 (2): 159-178. doi: 10.1016/j.pop.2023.01.003.
- de Las Vecillas L., Quirce S. The multiple trajectories of the allergic march. J. Investig. Allergol. Clin. Immunol. 2024; 34 (2): 75-84. doi: 10.18176/jiaci.0983.
- Gupta S.K., Kantesaria B., Banfield C., Wang Z. Desloratadine dose selection in children aged 6 months to 2 years: comparison of population pharmacokinetics between children and adults. Br. J. Clin. Pharmacol. 2007; 64 (2): 174-184. doi: 10.1111/j.1365-2125.2007.02859.x.
- Kapadia S., Nageswaramma S., Shah K., et al. The efficacy and safety of high dose (10 mg) of desloratadine (Dazit® 10) in the treatment of chronic spontaneous urticaria in India: a phase III, multicentric, open-label, single-arm study. Cureus. 2024; 16 (1): e53125. Published 2024 Jan 28. doi: 10.7759/cureus.53125.
- Kim J.H., Cha H.R., Ha E.K., et al. Association between first-generation antihistamine use in children and cardiac arrhythmia and ischemic heart disease:
a case-crossover study. Pharmaceuticals (Basel). 2023; 16 (8): 1073. Published 2023 Jul 28. doi: 10.3390/ph16081073. - Layton D., Wilton L., Boshier A., Cornelius V., Harris S., Shakir S.A. Comparison of the risk of drowsiness and sedation between levocetirizine and desloratadine: a prescription-event monitoring study in England. Drug Saf. 2006; 29 (10): 897-909. doi: 10.2165/00002018-200629100-00007.
- Linton S., Hossenbaccus L., Ellis A.K. Evidence-based use of antihistamines for treatment of allergic conditions. Ann. Allergy Asthma Immunol. 2023; 131 (4): 412-420. doi: 10.1016/j.anai.2023.07.019.
- Mahoney M.J., Bekibele R., Notermann S.L., Reuter T.G., Borman-Shoap E.C. Pediatric conjunctivitis: a review of clinical manifestations, diagnosis, and management. Children (Basel). 2023; 10 (5): 808. Published 2023 Apr 29. doi: 10.3390/children10050808.
- Podder I., Dhabal A., Chakraborty S.S. Efficacy and safety of up-dosed second-generation antihistamines in uncontrolled chronic spontaneous urticaria: a review. J. Clin. Aesthet. Dermatol. 2023; 16 (3): 44-50.
- Prenner B., Ballona R., Bueso A., et al. Safety of desloratadine syrup in children six months to younger than 2 years of age: a randomized, double-blinded, placebo-controlled study. Pediatric Asthma Allergy & Immunology. 2006; 19 (2): 91-99. doi: 10.1089/pai.2006.19.91.
- Sato T., Tareishi Y., Suzuki T., Ansai N., Asaka C., Ohta N. Effect of second-generation antihistamines on nighttime sleep and daytime sleepiness in patients with allergic rhinitis. Sleep Breath. 2023; 27 (6): 2389-2395. doi: 10.1007/s11325-023-02857-6.
- Tosca M.A., Trincianti C., Naso M., Nosratian V., Ciprandi G. Treatment of allergic rhinitis in clinical practice. Curr. Pediatr. Rev. 2024; 20 (3): 271-277. doi: 10.2174/1573396320666230912103108.
- Vandenberghe-Dürr S., Harr T., Vandenberghe F. Antihistaminiques : une histoire sans fin [Antihistamines: an ongoing narrative]. Rev. Med. Suisse. 2024; 20 (868): 711-719. doi: 10.53738/REVMED.2024.20.868.711.
- Wang D., Guo Q., Wu Z., et al. Molecular mechanism of antihistamines recognition and regulation of the histamine H1 receptor. Nat. Commun. 2024; 15 (1): 84. Published 2024 Jan 2. doi: 10.1038/s41467-023-44477-4.
- Weaver-Agostoni J., Kosak Z., Bartlett S. Allergic rhinitis: rapid evidence review. Am. Fam. Physician. 2023; 107 (5): 466-473.
- Wieczorek D., Wedi B. Zugelassene Therapien und ihre Wirkung auf die Leitsymptome der Urtikaria : Hilfreiche Therapieoptionen, wenn juckende Quaddeln nicht weichen – Viel hilft viel? [Approved therapies and their effects on the main symptoms of urticaria: When symptom control of itchy wheals is not adequate – does updosing help?]. Dermatologie (Heidelb). 2024; 75 (4): 281-288. doi: 10.1007/s00105-024-05315-w.
- Yosipovitch G., Biazus Soares G., Mahmoud O. Current and emerging therapies for chronic spontaneous urticaria: a narrative review. Dermatol. Ther. (Heidelb). 2023; 13 (8): 1647-1660. doi: 10.1007/s13555-023-00972-6.
- Zwierz A., Domagalski K., Masna K., Burduk P. Maximal medical treatment of adenoid hypertrophy: a prospective study of preschool children. Eur. Arch. Otorhinolaryngol. Published online January 31, 2024. doi: 10.1007/s00405-024-08459-6.
- Державний реєстр лікарських засобів України [Електронний ресурс]. – Режим доступу: http://www.drlz.com.ua.
- Довідник еквівалентності лікарських засобів [Електронний ресурс]. – Режим доступу: https://rx.ua/inn–mnn/levocetirizin.