#WEAREUEG: сила єдності, що рухає гастроентерологію вперед
Автор: Ігор Миколайович СКРИПНИК, доктор медичних наук, професор, президент ГО «Українська гастроентерологічна асоціація», проректор із науково-педагогічної роботи та післядипломної освіти, професор кафедри внутрішньої медицини № 1 Полтавського державного медичного університету
Світова гастроентерологічна спільнота цьогоріч зібралася 4-7 жовтня в серці Європи, в Берліні (Німеччина) – місті, в якому неймовірно поєднуються минуле, сучасне та майбутнє. Приводом для зустрічі стала значна наукова подія – тиждень Об’єднаної європейської гастроентерології (UEG Week 2025). У залах конгрес-холу Messe Berlin усе нагадувало про спадкоємність і спільні цінності UEG. На екранах і стендах сяяв знайомий зелений логотип – стилізоване зображення шлунково-кишкового тракту, ніби символ живого руху знань і єдності всього організму. Проте головним акцентом цього року став новий девіз – #weareUEG («Ми є UEG»). Він лунав у кожному виступі, на кожній панелі, відлунював у розмовах між колегами – як нагадування, що наука має справжню силу лише тоді, коли вона об’єднує.
Традиційно роботу конференції відкрив президент UEG, професор Matthias Löhr. Він привітав учасників і підкреслив, що з кожним роком UEG Week стає дедалі масштабнішим та інклюзивнішим заходом. Саме цього року активність спільноти сягнула рекордних показників: до події долучилися 12 230 делегатів зі 115 країн світу, які прослухали 178 лекцій і взяли участь у 21 індустріальному симпозіумі. Крім того, 5289 осіб узяли участь у програмі післядипломного навчання, що підтверджує зростання інтересу до поглибленого навчання та професійного розвитку. «Це робить UEG Week 2025 дійсно світовою подією в гастроентерології», – підкреслив M. Löhr.
Комунікація та дезінформація
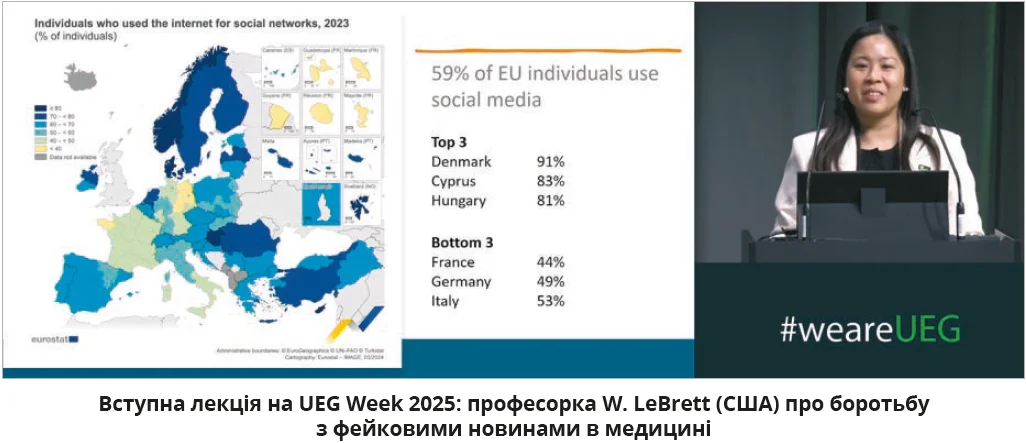
Особливу увагу делегати традиційно звертають на першу лекцію – почесний виступ, який зазвичай присвячений найсвіжішим і найвагомішим науковим відкриттям у галузі. Цього разу організатори вирішили здивувати делегатів. Тема першого виступу була геть несподіваною: «Як боротися з фейковими новинами в медицині?». Цю лекцію представила професорка Wendi LeBrett (США). Замість традиційного тріумфу наукових новин слухачі отримали глибокий і критичний аналіз того, як міфи та недостовірна інформація впливають на пацієнтів і професійну спільноту. Доповідачка констатувала сучасний тренд: пацієнти дедалі частіше отримують відомості про здоров’я через онлайн-платформи та соціальні мережі. Останні мають величезну аудиторію, і нерідко відео з недостовірними медичними порадами набирають мільйони переглядів: кількість переглядів таких відео може охоплювати аудиторію, порівнянну з населенням Данії. Лише 20% контенту про закрепи, запальні хвороби кишківника створено медичними фахівцями, а решта поширює недостовірну інформацію.
Доповідачка закликала колег ставати надійним джерелом інформації для громадськості, медичні організації – підтримувати наукову комунікацію, адаптуючи матеріали для онлайн-аудиторії та співпрацюючи з пацієнтськими організаціями.
Метаболічно-асоційована стеатотична хвороба печінки (МАСХП): нові дані
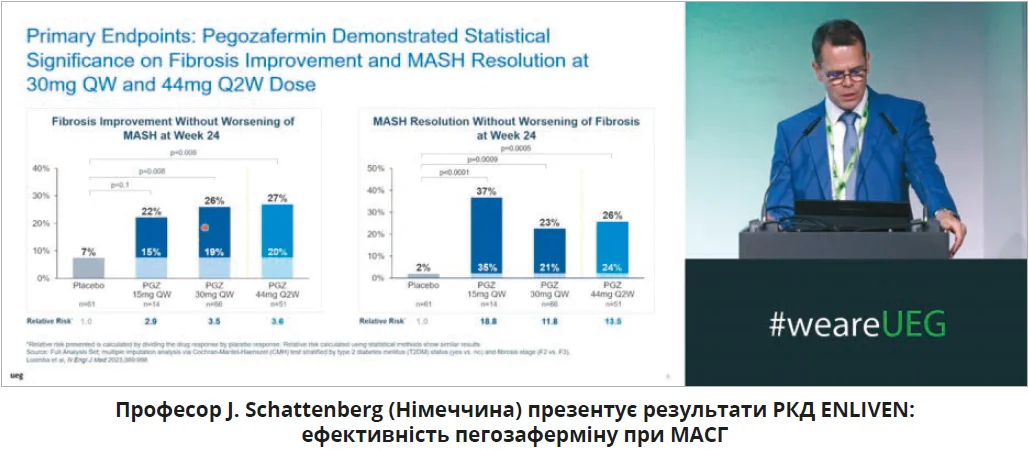
Після пленарної частини конгрес буквально «розгорнувся» на повну силу – десятки залів, сотні тем, тисячі учасників. Кожен міг знайти дискусію чи доповідь, найближчу до власних професійних інтересів. Серед численних наукових напрямів, представлених на цьогорічному конгресі, особливою увагою користувалися секції, присвячені МАСХП. Значну увагу на UEG Week 2025 привернула секція «Модифікація способу життя та терапія МАСХП», що зібрала рекордну кількість слухачів і стала однією з найдинамічніших. Відкрив її професор Jörn Schattenberg (Німеччина), представивши результати рандомізованого контрольованого дослідження (РКД) ENLIVEN, яке вперше показало, що експериментальний препарат пегозафермін не лише знижує активність метаболічно-асоційованого стеатогепатиту (МАСГ), а й сприяє регресу фіброзу печінки.
У РКД ENLIVEN (фаза IIb), проведеному за участю 222 пацієнтів з МАСГ і фіброзом F2-F3, через 24 тижні лікування констатовано регрес фіброзу печінки у 22-27% пацієнтів порівняно із 7% у групі плацебо (p <0,05). Зникнення ознак МАСГ відзначено майже в 37% пацієнтів. Препарат також покращував неінвазивні маркери хвороби: знижував рівні трансаміназ, жорсткість печінки та вміст жиру за даними МРТ. На думку професора Schattenberg, пегозафермін є одним з найперспективніших кандидатів для схвалення як препарату для лікування МАСГ.
Не менше зацікавлення викликала секція «Нова ера в лікуванні МАСГ: як цільові терапії змінюють правила гри», присвячена препарату ресметиром – першому схваленому цільовому засобу для лікування МАСГ. Ресметиром, селективний агоніст β-рецепторів тиреоїдних гормонів, активує β-оксидацію жирних кислот і знижує запалення та фіброз. У РКД MAESTRO-NASH (фаза III) через 52 тижні лікування гістологічне розрішення МАСГ досягнуто у 26-30% пацієнтів порівняно з 9,7% у групі плацебо, а регрес фіброзу зафіксовано у 24-26% хворих. Ресметиром рекомендований Управлінням США з контролю продовольства та медикаментів (FDA, 2024) і Європейським агентством з лікарських засобів (EMA, 2025) для лікування МАСГ у хворих з фіброзом F2-F3. Перспективним вважається вивчення ефективності комбінованої терапії ресметиромом з агоністами глюкагоноподібного пептиду-1 (зокрема семаглутидом). Імовірно, саме така комбінація сформує нову парадигму персоналізованої терапії МАСГ, де вибір лікування проводиться з урахуванням фенотипу пацієнта.
Саркопенія: що робити клініцисту
Одним з найпомітніших тематичних напрямів UEG Week 2025 стало обговорення ускладнень хронічних захворювань печінки. На сесії «Що нового в ускладненнях хронічних захворювань печінки 2025 року?» експерти представили оновлені стратегії ведення пацієнтів з портальною гіпертензією, енцефалопатією та метаболічними порушеннями, приділивши особливу увагу профілактиці й ранній діагностиці супутніх станів.
Жваву дискусію викликала доповідь професорки Francesca Ponziani (Італія) «Діагностика та лікування саркопенії при ураженнях печінки». Вона наголосила, що саркопенія (втрата м’язової маси та сили) виявляється майже в 40% пацієнтів із цирозом печінки й істотно погіршує прогноз, підвищуючи ризик енцефалопатії, інфекцій і смерті. Для клініцистів важливо не лише підтверджувати цей стан за допомогою тестів на силу хвату чи підведення з положення сидячи, а й оцінювати м’язову масу за допомогою МРТ, КТ або біоімпедансу. У своїй лекції професорка Ponziani розмежувала поняття саркопенії та крихкості (frailty): якщо перше характеризує суто втрату м’язів, то друге охоплює ширше зниження функціонального резерву організму. Серед ключових чинників розвитку саркопенії вона назвала мальнутрицію, гормональні зрушення, гіподинамію та порушення мікробіоти кишківника. Доповідачка закликала проводити регулярний моніторинг саркопенії (зокрема з використанням Liver Frailty Index) і здійснювати триступеневу профілактику: первинна – освіта пацієнтів, збалансоване харчування, фізична активність; вторинна – корекція виявлених дефіцитів, ведення багатодисциплінарною командою; третинна – спеціалізована реабілітація в тяжких випадках. Серед практичних порад: уникати тривалого голодування, допускати пізні перекуси, розглядати гормональну підтримку тестостероном у чоловіків і антиміостатинову терапію, що наразі активно досліджується.
Результати провідних РКД
UEG Week 2025 традиційно став майданчиком для представлення найразючіших результатів РКД, здатних змінити підходи до ведення гастроентерологічної патології. Цьогоріч серед найобговорюваніших тем стали наступні дані. У межах двох доповідей представлено результати РКД ABTECT-1 і ABTECT-2 (фаза III), які оцінювали ефективність нового перорального засобу обефазимод у пацієнтів з помірним/тяжким активним виразковим колітом, стійким до біологічної терапії чи інгібіторів Янус-кінази. Обефазимод – експериментальний препарат першого класу, що підсилює експресію мікроРНК-124, регулюючи запальну відповідь і відновлюючи мукозальний гомеостаз. У випробуваннях понад 1200 пацієнтів були рандомізовані до приймання 50, 25 мг або плацебо; клінічної ремісії досягли 20-24% пацієнтів із груп активного лікування порівняно з 2-6% хворих з контрольної групи.
Експерти зазначають, що обефазимод може стати перспективною опцією для пацієнтів, які вичерпали інші можливості лікування, та зручним засобом для ранніх етапів ведення виразкового коліту.
Ще однією ключовою подією стало представлення результатів III фази РКД GLISTEN, у якому оцінювали ефективність нового перорального інгібітора транспортера жовчних кислот лінерксиблату в лікуванні холестатичного свербежу при первинному біліарному холангіті. Як повідомив професор Andreas E. Kremer (Швейцарія), препарат швидко й істотно зменшує інтенсивність свербежу, покращує сон і має прийнятну переносимість. Через 24 тижні спостерігалося зниження інтенсивності свербежу за шкалою WI-NRS (Worst Itch Numeric Rating Scale) на 2,86 бала порівняно з 2,15 бала в групі плацебо (p=0,001), причому позитивну динаміку відзначали вже через 2 тижні. Поліпшення сну та зменшення частоти епізодів свербежу відзначала понад половина пацієнтів, а кожен п’ятий повідомив про повне зникнення симптомів. На думку професора Frank Tacke (Німеччина), це перший препарат, спрямований на контроль симптомів первинного біліарного холангіту, а не лише на досягнення біохімічної відповіді.
Функціональна патологія та дієта
Відомий дослідник нейрогастромоторики, професор Magnus Simrén (Швеція) представив доповідь «Терапевтичний підхід до порушень взаємодії кишківник – мозок: ліки чи дієта?», в якій наголосив на важливості функціонування осі кишківник – мозок. Хронічні або рецидивні функціональні розлади, які виникають при порушенні взаємодії центральної й ентеральної нервових систем, стають дедалі поширенішими. Найдослідженішим серед них є синдром подразненого кишківника (СПК), саме тому доповідач проаналізував місце дієтичних і фармакологічних підходів у терапії цієї патології. Більшість пацієнтів з СПК самі відзначають зв’язок симптомів з харчуванням, тому першим кроком у лікуванні є модифікація харчового раціону. У клінічних настановах Британського товариства гастроентерології й Американської гастроентерологічної асоціації саме дієтичні рекомендації стоять на початку алгоритму ведення пацієнта. На початковому етапі радять запроваджувати прості зміни: регулярно харчуватися невеликими порціями, зменшити частку жирної їжі, відмовитися від уживання кофеїну, алкоголю та зосередитися на виявленні індивідуальних тригерів. Якщо ці заходи неефективні, то призначають спеціальні дієти. Найчастіше рекомендують дієту з мінімальним умістом FODMAP (ферментовані оліго-, ди-, моносахариди й поліоли), яка обмежує споживання ферментованих вуглеводів. Саме вона, за даними метааналізів, демонструє найвищу ефективність, але є дуже складною для дотримання та може несприятливо впливати на кишкову мікробіоту.
Доповідач навів результати останніх досліджень, проведених під його керівництвом. Вони довели, що дієта зі зниженим умістом крохмалю та сахарози має подібну до дієти FODMAP ефективність, але є простішою й соціально прийнятнішою. У великому порівняльному дослідженні ефективність обидвох дієтичних стратегій перевершила таку оптимізованої медикаментозної терапії, зокрема в зменшенні здуття та болю в животі. Ефект зберігався навіть через пів року після завершення активного втручання, що свідчить про його стійкість. На думку доповідача, не варто протиставляти дієту й медикаментозну терапію. Оптимальний підхід полягає в поєднанні дієтичних, фармакологічних і поведінкових стратегій, адаптованих до індивідуальних потреб пацієнта. «Мета не в тому, щоб пацієнт дотримувався жорстких обмежень, – наголосив професор M. Simrén. – Головне навчити його розуміти свій організм і знаходити баланс між харчуванням, лікуванням та якістю життя».
UEG Week 2025 завершився, але його енергія продовжує надихати на нові ідеї, відкриття та співпрацю. Попереду UEG Week 2026 у Барселоні (Іспанія), котрий стане черговим підтвердженням того, що всі гастроентерологи у світі мають спільну мету та професійну пристрасть, і саме це втілює девіз #weareUEG.