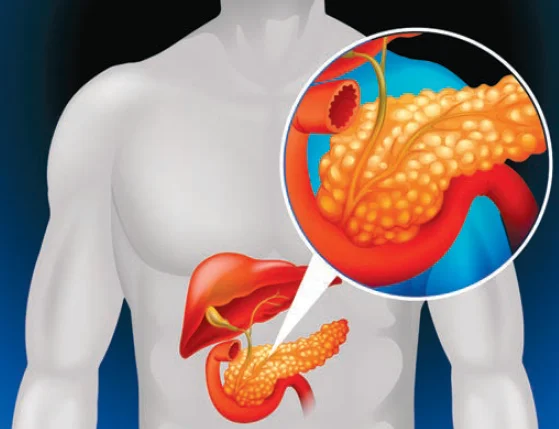
Взаємодія між екзокринною й ендокринною частинами підшлункової залози
Переклала й адаптувала канд. мед. наук Тетяна Можина
Підшлункова залоза (ПЗ) – це орган, розташований у заочеревинному просторі, позаду шлунка, в безпосередній близькості до дванадцятипалої кишки (ДПК), воріт печінки, селезінки. З давніх часів ПЗ цікавила науковців своєю анатомією та функціями, але розуміння анатомії ПЗ покращилося лише після публікації досліджень, проведених Йоганном Вірсунґом в Італії в 1642 р. Наступні дослідження Абрагама Фатера та Джованні Санторіні, які були проведені до середини 1700-х рр., представили повну картину анатомії ПЗ. Розуміння функцій ПЗ довелося чекати до кінця 1800-х рр. У 1850 р. Клод Бернар припустив, що ПЗ бере участь у травленні, й лише в 1890 р. Пауль Ланґерганс висунув гіпотезу щодо ролі ПЗ у розвитку цукрового діабету (ЦД) [1].
Вивченню взаємодії між двома компонентами ПЗ, екзокринною й ендокринною системами, досі відводиться значна увага в дослідженнях ПЗ.
Як свідчення цього, у 2022 р. відбулася окрема конференція, організована Національним інститутом діабету та хвороб органів травлення й нирок США (NIDDK). Її метою стало представлення останніх досягнень у галузі фізіопатології ПЗ серед медичних працівників різних спеціальностей, у тому числі педіатрів, діабетологів, терапевтів, гастроентерологів [2].
Мета цього огляду полягає у висвітленні найновіших даних у цій галузі та їх поширенні серед таких фахівців, як панкреатичні хірурги й ендоскопісти.
Фізіологія ПЗ
ПЗ є складним органом, який містить як ендокринний, так і екзокринний компонент. Екзокринна частина відповідає за вироблення, зберігання та секрецію ферментів ПЗ. Ацинарні клітини виробляють, зберігають і виділяють травні ферменти, включаючи амілазу, ліпазу, нуклеази та протеази (трипсиноген, хімотрипсин). Вивільнення цих ферментів стимулюється гормонами холецистокініном (ХЦК) і секретином [3, 4].
Секреція ПЗ ініціюється під час цефалічної та шлункової фаз травлення, але саме під час кишкової фази відбувається порожнинна фаза травлення [5, 6]. Остання фаза секреції ПЗ зумовлена переважно вивільненням ХЦК, нейроентероендокринного гормону. ХЦК вивільняється при взаємодії кишкової стінки із жирними кислотами, амінокислотами та кислим хімусом. ХЦК, своєю чергою, активує блукаючий нерв, що призводить до дегрануляції зимогена в ацинарних клітинах завдяки холінергічній стимуляції [7].
Контакт кислого хімусу зі слизовою оболонкою ДПК стимулює аферентні волокна, які походять з її стінки. Ці волокна сприяють розвитку ваго- вагального ентеропанкреатичного рефлексу, який активує інтрапанкреатичні постгангліонарні нейрони, котрі відіграють певну роль у стимулюванні ацинарної секреції [8]. Коли кислий хімус потрапляє в ДПК, рН порожнинного середовища знижується. Наявність як низького дуоденального рН, так і секретинових стимулів призводить до секреції натрію, хлориду, бікарбонату, води в головну панкреатичну протоку, які в підсумку потрапляють у просвіт ДПК. Цей процес відбувається за участю муковісцидозного трансмембранного каналу провідності й аквапоринів, що відіграє життєво важливу роль у полегшенні травлення. Секреція води та бікарбонату сприяє підвищенню рН кишківника, стабілізуючи тим самим активність ферментів ПЗ [9, 10].
Окрім екзокринної функції та вироблення травних ферментів, ПЗ також є ендокринним органом, який відіграє важливу роль у виробленні різних гормонів, відповідальних, серед іншого, за регуляцію рівня глікемії. Ендокринна частина ПЗ складається з п’яти підтипів острівцевих клітин: α-, β-, γ-, δ- та ε-клітин. Серед них більшість (75%) становлять β-клітини, які відповідають за вироблення аміліну й інсуліну [4]. Глюкагон виробляється α-клітинами, соматостатин – δ-клітинами, р-поліпептид – γ-клітинами, а грелін – ε-клітинами.
Інсулін і глюкагон чинять ключовий вплив у підтриманні гомеостазу глюкози. Інсулін сприяє засвоєнню глюкози в крові та її перетворенню на жирні кислоти за допомогою процесу, відомого як ліпогенез. Ці жирні кислоти запасаються та являють собою основний резерв енергії в організмі [11]. Глюкагон, 29-амінокислотний білок, виконує низку біологічних функцій, пов’язаних насамперед з регуляцією рівня глюкози. Секреція глюкагону запускається численними метаболічними сигналами, включаючи коливання рівня глікемії, специфічних амінокислот і потенційно вільних жирних кислот.
Стресові чинники, як-от активація симпатичної нервової системи, здатні стимулювати його вивільнення [12].
Взаємозв’язок між ендокринною й екзокринною частинами ПЗ
Різні гормони, що виробляються та вивільняються ендокринною частиною ПЗ, впливають на ацинарну функцію екзокринної ПЗ. Одним зі способів взаємодії є трофіка клітин. Інсулін діє як трофічний фактор в ацинарному епітелії, стимулюючи як синтез, так і секрецію амілази, одночасно сприяючи росту ацинарних клітин. Вплив панкреатичних поліпептидів, соматостатинів, греліну на секрецію менш вивчений, але вони можуть мати протилежні ефекти [9, 13]. Вплив глюкагону на ацинарну функцію є двоспрямованим і залежить від тривалості дії стимулу.
Другим потенційним механізмом взаємодії ендокринної та екзокринної частин ПЗ є фільтрація. У тваринних моделях продемонстровано, що острівці Ланґерганса діють як фільтри екзокринної частини ПЗ [14], оскільки анатомічно кровотік і токсичні агенти спочатку досягають острівців, а потім екзокринних клітин через острівцево-ацинарну портальну систему [15, 16].
Третім важливим аспектом, який запускається прийомом їжі, що варто враховувати у складній паракринній взаємодії, є одночасна стимуляція як екзокринної, так і ендокринної частини ПЗ.
Насправді, на регуляцію ендокринної частини ПЗ також впливають паракринні стимули з кишківника. Прийом їжі запускає секрецію численних кишкових пептидів, ключаючи гормони інкретин, глюкозозалежний інсулінотропний поліпептид (ГІП) і глюкагоноподібний пептид-1 (ГПП-1) [20]. ГІП і ГПП-1 вивільняються з клітин тонкої кишки та стимулюють функцію й виживання β-клітин, що призводить до посилення сигналізації інсуліну [21, 22]. ГПП-1 секретується у двофазному режимі при споживанні продуктів, багатих на вуглеводи, жири й амінокислоти, причому перша фаза відбувається приблизно через 10-15 хвилин після їди, а друга – через 30-60 хвилин. ГПП-1 сприяє вивільненню інсуліну у відповідь на підвищений рівень глікемії, стимулюючи β-клітини; він також стимулює вивільнення глюкагону та соматостатину [23].
Екзокринна недостатність ПЗ
Екзокринна недостатність ПЗ (ЕНПЗ) є наслідком хвороб, які призводять до втрати паренхіми ПЗ (хронічний або автоімунний панкреатит), обструкції протоки Вірсунґа (рак ПЗ), інактивації панкреатичних ферментів, спричинених гіперсекрецією соляної кислоти (синдром Золлінґера – Еллісона), чи станів, пов’язаних зі зниженням панкреатичної секреції (целіакія) [27-29]. Окрім первинних панкреатичних причин, важливо брати до уваги позапанкреатичні фактори (хірургічні втручання), котрі змінюють анатомію та координацію ферментативної секреції з проходженням кислого хімусу, нейрогормональні зміни й аномалії панкреатичної протоки [30-32]. Інші позапанкреатичні стани, пов’язані з ЕНПЗ, включають автоімунні хвороби (синдром Шеґрена, целіакія), інфекційні захворювання (вірус імунодефіциту людини, запальні хвороби кишківника) [29, 31, 33, 34].
Куріння сигарет і прийом таких препаратів, як соматостатин, пов’язані з 20% поширеністю ЕНПЗ [35]. ЦД (як 1-го, так і 2-го типу) є одним з найпоширеніших позапанкреатичних захворювань, асоційованих з ЕНПЗ [31].
ЕНПЗ характеризується недостатньою активністю ферментів ПЗ у кишківнику, що призводить до порушення перетравлення жирної їжі та зниження всмоктування жиророзчинних вітамінів [30]. Порушення секреції ферментів не ідеально корелює із симптомами недостатності ПЗ, оскільки певний ступінь залишкової секреції може компенсувати інша частина органа. Яскраві клінічні прояви, як-от стеаторея, можуть бути відсутні доти, доки функція залози не буде порушена на 90% [30].
Ацинуси ПЗ здатні підтримувати нормальну травну функцію навіть у разі значного зниження функціонального резерву [36].
ЕНПЗ може призвести до втрати ваги, мальнутриції, стеатореї, мальабсорбції жирів, порушення всмоктування жиророзчинних мікроелементів, включаючи вітаміни A, D, E та K [37]. Численні дослідження встановили кореляцію між хронічним панкреатитом і ЕНПЗ, зростанням ризику розвитку остеопорозу й остеопенії внаслідок порушення всмоктування вітаміну D [37]. ЕНПЗ асоційована з кволістю, серцево-судинними хворобами, інфекціями, раком і підвищенням смертності [38].
Поширеність ЕНПЗ при ЦД 1-го типу
ЦД 1-го типу асоційований з ЕНПЗ та вираженою атрофією паренхіми. У пацієнтів із ЦД 1-го типу об’єм і маса ПЗ зменшені, відповідно, на 19-50 і 55% порівняно з хворими на ЦД 2-го типу та здоровими особами [3, 4].
У дітей із ЦД 1-го типу спостерігають зменшення об’єму ПЗ на 16-61% [51, 52]. Цікаво, що переважна більшість втрати маси ПЗ відбувається під час першої фази ЦД [53]. Мікроскопічний аналіз виявляє наявність фіброзу, жирової дегенерації, що визначається як пропорційне збільшення вмісту жиру в залозі, та запальних інфільтратів у ПЗ пацієнтів із ЦД як 1-го, так і 2-го типу [54]. Ці ознаки також часто спостерігають у хворих на хронічний панкреатит і ЕНПЗ. На відміну від хронічного панкреатиту фіброз у діабетичній ПЗ зазвичай описують як внутрішньочасточковий/внутрішньоацинарний з ознаками атрофії ацинусів, а протоковий компонент залишається інтактним. Приблизно в 30% хворих на ЦД 1-го та 2-го типів спостерігається жирова інфільтрація ПЗ, у 47% – лімфоцитарна інфільтрація, мікросудинні зміни присутні майже в усіх пацієнтів під час автопсії, що проявляється потовщенням стінок дрібних артеріол [3].
У дітей, хворих на ЦД 1-го типу, поширеність тяжкої ЕНПЗ становить близько 10%, тоді як помірна ЕНПЗ спостерігається в 45% випадків. У дослідженні, проведеному Larger і співавт., вивчали наявність ЕНПЗ у когорті пацієнтів із ЦД. У дітей, хворих на ЦД 1-го типу (n=95), поширеність тяжкої ЕНПЗ, яку діагностували при зниженні вмісту фекальної еластази-1 <200 мкг/г, становила 34% [45, 55, 56].
За оцінками, близько 10-30% дорослих із ЦД 1-го типу страждають на тяжку ЕНПЗ, тоді як 22-56% пацієнтів із цієї когорти мають помірну ЕНПЗ [56].
ЕНПЗ при ЦД 1-го типу може проявлятися такими симптомами, як діарея, здуття живота, спастичний біль, втрата маси тіла [21]. Симптоми ЕНПЗ при ЦД 1-го типу часто перетинаються з іншими ускладненнями ЦД, включаючи автономну нейропатію, целіакію та бактерійні інфекції.
Поширеність ЕНПЗ при ЦД 2-го типу
Дані про поширеність ЕНПЗ у дорослих із ЦД 2-го типу є численними, хоча й неоднорідними. У дослідженні Е. Larger і співавт. у когорті хворих на ЦД 2-го типу (n=472) поширеність тяжкої ЕНПЗ становила 20% [56].
Lidkvist і співавт. аналізували рівень фекальної еластази-1 і харчовий статус у хворих на ЦД 2-го типу (n=315). Дослідження показало, що поширеність тяжкої ЕНПЗ становить 5,2%, легкої ЕНПЗ – 4,9% [59].
У великому проспективному дослідженні, проведеному за участю хворих на ЦД (n=1231), поширеність ЕНПЗ у когорті пацієнтів із ЦД 2-го типу (n=697) становила 35%. Однак дослідження не виявило жодних значущих зв’язків між тривалістю хвороби й інсулінотерапією в підгрупі хворих на ЦД 2-го типу, на відміну від спостережень, зроблених у загальній популяції (n=1231). Це свідчить про те, що інші чинники, крім тривалості хвороби й інсулінотерапії, можуть зумовлювати розвиток ЕНПЗ в осіб із ЦД 2-го типу [46].
Висновки
Ендокринна й екзокринна частини ПЗ взаємодіють, і хвороби, що вражають одну з них, здатні впливати на іншу. Хоча поширеність ЕНПЗ при ЦД 1-го та 2-го типів досліджувалася в перехресних дослідженнях, частота виникнення хвороби при ЦД описана недостатньо добре. Приблизно ½ пацієнтів із ЦД 1-го типу та 1/3 хворих на ЦД 2-го типу мають ЕНПЗ, яка асоціюється з більшою тривалістю хвороби та поганим глікемічним контролем. Потрібні подальші дослідження для визначення точної поширеності ЕНПЗ у хворих на ЦД й оцінювання можливості покращення глікемічного контролю та зниження ризику потенційно небезпечних гіпоглікемічних епізодів за допомогою замісної терапії панкреатичними ферментами.
Література
Valente R., et al. Interactions between the exocrine and the endocrine pancreas. J. Clin. Med. 2024; 13 (4): 1179. doi: 10.3390/jcm13041179.