Втома при хронічних захворюваннях печінки: фокус на метаболічно-асоційовану стеатотичну хворобу печінки
Автор: Ігор Миколайович СКРИПНИК, доктор медичних наук, професор, президент ГО «Українська гастроентерологічна асоціація», проректор із науково-педагогічної роботи та післядипломної освіти, професор кафедри внутрішньої медицини № 1 Полтавського державного медичного університету
 Метаболічно-асоційована стеатотична хвороба печінки (МАСХП) визнана найпоширенішим хронічним захворюванням печінки (ХЗП) у світі. Глобальна поширеність МАСХП серед дорослого населення становить близько 30-32% [13]. Цей показник продовжує зростати на тлі епідемії ожиріння, метаболічного синдрому та цукрового діабету (ЦД) 2-го типу [3, 5, 10, 13]. У групах високого кардіометаболічного ризику поширеність МАСХП значно вища: її виявляють у 70-75% осіб з надмірною масою тіла / ожирінням і в ≥55% пацієнтів із ЦД 2-го типу [10]. Щороку реєструють близько 138 тис. асоційованих з МАСХП летальних випадків, включно з приблизно 97 тис. смертей від цирозу печінки, що розвинувся на її тлі [5].
Метаболічно-асоційована стеатотична хвороба печінки (МАСХП) визнана найпоширенішим хронічним захворюванням печінки (ХЗП) у світі. Глобальна поширеність МАСХП серед дорослого населення становить близько 30-32% [13]. Цей показник продовжує зростати на тлі епідемії ожиріння, метаболічного синдрому та цукрового діабету (ЦД) 2-го типу [3, 5, 10, 13]. У групах високого кардіометаболічного ризику поширеність МАСХП значно вища: її виявляють у 70-75% осіб з надмірною масою тіла / ожирінням і в ≥55% пацієнтів із ЦД 2-го типу [10]. Щороку реєструють близько 138 тис. асоційованих з МАСХП летальних випадків, включно з приблизно 97 тис. смертей від цирозу печінки, що розвинувся на її тлі [5].
Водночас перебіг МАСХП тісно пов’язаний із психоемоційними порушеннями та зниженням якості життя [4]. Одним із ключових симптомів, який визначає це зниження, є втома, котра часто поєднується з психоемоційними порушеннями [4]. Систематичний огляд і метааналіз 31 дослідження (n=2 126 593) довели, що депресію виявляють приблизно у 26% пацієнтів з МАСХП / неалкогольною жировою хворобою печінки (НАЖХП), тривогу – у 37%, а ознаки хронічного стресу – майже в половини хворих [12].
З огляду на високу поширеність втоми та її значний вплив на повсякденну активність, постає важливе завдання: зрозуміти механізми виникнення втоми при ХЗП, МАСХП і визначити ефективні підходи до її корекції.
Втома при ХЗП: «простий» симптом зі складною патофізіологією
Втома є одним з найбільш поширених і найменш специфічних симптомів, адже вона супроводжує перебіг різних захворювань. Пацієнти описують таку втому як стійке відчуття виснаження, зниження енергії та працездатності, яке не відповідає рівню фізичного навантаження й часто не минає після відпочинку. Доведено, що патологічна втома асоціюється зі значним зниженням якості життя, погіршенням якості сну, а також є фактором, асоційованим зі зростанням смертності у 2,3 раза серед хворих на НАЖХП [15].
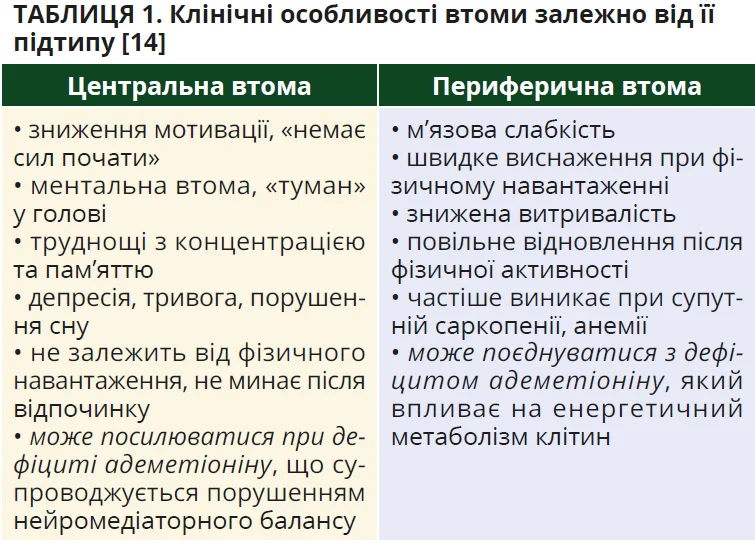
Нині втому розглядають як складний багатофакторний симптом, формування котрого зумовлене взаємодією центральних (пов’язаних з функцією центральної нервової системи) та периферичних механізмів. З патофізіологічного погляду розрізняють центральну й периферичну втому (табл. 1).
Центральна втома формується внаслідок порушення активності нейромедіаторних систем головного мозку (ГМ) і дисфункції так званих центрів винагороди. Периферична втома, навпаки, пов’язана переважно з нейром’язовою дисфункцією та порушенням енергетичного забезпечення м’язів [14].
Окреме місце серед них посідає так звана гепатогенна (патологічна) втома – особливий варіант центральної втоми, характерний для пацієнтів
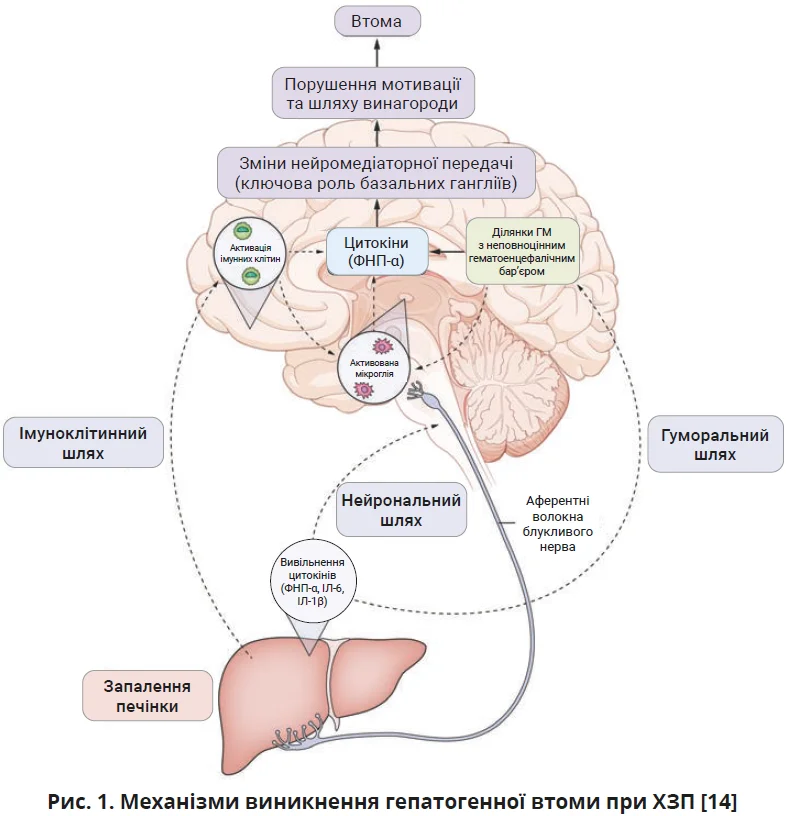
з ХЗП. Її розвиток пов’язують з порушенням взаємодії між печінкою та центральною нервовою системою. Важливу роль у цьому процесі відіграє системне низькоінтенсивне запалення, що виникає при ушкодженні печінки та прогресуванні фіброзу. Прозапальні цитокіни (фактор некрозу пухлин-α (ФНП-α), інтерлейкін-6 (ІЛ-6), IЛ-1β), які утворюються в печінці, потрапляють у системний кровообіг і впливають на функціонування ГМ, змінюючи нейроімунні та нейрохімічні процеси. Передача сигналів від печінки до ГМ відбувається нейрональним, гуморальним та імуноклітинним шляхами (рис. 1).
Унаслідок цього змінюється нейромедіаторна передача у структурах ГМ, які регулюють мотивацію та поведінкові реакції: знижується синтез дофаміну, змінюється серотонінергічна передача й підвищується активність гальмівних нейромедіаторів. Такі нейрохімічні зміни порушують роботу центрів мотивації, емоцій і когнітивних функцій, що клінічно проявляється типовим комплексом симптомів ХЗП: втомою, депресією та когнітивними порушеннями [14].
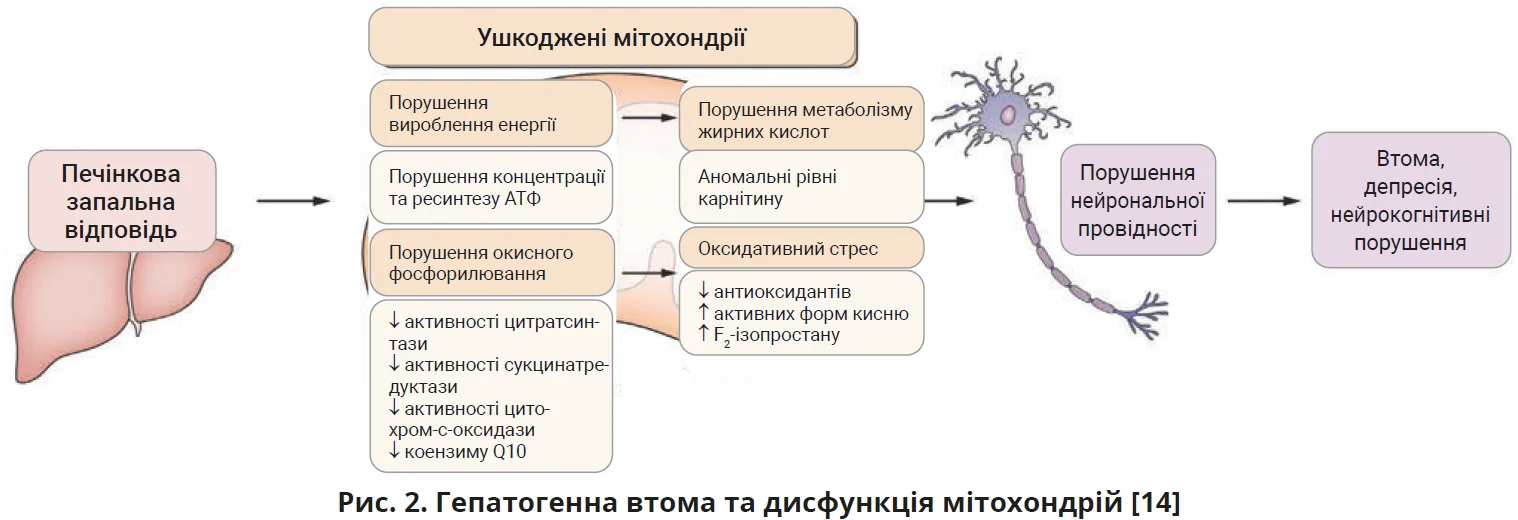
Утім, гепатогенна втома не завжди має виключно центральний характер і може поєднуватися з периферичними механізмами. Зокрема, при ХЗП описано порушення функції мітохондрій у м’язових клітинах, що супроводжується зниженням синтезу аденозинтрифосфату (АТФ), порушенням метаболізму жирних кислот і посиленням оксидативного стресу. Унаслідок цього знижується енергетичний потенціал клітин, що спричиняє формування м’язової слабкості, швидке виснаження під час фізичного навантаження [14].
Додаткову роль у цих процесах може відігравати зниження рівня S-адеметіоніну (SAMe), що характерне для внутрішньопечінкового холестазу (ВПХ) та ХЗП. Дефіцит SAMe супроводжується посиленням оксидативного стресу та дисфункцією мітохондрій, що може погіршувати енергетичне забезпечення клітин і спричиняти розвиток периферичних проявів втоми [2, 9]. Крім цього, SAMe залучений у процеси регуляції синтезу та метаболізму деяких нейромедіаторів (дофамін, серотонін), тому його зниження потенційно може впливати й на центральні механізми формування втоми.
Гепатогенна втома: така однакова й така різна
Втома є одним з найпоширеніших симптомів ХЗП. Хоча механізми її розвитку мають багато спільного, клінічні прояви, поширеність і тяжкість цього симптому значною мірою залежать від етіології хвороби. Зокрема, при холестатичних захворюваннях печінки (первинний біліарний холангіт, первинний склерозивний холангіт) втома часто є першим і домінувальним симптомом і може мати інвалідизувальний характер. Вона нерідко зберігається навіть за контролю перебігу основної хвороби.
При вірусних гепатитах, особливо при HCV- інфекції, втома також є типовим клінічним проявом. Її інтенсивність не завжди залежить від рівня віремії або активності запального процесу в печінці. Хоча ерадикація вірусу на тлі сучасної противірусної терапії може сприяти зменшенню вираженості втоми, повне її зникнення спостерігається не в усіх пацієнтів [14]. Важливу роль у формуванні цього симптому відіграють психоемоційні чинники, зокрема депресія та тривога.
Гепатогенна втома спостерігається приблизно в 40% пацієнтів з МАСХП, але часто залишається недооціненою як пацієнтами, так і лікарями. Її розвиток тісно пов’язаний з кардіометаболічними порушеннями, зокрема ожирінням та інсулінорезистентністю. Водночас інтенсивність гепатогенної втоми часто не корелює з активністю цитолізу або стадією фіброзу печінки. У пацієнтів з МАСХП гепатогенна втома часто поєднується з депресивними симптомами, порушенням сну, когнітивними скаргами, а також проявами периферичної втоми, зумовленої саркопенією або ожирінням [14]. Терапія МАСХП, спрямована на зниження маси тіла та регресію фіброзу, може сприяти зменшенню вираженості гепатогенної втоми. Водночас саме цей симптом часто обмежує можливість модифікації способу життя.
У пацієнтів з алкогольним ураженням печінки гепатогенна втома нерідко поєднується з депресією, саркопенією та дефіцитом мікронутрієнтів, що формує вираженіший периферичний компонент астенії. При цирозі печінки будь-якої етіології вираженість гепатогенної втоми зазвичай зростає з прогресуванням хвороби, особливо при розвитку анемії, саркопенії або гіперамоніємії. У багатьох випадках вона поєднується з когнітивною дисфункцією, що додатково погіршує функціональний стан пацієнтів.
Виміряти невимірюване: дієві способи оцінювання втоми
Втому при ХЗП оцінюють за допомогою об’єктивних функціональних тестів і стандартизованих опитувальників, що дає змогу розрізняти периферичні та центральні механізми цього симптому. Периферичну втому оцінюють за допомогою тестів фізичної витривалості та м’язової сили (тредміл, нейром’язові тести, тест 6-хвилинної ходьби).
Центральну втому визначають переважно за допомогою валідованих шкал (Fatigue Severity Scale, Fatigue Impact Scale, Multidimensional Fatigue Inventory), які дають змогу оцінити фізичний, когнітивний і соціальний компоненти втоми. Коротку валідовану шкалу Fatigue Assessment Scale (FAS) часто використовують у хворих на МАСХП.
Додаткову інформацію про центральну втому надають опитувальники якості життя, зокрема компонент Vitality шкали SF-36 і Chronic Liver Disease Questionnaire (CLDQ); шкали PBC-40 або PBC-27 спеціалізовані для холестатичних захворювань. Оскільки втома часто поєднується з психоемоційними порушеннями, депресію та тривогу у хворих на ХЗП оцінюють за допомогою шкали HADS або шкали депресії Бека.
Лікування гепатогенної втоми
- Загальні підходи
Специфічні фармакологічні методи лікування гепатогенної втоми при ХЗП наразі обмежені, що зумовлено складним і багатофакторним патогенезом цього симптому. У позиційному документі European Reference Network for Rare Liver Diseases (2026), присвяченому проблемі гепатогенної втоми в пацієнтів з первинним біліарним холангітом, експерти пропонують використовувати структурований алгоритм ask – measure – treat для системного оцінювання та ведення цього симптому [6]. Перший етап (ask) передбачає активний скринінг утоми під час клінічного прийому. Лікарю рекомендується цілеспрямовано уточнювати, чи відчуває пацієнт утому більшою, ніж раніше, чи впливає вона на працездатність і повсякденну активність. Наступний етап (measure) полягає у визначенні вираженості втоми за допомогою валідованих шкал. Одночасно доцільно провести лабораторне обстеження, включно з визначенням рівнів гемоглобіну, тиреотропного гормону, глюкози, феритину, вітамінів B12 і D [6]. Етап treat передбачає багатокомпонентне лікування, спрямоване як на терапію основної хвороби печінки, так і на корекцію факторів, які можуть посилювати гепатогенну втому.
З огляду на обмежену доказову базу фармакологічного лікування, важливу роль відіграють підтримувальні та поведінкові стратегії ведення пацієнтів. Одним із практичних прикладів такого структурованого підходу є концепція TrACE, яка передбачає послідовне виявлення та лікування корегованих причин утоми, зменшення факторів, що її погіршують, навчання пацієнта ефективним стратегіям подолання симптомів і формування емпатійної взаємодії між лікарем і пацієнтом (табл. 2).
Поки що не розроблено специфічної терапії гепатогенної втоми при ХЗП, тому лікування має бути комплексним і спрямованим на лікування основної хвороби печінки, корекцію сну, підтримання фізичної активності та психологічну підтримку [11]. Попри важливість немедикаментозних заходів, пошук ефективних фармакологічних підходів до корекції гепатогенної втоми триває [11]. З огляду на роль системного запалення, мітохондріальної дисфункції та порушень нейромедіаторного балансу в її патогенезі, значну увагу привертають препарати, здатні впливати на ці механізми. Одним з таких засобів є S-адеметіонін (SAMe), який бере участь у процесах метилювання, синтезі нейромедіаторів і підтриманні функції мітохондрій.
Патогенетичний підхід до корекції гепатогенної втоми при ВПХ та ХЗП: роль SAMe
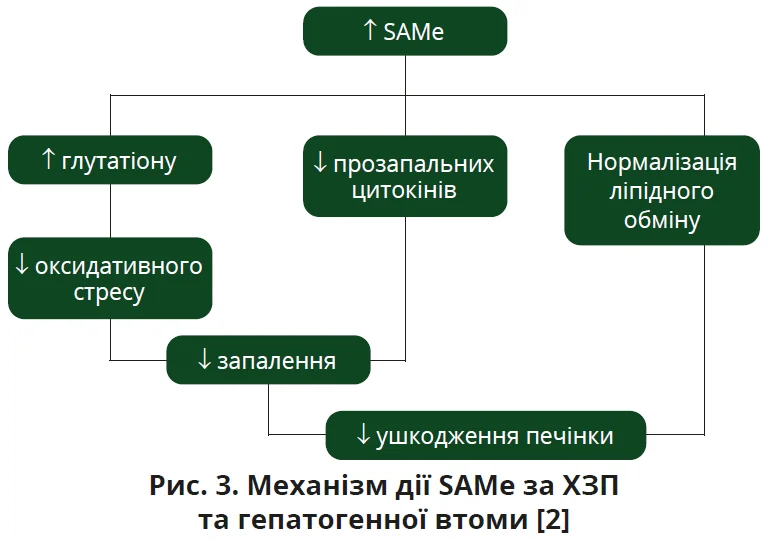
SAMe, ендогенна молекула, має плейотропні біологічні ефекти та впливає на кілька ключових ланок патогенезу ХЗП. Як донор метильних груп, SAMe бере участь у синтезі нейромедіаторів, регуляції ліпідного обміну й підтриманні антиоксидантного захисту клітини. Підвищуючи рівень глутатіону, SAMe зменшує оксидативний стрес, модулює запальні процеси та підтримує функціонування мітохондрій (рис. 3). Його участь у метаболізмі дофаміну й серотоніну також пов’язує печінкові метаболічні процеси з нейромедіаторною регуляцією центральної нервової системи [2, 9]. Такий комплексний вплив створює патогенетичні передумови для використання SAMe не лише як молекули з гепатопротекторною активністю, а і як засобу корекції гепатогенної втоми при ВПХ та ХЗП [2, 9].
Слід зауважити, що значну частину клінічних досліджень, які сформували доказову базу ефективності й безпеки SAMe при різноманітних ХЗП та ВПХ, проведено із застосуванням оригінального препарату, зареєстрованого в нашій країні під торговою назвою Гептрал®.
Експериментальні дослідження підтверджують, що SAMe здатний впливати на ключові патогенетичні механізми ураження печінки. Зокрема, показано, що препарат зменшує оксидативний стрес і апоптоз клітин, активуючи сигнальний шлях ФНП-α/Nrf2/HO-1 і посилюючи синтез глутатіону. У моделях холестатичного ушкодження печінки SAMe захищав холангіоцити від дії оксидативного стресу, знижував інтенсивність запальних реакцій, що свідчить про його антиоксидантні та цитопротекторні властивості [1].
Клінічні дані також підтверджують гепатопротекторний потенціал SAMe. У систематичному огляді 15 клінічних досліджень продемонстровано, що застосування SAMe асоціюється з покращенням біохімічного профілю печінки: в усіх включених дослідженнях відзначено позитивну динаміку печінкових маркерів (аланінамінотрансферази, аспартатамінотрансферази, γ-глутамілтранспептидази, білірубіну, лужної фосфатази, альбуміну). При цьому ефективність SAMe було продемонстровано при різних ХЗП, включно з МАСХП, холестатичними хворобами, вірусними гепатитами, алкогольною хворобою печінки, медикаментозно-індукованим ураженням печінки. В окремих дослідженнях застосування SAMe супроводжувалося не лише покращенням лабораторних показників, але й зменшенням гепатогенної втоми при ВПХ і ХЗП та підвищенням якості життя пацієнтів [2].
SAMe також проявляє синергічну дію при одночасному застосуванні з іншими препаратами. Зокрема, додавання SAMe підсилює ефект урсодезоксихолевої кислоти та преднізолону при, відповідно, холестатичних захворюваннях печінки й алкогольному гепатиті; введення SAMe до схеми лікування онкологічних хворих супроводжується зменшенням гепатотоксичності хіміотерапії [2]. Найпоширенішим є режим дозування SAMe 1000-1500 мг/добу з можливістю розпочати з введення препарату внутрішньовенно або внутрішньом’язево у перші 7-14 днів із наступним переходом на пероральний прийом.
Ефективність SAMe у нівелюванні гепатогенної втоми при ВПХ та ХЗП продемонстровано і в інших клінічних ситуаціях. Наприклад, у систематичному огляді 33 клінічних досліджень, у яких аналізували ефективність нутритивних утручань у подоланні втоми на тлі онкологічних захворювань, SAMe визнаний одним з перспективних засобів для зменшення цього симптому [8].
Відомо, що формування центральної втоми тісно пов’язане з порушенням нейромедіаторної регуляції в центральній нервовій системі. Зазначені механізми лежать в основі не лише астенії, а й афективних розладів, зокрема депресії. Це пояснює, чому симптоми втоми й депресії при ХЗП часто поєднуються та взаємно посилюють один одного. У таких випадках SAMe виявляє себе не лише як гепатопротектор, а і як потенційний засіб, здатний впливати на нейромедіаторний баланс і емоційний стан пацієнтів.
Висновки
Втома є одним з найпоширеніших, але водночас недооцінених симптомів ХЗП, зокрема МАСХП. Виникнення втоми має багатофакторний характер і зумовлено центральними та периферичними механізмами. Гепатогенна втома часто супроводжує перебіг різноманітних ХЗП. Системний підхід до її оцінювання (скринінг, використання валідованих шкал) є важливим компонентом ведення пацієнтів з МАСХП. Зважаючи на провідну роль запалення, оксидативного стресу, зміни вмісту нейромедіаторів у виникненні гепатогенної втоми, перспективним напрямом її патогенетичної корекції є застосування SAMe. SAMe не лише сприяє нормалізації функціональних показників печінки, але й може зменшувати прояви як центральної, так і периферичної втоми, що робить доцільним його застосування при різних ХЗП, зокрема МАСХП, які супроводжуються ВПХ.
Література
- Angelara M., Papachristou K., Papatheodoridi M., et al. Primary biliary cholangitis. Treatment options in 2025. A narrative review. Frontiers in Immunology. 2025; 16: 1698833. doi: 10.3389/fimmu.2025.1698833.
- Baden K.E.R., McClain H., Craig E., et al. S-adenosylmethionine (SAMe) for liver health: a systematic review. Nutrients. 2024; 16 (21): 3668. doi: 10.3390/nu16213668.
- Danpanichkul P., Suparan K., Diaz L.A., et al. The rising global burden of MASLD and other metabolic diseases (2000-2021). United European Gastroenterology Journal. 2025; 13 (7): 1141-1154. doi: 10.1002/ueg2.70072.
- Golubeva J.A., Sheptulina A.F., Yafarova A.A., et al. Reduced quality of life in patients with non-alcoholic fatty liver disease may be associated with depression and fatigue. Healthcare. 2022; 10 (9): 1699. doi: 10.3390/healthcare10091699.
- Guo Z., Wu D., Mao R., et al. Global burden of MAFLD, MAFLD related cirrhosis and MASH related liver cancer from 1990 to 2021. Scientific Reports. 2025; 15: 7083. doi: 10.1038/s41598-025-91312-5.
- Koc O.M., Toussaint A.K., Untas A., et al. Fatigue in people with primary biliary cholangitis: a position paper from the European Reference Network for Rare Liver Diseases. The Lancet Gastroenterology and Hepatology. 2026; 11 (1): 71-86. doi: 10.1016/S2468-1253(25)00257-2.
- Kośnik A., Wójcicki M. Fatigue in chronic liver disease patients: prevalence, pathophysiology, and management. Przeglad Gastroenterologiczny. 2022; 17 (1): 21-27. doi: 10.5114/pg.2022.114594.
- Li M., Zhang Y., Liu J., et al. Complementary and alternative medicine: a narrative review of nutritional approaches for cancer-related fatigue. Medicine. 2024; 103 (11): e37480. doi: 10.1097/MD.0000000000037480.
- Limveeraprajak N., Nakhawatchana S., Visukamol A., et al. Efficacy and acceptability of S-adenosyl-L-methionine (SAMe) for depressed patients: a systematic review and meta-analysis. Progress in Neuro-Psychopharmacology and Biological Psychiatry. 2024; 132: 110985. doi: 10.1016/j.pnpbp.2024.110985.
- Lou T.W., Yang R.X., Fan J.G. The global burden of fatty liver disease: the major impact of China. Hepatobiliary Surgery and Nutrition. 2024; 13 (1): 119-123. doi: 10.21037/hbsn-23-556.
- Niezen S., Noll A., Bamporiki J., et al. Management of fatigue and sleep disorders in patients with chronic liver disease. Clinical Liver Disease. 2024; 23 (1): e0122. doi: 10.1097/CLD.0000000000000122.
- Shea S., Lionis C., Kite C., et al. Non-alcoholic fatty liver disease and coexisting depression, anxiety and/or stress in adults: a systematic review and meta-analysis. Frontiers in Endocrinology. 2024; 15: 1357664. doi: 10.3389/fendo.2024.1357664.
- Younossi Z.M., Golabi P., Paik J.M., et al. The global epidemiology of nonalcoholic fatty liver disease (NAFLD) and nonalcoholic steatohepatitis (NASH): a systematic review. Hepatology. 2023; 77 (4): 1335-1347. doi: 10.1097/HEP.0000000000000004.
- Younossi Z.M., Kremer A.E., Swain M.G., et al. Assessment of fatigue and its impact in chronic liver disease. Journal of Hepatology. 2024; 81 (4): 726-742. doi: 10.1016/j.jhep.2024.04.008.
- Younossi Z.M., Paik J.M., Golabi P., et al. The impact of fatigue on mortality of patients with non-alcoholic fatty liver disease: data from National Health and Nutrition Examination Survey 2005-2010 and 2017-2018. Liver International. 2022; 42 (12): 2646-2661. doi: 10.1111/liv.15437.