Сучасні підходи до диференційної діагностики туберкульозу кишківника та хвороби Крона
Переклала й адаптувала канд. біол. наук Олександра Демецька
У країнах з високою поширеністю туберкульозу (ТБ) та зростанням частоти хвороби Крона диференціація цих двох гранульоматозних захворювань залишається складним завданням. Жоден окремий симптом, ендоскопічна ознака чи лабораторний тест не є достатньо специфічним. Помилкове призначення імуносупресивної терапії при невиявленому ТБ може призвести до генералізованої інфекції, тоді як затримка лікування хвороби Крона загрожує тяжкими ускладненнями. Це актуалізує сучасні алгоритми діагностики, ключові клінічні та морфологічні відмінності, а також роль пробного курсу протитуберкульозної терапії (ПТТ) за діагностичної невизначеності [1].
Клінічний випадок
Чоловік 57 років, мешканець Нью-Делі (Індія), звернувся у вересні 2024 року зі скаргами на періодичну появу крові у випорожненнях і чергування закрепів і діареї протягом останніх 2 років. Він повідомив про супутні симптоми втоми та прогресивної втрати ваги. Його початкова маса тіла становила 50 кг. Лихоманки чи нічної пітливості в анамнезі не було. Під час клінічного огляду не виявлено значних абдомінальних або позаабдомінальних змін, окрім блідості. Пацієнт не курить, не має історії зловживання психоактивними речовинами та відомих супутніх захворювань. Він заперечує контакт з відомими випадками ТБ, приймання ПТТ в минулому, а також історію ТБ або запальних захворювань кишківника в родині.
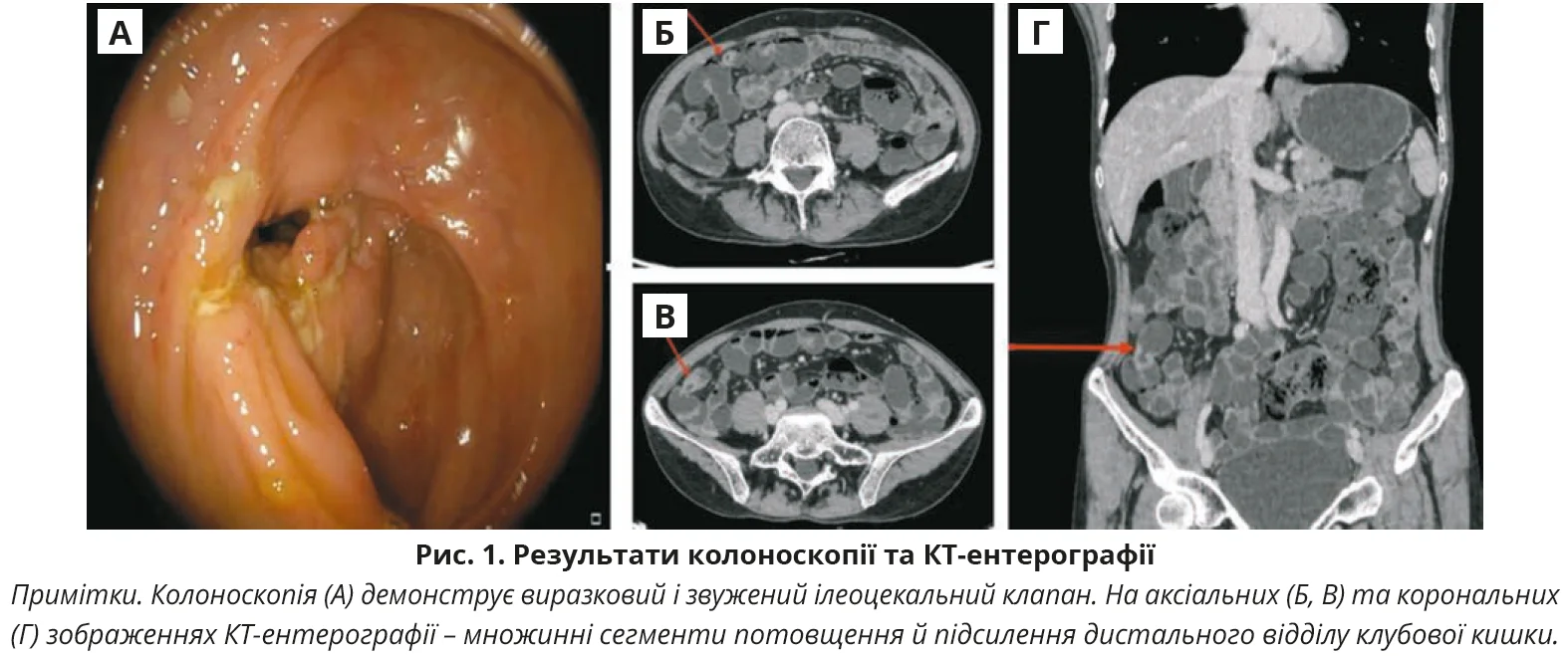
Колоноскопія (вересень 2024 року) виявила виразковий стеноз, що охоплює ілеоцекальний клапан (рис. 1, А). Ендоскоп не вдалося провести за межі стенозу. Біопсії слизової оболонки зі стенозу продемонстрували хронічний активний коліт без ознак гранульом. У відібраних тканинах не виявлено дисплазії або злоякісності. Фарбування за Цілем – Нільсеном, полімеразна ланцюгова реакція (ПЛР) на ТБ, молекулярний тест TB GeneXpert і культуральне дослідження біоптатів були негативними.
Лабораторні дослідження на цей момент показали рівень гемоглобіну 10 г/дл, без еозинофілії чи лейкоцитозу. Показники функції печінки, нирок і рівень альбуміну в сироватці були в межах норми. С-реактивний білок був підвищений. Тест на вивільнення інтерферону-γ (IGRA) та туберкулінова проба були негативними. Серологія на вірус імунодефіциту людини – негативна.
Контрастно-підсилена КТ-ентерографія виявила множинні ділянки потовщення стінки в дистальних петлях клубової кишки (рис. 1, Б-Г). Не було чітких ознак нориць, абсцесів або періанальної патології. Мезентеріальної лімфаденопатії чи асциту не виявлено. Зображення грудної клітки – без патології.
Клінічна картина, ендоскопічні знахідки та відсутність мікробіологічного підтвердження актуалізували питання тактики подальшого ведення пацієнта на цьому етапі діагностичного процесу. Серед можливих рішень розглядалися:
- проведення позитронно-емісійної томографії з КТ для розширеної оцінки розповсюдженості процесу;
- ініціація кортикостероїдної терапії, орієнтованої на хворобу Крона, за наявності відповідних клініко-ендоскопічних аргументів;
- хірургічна резекція ураженого сегмента як варіант при ускладненнях або невизначеності діагнозу після повного дообстеження;
- пробний курс ПТТ, який у регіонах з високою поширеністю ТБ може бути доцільним за діагностичної невизначеності та відсутності протипоказань.
Зважаючи на епідеміологічний контекст, перекриття клінічних і морфологічних ознак і ризики імуносупресії при невиявленому ТБ, на цьому етапі найобґрунтованішим рішенням є початок пробного курсу ПТТ з плановим повторним ендоскопічним і клінічним оцінюванням через 8-12 тижнів. Це дає змогу підтвердити запальний процес інфекційної природи в разі загоєння слизової оболонки та водночас мінімізує ризики несвоєчасного або неправильного призначення імуносупресії.
Багатодисциплінарне обговорення випадку
Гістологічне дослідження виключило еозинофільний ентерит і злоякісність, залишивши два основні діагностичні варіанти: хворобу Крона та ТБ кишківника. Ця дилема є особливо актуальною в регіонах з високою поширеністю ТБ, де обидві хвороби демонструють значне перекриття клінічних, ендоскопічних, візуалізаційних і морфологічних ознак.
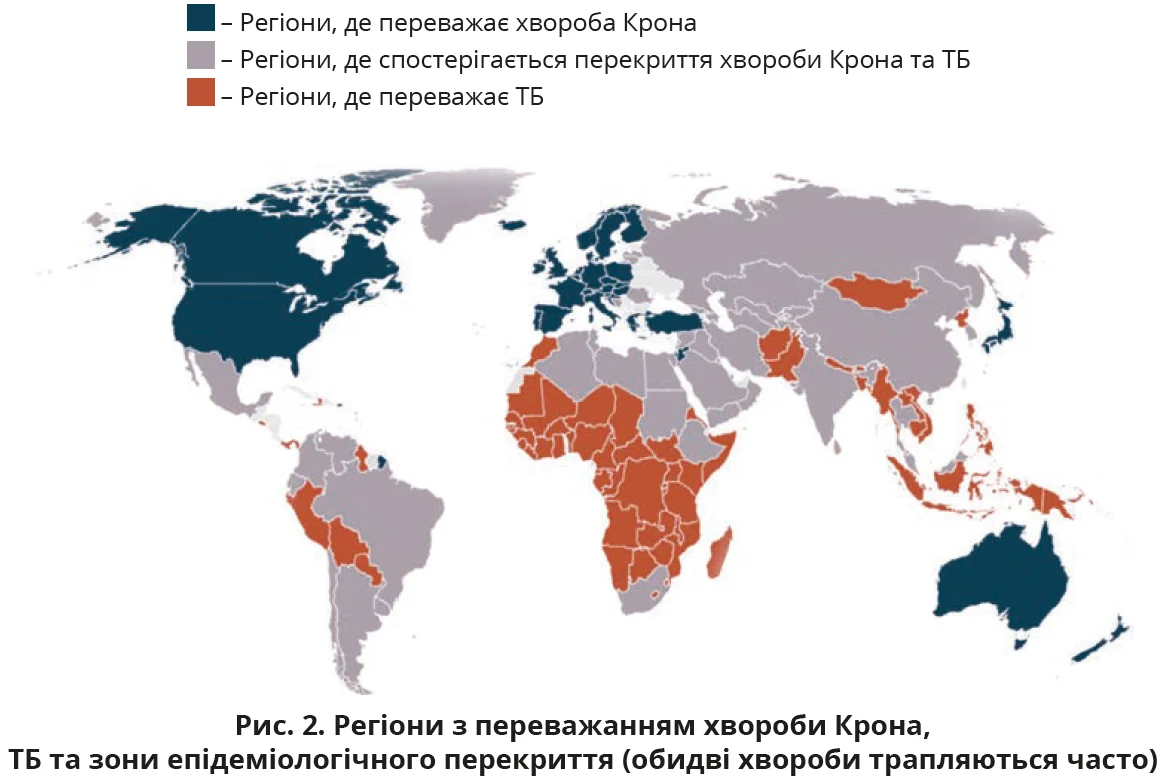
ТБ кишківника діагностично складніший за легеневий, оскільки має малобактерійний характер і низьку чутливість мікробіологічних тестів, тоді як легеневий ТБ легко підтверджується за допомогою мазків, культур і ПЛР. Найбільші труднощі виникають у регіонах, де ТБ є ендемічним, а захворюваність на хворобу Крона зростає (Індія, Китай, Південна Корея, Латинська Америка, Південно-Східна Азія, Південна Африка) (рис. 2). Поширеність ТБ у цих регіонах коливається від 29 до 195 на 100 тис. населення, ТБ кишківника – 0,4-3,9 на 100 тис., хвороби Крона – 1-3 на 100 тис. Це контрастує з регіонами, в яких переважає хвороба Крона, наприклад США, де захворюваність на ТБ становить 3,1 на 100 тис. населення, на ТБ кишківника – 0,05 на 100 тис., а на хворобу Крона – 5 на 100 тис. Вочевидь, у зазначених регіонах поширеність ТБ значно перевищує показники хвороби Крона, що визначає необхідність регіонально-специфічних діагностичних алгоритмів.
Клінічні ознаки обох станів значною мірою перекриваються: біль у животі, непрохідність, лихоманка, анорексія, втрата ваги й анемія. Діарея, ректальні кровотечі, періанальні ураження та позакишкові прояви частіше трапляються при хворобі Крона, тоді як асцит і легеневі симптоми є характернішими для ТБ кишківника. Жоден симптом не є патогномонічним, тому діагноз має ґрунтуватися на комплексній оцінці.
Методи візуалізації, зокрема КТ-ентерографія, допомагають уточнити діагноз. Ознаки на користь ТБ охоплюють некротичні лімфовузли, ураження ілеоцекальної ділянки, асцит, конгломерат мезентеріальних вузлів і потовщення сальника. Для хвороби Крона характернішими є skip-ураження, довгі сегменти запалення, ознака «гребінця», асиметричне потовщення стінки та фіброзно-жирова проліферація. КТ грудної клітки є важливим доповненням у регіонах з високою поширеністю ТБ, оскільки дає змогу виявити легеневі ознаки, що підвищує діагностичну точність.
Ендоскопічні ознаки також мають діагностичну цінність: довгі поздовжні виразки, «бруківка», афтоїдні виразки та залучення ректосигмоїду є характернішими для хвороби Крона, тоді як поперечні виразки та розширений ілеоцекальний клапан – для ТБ. Для підвищення діагностичної точності рекомендується брати щонайменше вісім біопсій з уражених сегментів, особливо з основи виразок.
Гістологічно казеозні гранульоми залишаються золотим стандартом для підтвердження ТБ кишківника, проте їхня чутливість низька. Хвороба Крона зазвичай характеризується дрібними ізольованими гранульомами та локально посиленим колітом. Морфологія гранульом має інтерпретуватися разом з локалізацією ураження та патерном запалення.
Мікробіологічні тести, включно з фарбуванням на кислотостійкі бактерії, тестом GeneXpert і культурою, мають високу специфічність, але низьку чутливість у разі ТБ кишківника. Серологічні тести й імунні біомаркери, як-от IGRA, не забезпечують достатньої точності для диференціації двох станів у ендемічних регіонах. Нові методи, включно з протеомікою та метаболомікою, залишаються експериментальними.
Тактика ведення при діагностичній невизначеності
У регіонах з високою поширеністю ТБ, коли клінічні, ендоскопічні, гістологічні та мікробіологічні дані не дають змоги встановити остаточний діагноз, рекомендовано пробний курс ПТТ. Такий підхід безпечніший, аніж призначення імуносупресії при невиявленому ТБ, що може призвести до дисемінованої інфекції. Стандартний режим включає чотири препарати (ізоніазид, рифампіцин, піразинамід, етамбутол) з дозуванням за масою тіла.
Ефективність оцінюється на 4-8-му тижні, ключовою є контрольна колоноскопія через 8-12 тижнів. Загоєння слизової оболонки та зниження фекального кальпротектину свідчать на користь ТБ кишківника, тоді як збереження активних уражень після виключення мультирезистентності вказує на хворобу Крона. Тимчасове полегшення симптомів можливе при обох станах, але стійке загоєння слизової оболонки характерне лише для ТБ. Продовження терапії понад 12 тижнів без ознак відповіді небажане, щоб уникнути формування стриктур і затримки лікування. Повне загоєння після 6 місяців підтверджує діагноз ТБ кишківника.
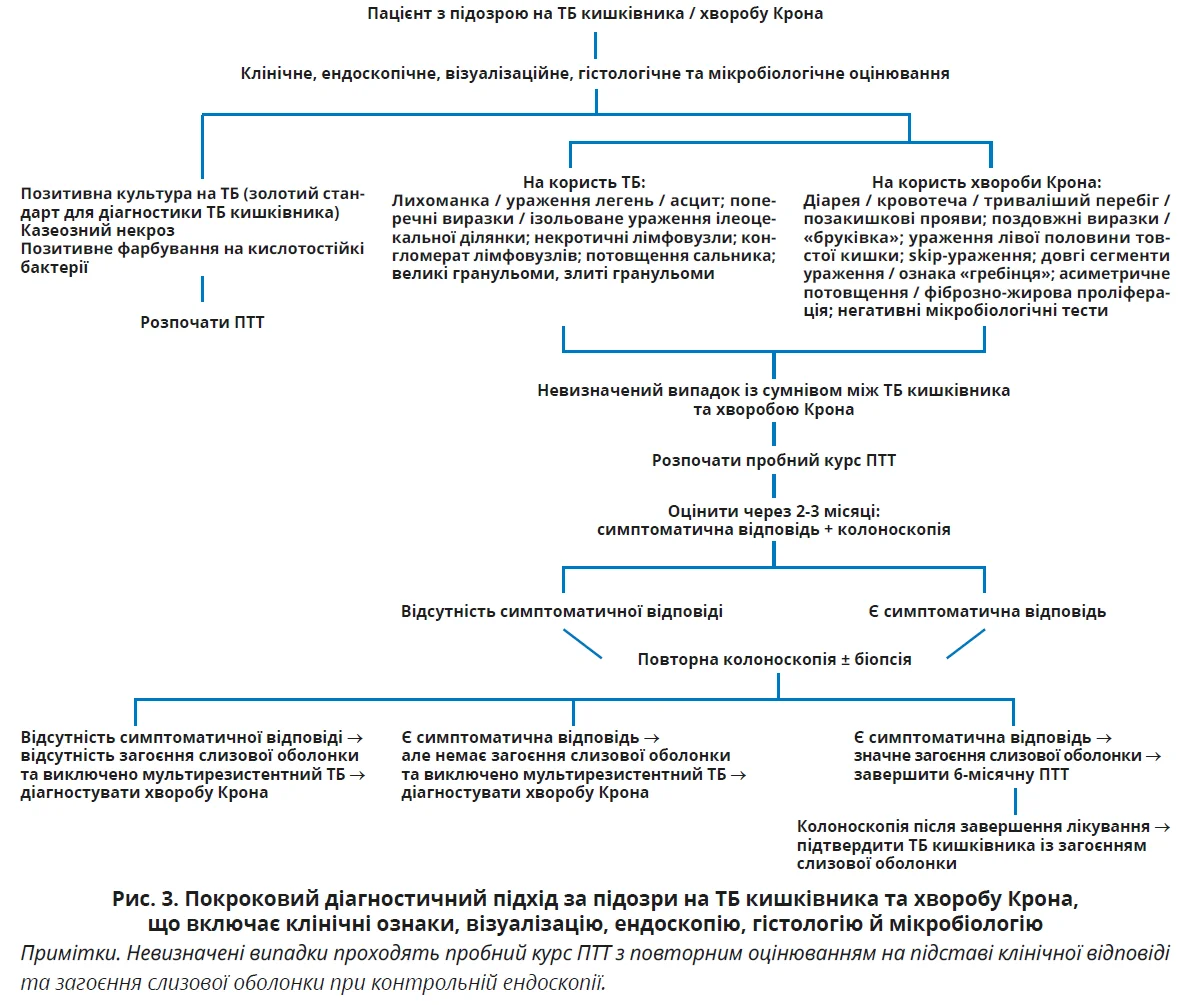
Алгоритм прийняття рішень наведено на рисунку 3, який демонструє покроковий підхід: від комплексного оцінювання до пробного курсу терапії та повторної ендоскопії для підтвердження діагнозу.
Ключові тези
- Складність діагностики. У регіонах з високою поширеністю ТБ відрізнити ТБ кишківника від хвороби Крона складно через перекриття клінічних, ендоскопічних і морфологічних ознак; жоден маркер не є патогномонічним, потрібен комплексний підхід.
- Еволюція підходів. Стратегії змістилися від суворих мікробіологічних критеріїв до пробного курсу ПТТ у невизначених випадках.
- Клінічні орієнтири. За хвороби Крона частіше відзначаються діарея, періанальні ураження, триваліший перебіг і позакишкові прояви; за ТБ кишківника – коротший перебіг, системні симптоми, асцит і легеневі ознаки.
- Візуалізація. На користь ТБ свідчать некротичні лімфовузли, асцит і легеневі зміни; на користь хвороби Крона – skip-ураження, довгі сегменти запалення, асиметричне потовщення стінки та фіброзно-жирова проліферація (ознака «гребінця»).
- Ендоскопічні критерії. Поздовжні й афтоїдні виразки, «бруківка», залучення лівих і правих відділів товстої кишки є типовішими для хвороби Крона; ураження ілеоцекальної ділянки та поперечні виразки – для ТБ кишківника.
- Гістологічні маркери. Великі, злиті, казеозні гранульоми відповідають діагнозу ТБ кишківника; дрібні, ізольовані та неказеозні гранульоми характерні для хвороби Крона.
- Мікробіологічні обмеження. Позитивність фарбування на кислотостійкі бактерії при ТБ кишківника низька через малобактерійний характер процесу.
- Тактика при невизначеності. Доцільно розпочати пробний курс ПTT з повторним клінічним та ендоскопічним оцінюванням на 8-12-му тижні. Клінічна відповідь, зниження фекального кальпротектину та загоєння слизової оболонки підтримують діагноз ТБ. Тимчасове полегшення без загоєння слизової оболонки є типовішим для хвороби Крона. Відсутність відповіді після виключення мультирезистентності є підставою для встановлення діагнозу хвороби Крона та зміни терапії. ПТT не варто продовжувати понад 12 тижнів без ознак відповіді, щоб уникнути формування стриктур і затримки лікування.
- Кінцева верифікація. Повне загоєння слизової оболонки при колоноскопії після завершення 6-місячного курсу ПTT підтверджує ТБ кишківника, хоча фіброзні зміни можуть зберігатися.
- Застосовність. Підхід прийнятний лише в ендемічних регіонах; у неендемічних – рішення має ґрунтуватися на остаточному гістологічному або мікробіологічному підтвердженні, а не на пробних курсах терапії.
Література
Mouli V.Р., Kedia S., Sharma V., еt al. Navigating the differential diagnosis of intestinal tuberculosis and Crohn’s disease. Gastroenterology. 2025; 169 (6): 1139-1146. doi: 10.1053/j.gastro.2025.08.007.