Штучний інтелект у ранній діагностиці неоплазій стравоходу та шлунка: сучасні можливості й виклики
Переклала й адаптувала канд. біол. наук Олександра Демецька
Штучний інтелект (ШІ) відкриває нові перспективи для раннього виявлення неоплазій верхнього відділу шлунково-кишкового тракту, зокрема стравоходу та шлунка. Моделі глибинного навчання на основі згорткових нейронних мереж демонструють високу точність у діагностиці, визначенні меж ураження та прогнозуванні глибини втручання, що сприяє оптимізації лікування. Водночас упровадження ШІ супроводжується низкою викликів, зокрема обмеженою здатністю моделей до узагальнення через вузькі навчальні вибірки, складною морфологією уражень і низькою пояснюваністю алгоритмів [1].
Перспективи розвитку охоплюють інтеграцію мультимодальних даних, автоматизоване керування ендоскопією в реальному часі та персоналізоване оцінювання ризику, що може істотно покращити результати лікування й економічну ефективність.
ШІ у виявленні неоплазії при стравоході Барретта
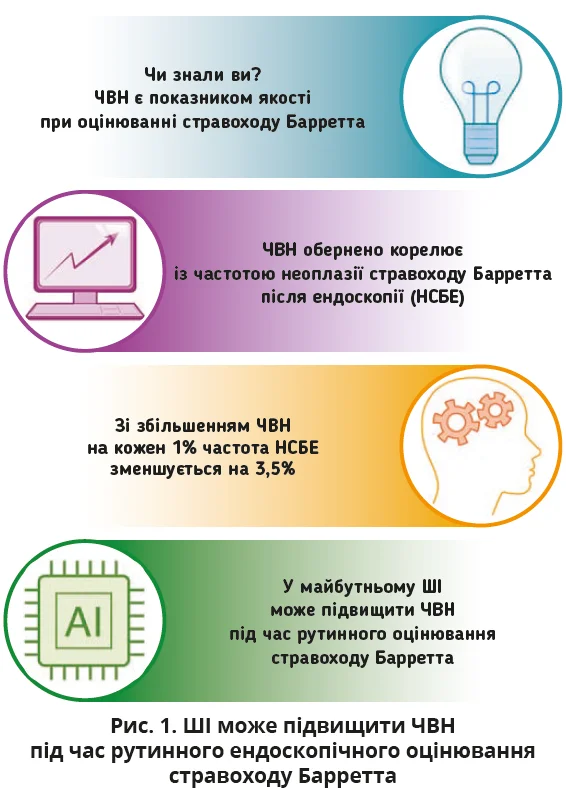
Підтримка ШІ при стравоході Барретта спрямована на виявлення тонких морфологічних змін, пов’язаних з ранньою аденокарциномою стравоходу, які часто залишаються непоміченими ендоскопістами. Натомість підвищення частоти виявлення неоплазії (ЧВН) навіть на 1% може знизити показник пропущених випадків на 3,5% (рис. 1).
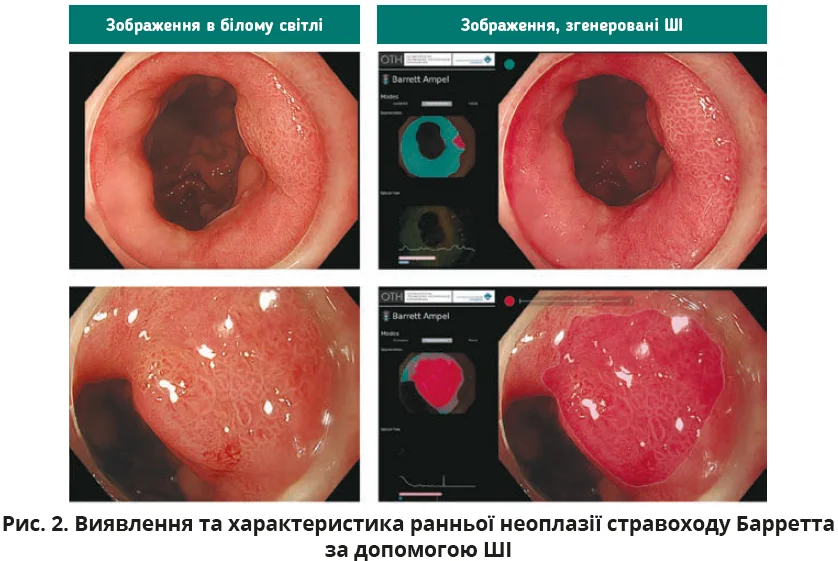
Ранні дослідження зосереджувалися на статичних зображеннях, але сучасні системи працюють з відеопотоками й інтегруються в реальному часі, відображаючи результати у вигляді теплових мап або рамок навколо зон інтересу (ROI), що забезпечує інтуїтивну підтримку під час процедур (рис. 2).
Ліва частина рисунку 2 показує загальний огляд і зображення в білому світлі з близьким фокусом тонкого ураження, розташованого на рівні кардії; права частина демонструє теплові мапи та накладення, згенеровані ШІ, в межах інтерфейсу користувача для прогнозування неоплазії.
ШІ демонструє значну ефективність у клінічній підтримці прийняття рішень: хоча в автономному режимі він перевершує показники ендоскопістів, найбільшу користь приносить саме фахівцям без великого досвіду, підвищуючи ЧВН на 9-12%. Для експертів істотного приросту немає, що підкреслює допоміжну, а не замінювальну роль ШІ.
Алгоритми можуть розрізняти неоплазію, пов’язану зі стравоходом Барретта, і стравохід Барретта без дисплазії, прогнозувати глибину втручання та допомагати у виборі оптимальної тактики резекції. Їхня точність, що сягає приблизно 71%, перевищує показники оптичної оцінки досвідчених ендоскопістів (40-50%).
Морфологічні особливості уражень істотно впливають на якість діагностики. Пласкі ураження (Paris IIa/IIb) найчастіше залишаються непоміченими, тому їх включення до навчальних наборів є критичним. ШІ досягає чутливості на рівні 88-100% для таких уражень, значно підвищуючи ефективність роботи лікарів.
У гістопатології методи глибинного навчання на основі згорткових нейронних мереж і механізмів уваги демонструють точність 0,83-0,89 у класифікації стравоходу Барретта без дисплазії, а також дисплазії й аденокарциноми. Використання методів слабкого навчання дає змогу суттєво зменшити потребу в ручних анотаціях зразків. Завдяки цьому моделі можуть визначати ступінь дисплазії на повних гістологічних зрізах з високою точністю, що допомагає лікарям обирати найвідповіднішу терапевтичну тактику.
ШІ на основі зображень за плоскоклітинного раку стравоходу
Системи ШІ демонструють високу ефективність у виявленні та діагностиці плоскоклітинного раку стравоходу (ПКРС), подекуди перевершуючи досвідчених ендоскопістів. Вони здатні визначати межі пухлини під час ендоскопії в білому світлі й оцінювати глибину втручання за характером внутрішньососочкових капілярних петель, що використовується в японській класифікації уражень стравоходу. Це дає змогу розрізняти внутрішньослизові форми раку та підслизові інвазивні форми, що має ключове значення для вибору методу резекції.
Для підвищення точності моделі навчають на даних, які містять не лише карциноми, а й некарциномні ураження (запальні зміни, ектопічну слизову оболонку), а також ранні форми раку з тонкими морфологічними ознаками, що часто залишаються непоміченими при стандартній ендоскопії. У перспективі системи ШІ можуть стати важливим інструментом для відбору уражень, придатних до ендоскопічної резекції, та для підвищення точності діагностики загалом.
Попри суттєвий прогрес, використання систем ШІ при ранньому раку стравоходу залишається складним. Ураження при стравоході Барретта часто є пласкими, мультифокальними та малопомітними, що ускладнює їх виявлення порівняно з очевиднішими ураженнями товстої кишки. Відсутність єдиного еталонного стандарту (чи вважати основою гістологічне підтвердження, чи консенсус експертів), а також значна міжоператорна варіабельність, особливо для дисплазії низького ступеня, створюють труднощі для навчання алгоритмів.
Більшість систем орієнтовані на виявлення дисплазії високого ступеня, тоді як якісних даних для дисплазії низького ступеня бракує. Навчальні вибірки здебільшого походять зі спеціалізованих центрів, що обмежує можливість узагальнення результатів на ширшу популяцію пацієнтів. Окремою проблемою залишається точне окреслення меж ураження, особливо для пласких неоплазій, що безпосередньо впливає на вибір методу лікування.
Для ПКРС додатковим викликом є інтеграція ШІ в рутинну практику. Проспективні дослідження показують, що точність систем ШІ наразі не перевищує показників досвідчених ендоскопістів. У регіонах з низькою поширеністю цього виду раку розвиток моделей ускладнюється браком достатніх обсягів якісних даних. Для широкого впровадження потрібні великі, різноманітні й добре анотовані набори даних, а також оптимізація алгоритмів для швидкої та надійної роботи в режимі реального часу.
ШІ у виявленні неоплазії шлунка: поточні дані та клінічні показання
ШІ активно застосовується для виявлення передракових і злоякісних уражень шлунка, знижуючи частоту пропусків і допомагаючи як менш досвідченим, так і досвідченим ендоскопістам.
Системи забезпечують автоматичне визначення та класифікацію підозрілих ділянок у режимі реального часу, що підвищує якість огляду.
Особливе значення мають можливості ШІ в діагностиці атрофічного гастриту й кишкової метаплазії – ключових етапів канцерогенезу, пов’язаного з інфекцією Helicobacter pylori. Пацієнтам з поширеними змінами рекомендовано ендоскопічний нагляд, але звичайна ендоскопія має недостатню чутливість і часто пропускає тонкі ураження, особливо у важкодоступних зонах шлунка. Сучасні моделі глибинного навчання й алгоритми на основі згорткових нейронних мереж значно перевищують точність навіть експертів у діагностиці атрофії та метаплазії, швидше аналізують зображення та зменшують кількість пропущених передракових змін. Алгоритми, розроблені для виявлення інфекції H. pylori й атрофічних уражень, демонструють високу точність на реальних клінічних зображеннях, що підтверджує їхній потенціал для покращення скринінгу.
Раннє виявлення раку шлунка є критичним, оскільки на ранній стадії п’ятирічна виживаність перевищує 90%, тоді як за поширених форм є суттєво нижчою. ШІ вже працює точніше, ніж фахівці, які проводять ендоскопічні огляди, зокрема у виявленні раннього раку, оцінюванні глибини ураження й визначенні типу патології. Алгоритми, розроблені на основі глибинного навчання та згорткових нейронних мереж, успішно розрізняють ураження з різним ступенем дисплазії та стадії раку шлунка, забезпечуючи точність, що не поступається експертним оцінкам. Вони також покращують здатність прогнозувати глибину ураження, що має ключове значення для визначення показань до ендоскопічної резекції.
Збільшена ендоскопія та методи покращеної візуалізації значно підвищують ефективність виявлення ранніх форм раку, але потребують високої кваліфікації. Системи ШІ здатні забезпечити точність, порівнянну з такою експертів, і покращити діагностику передракових станів, зменшуючи потребу в надмірній кількості біопсій. Алгоритми можуть окреслювати межі раннього раку шлунка в режимі реального часу та прогнозувати ступінь диференціації пухлини.
Окремим напрямом розвитку є пояснювані моделі ШІ, спрямовані на зменшення ефекту «чорної скриньки». Такі системи надають лікарю прозорі пояснення щодо того, які ознаки вплинули на рішення алгоритму, що підвищує довіру, полегшує клінічне впровадження та робить використання ШІ безпечнішим і обґрунтованішим.
Гістопатологічна діагностика залишається трудомістким процесом, але методи глибинного навчання значно прискорюють його виконання. Використання слабкого та неконтрольованого навчання зменшує потребу в ручному маркуванні зразків, забезпечуючи високу точність класифікації аденокарцином і понад 91% точності при виділенні ділянок пухлини. Клінічно орієнтовані системи досягають майже 100% чутливості та понад 80% специфічності, що підтверджує потенціал ШІ для автоматизації патологічних досліджень.
Виклики та перспективи
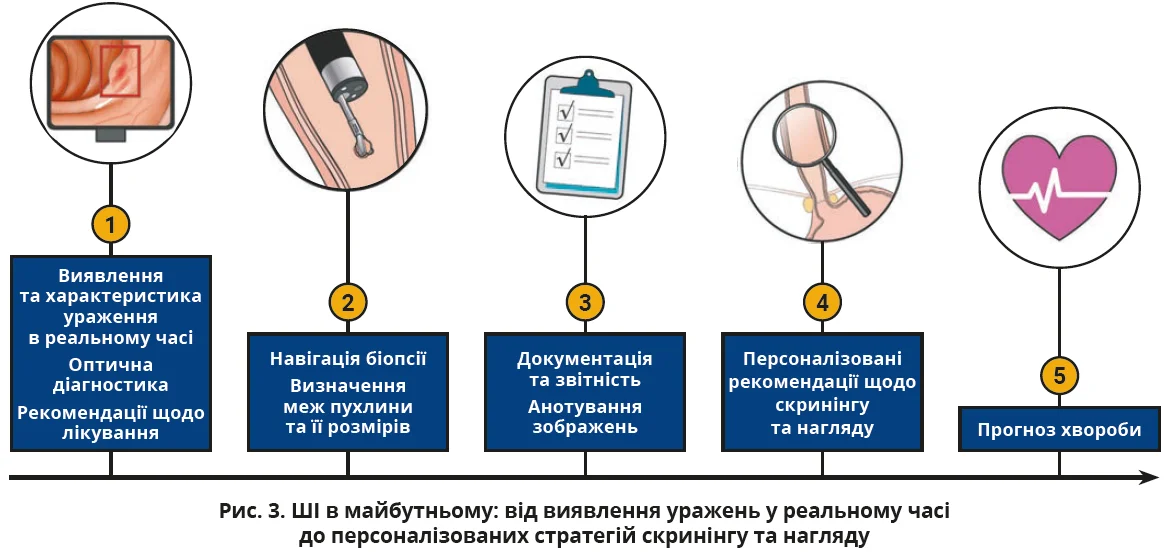
Основні виклики в упровадженні ШІ пов’язані з непрозорістю роботи алгоритмів, браком великих багатоцентрових наборів даних і залежністю від ретельного ручного маркування. Подолати ці обмеження можуть пояснювані моделі, напівконтрольоване навчання й істотне збільшення обсягів зображень, а також зовнішня валідація й оптимізація алгоритмів для роботи в реальному часі. Водночас технології стрімко розвиваються: в клінічній практиці системи ШІ вже застосовують для скринінгу, нагляду та персоналізованого планування лікування, включно з тривимірною реконструкцією уражених ділянок, прогнозуванням ризиків і оптимізацією терапії (рис. 3). У гістопатології моделі, що працюють з мінімальною кількістю ручних анотацій, демонструють потенціал для масштабного скринінгу та значного зменшення навантаження на фахівців.
Зміщення фокусу ШІ від простого інструменту для виявлення та характеристики до універсальнішого рішення може підвищити його прийнятність і застосовність у разі стравоходу Барретта.
ШІ доводить здатність підвищувати точність діагностики, покращувати визначення глибини втручання та підтримувати клінічні рішення в реальному часі, проте залишається низка перешкод, включно зі складною морфологією уражень, обмеженістю різноманітних даних і міжоператорною варіабельністю. Подальший розвиток охоплюватиме мультимодальні системи, здатні аналізувати ендоскопічні зображення, променеві дослідження та повні гістологічні зрізи одночасно, а також використання великих мовних моделей для автоматизації процесів – від виявлення до формування звітів. У перспективі інтеграція ШІ в клінічні протоколи скринінгу й лікування відкриє можливості для персоналізованої медицини, підвищить ефективність терапії та зменшить навантаження на лікарів. Усунення поточних обмежень і широке впровадження пояснюваних рішень здатні суттєво трансформувати ендоскопію верхнього відділу шлунково-кишкового тракту й патологію, покращуючи результати лікування пацієнтів з ранніми неоплазіями.
Література
Ebigbo A., et al. Artificial intelligence applications in image-based diagnosis of early esophageal and gastric neoplasms. Gastroenterology. 2025; 169 (3): 396-415.e2. doi: 10.1053/j.gastro.2025.01.253.