Практичні настанови AASLD із клінічної оцінки та лікування неалкогольної жирової хвороби печінки
Автор: Ігор Миколайович СКРИПНИК, доктор медичних наук, професор, президент ГО «Українська гастроентерологічна асоціація», проректор із науково-педагогічної роботи та післядипломної освіти, професор кафедри внутрішньої медицини № 1 Полтавського державного медичного університету
 Протягом останніх років вивчення неалкогольної жирової хвороби печінки (НАЖХП) значно інтенсифікувалося: з 2018 р. опубліковано понад 1400 публікацій, у тому числі попередні рекомендації Американської асоціації з вивчення захворювань печінки (AASLD) [1]. Нові практичні настанови AASLD відображають значні досягнення в цій галузі, що стосуються будь-якого лікаря, котрий доглядає за пацієнтами з НАЖХП, і підкреслює досягнення в галузі неінвазивної стратифікації ризику та терапії.
Протягом останніх років вивчення неалкогольної жирової хвороби печінки (НАЖХП) значно інтенсифікувалося: з 2018 р. опубліковано понад 1400 публікацій, у тому числі попередні рекомендації Американської асоціації з вивчення захворювань печінки (AASLD) [1]. Нові практичні настанови AASLD відображають значні досягнення в цій галузі, що стосуються будь-якого лікаря, котрий доглядає за пацієнтами з НАЖХП, і підкреслює досягнення в галузі неінвазивної стратифікації ризику та терапії.
Визначення
НАЖХП являє собою загальний термін, що об’єднує всі стадії захворювання та стосується популяції, в якій ≥5% гепатоцитів мають макровезикулярний стеатоз за відсутності легко ідентифікованої альтернативної причини стеатозу (ліки, голодування, моногенні розлади) в осіб, які вживають мало / зовсім не вживають алкоголь (визначається як <20 г/добу для жінок і <30 г/добу для чоловіків). Спектр захворювання включає неалкогольний стеатоз, який характеризується макровезикулярним стеатозом печінки, котрий може супроводжуватися легким запаленням; неалкогольний стеатогепатит (НАСГ), який додатково визначається наявністю запалення та пошкодженням клітин (балонна дистрофія) з/без фіброзу; та, нарешті, цироз печінки (ЦП), який характеризується появою фіброзних смуг/перегородок, що призводять до утворення циротичних вузликів, за яких попередні ознаки НАСГ не можуть бути повністю визначені при біопсії печінки.
Оновлені дані з епідеміології та природного перебігу
Поширеність НАЖХП та НАСГ зростає в усьому світі одночасно зі збільшенням поширеності ожиріння, супутніх метаболічних захворювань – МЗ (інсулінорезистентності (ІР), дисліпідемії, центрального ожиріння й артеріальної гіпертензії) [5, 6]. Поширеність НАЖХП у дорослих у загальній популяції оцінюється на рівні 25-30% [7-9] і варіює залежно від клінічних умов, расової/етнічної приналежності та географічного регіону, але ще залишається недостатньо вивченою [10-14].
Зв’язок між стадією захворювання та несприятливими наслідками
Найчастішими причинами смерті хворих на НАЖХП є серцево-судинні захворювання (ССЗ) та позапечінкові злоякісні новоутворення, за якими слідують захворювання печінки. Розмір фіброзу печінки, виявлений гістологічно в пацієнтів із НАЖХП, асоційований із розвитком гепатологічних наслідків і смерті [24, 26, 36, 37]. Мостоподібний фіброз і ЦП пов’язані з експоненційним зростанням ризику захворюваності та смертності, асоційованої із захворюваннями печінки, порівняно з ранніми стадіями фіброзу [23, 24, 35]. У проспективному дослідженні (n=1773) продемонстровано, що смертність
від усіх причин у пацієнтів із фіброзом F0-2 становить 0,32 на 100 людино-років порівняно з 0,89 на 100 людино-років у осіб із мостоподібним фіброзом та 1,76 на 100 людино-років у пацієнтів із ЦП. Після поправки на численні фактори встановлено зв’язок між печінковою декомпенсацією та смертністю від усіх причин (відношення шансів 6,8; 95% довірчий інтервал 2,2-21,3) [35]. За даними клінічних досліджень, регресія ЦП асоціюється з 6-кратним зменшенням кількості подій, зумовлених станом печінки [38].
Ключові моменти
- Пацієнти з НАСГ та фіброзом F2-4 мають вищий ризик розвитку асоційованих із печінкою подій і смертності та належать до групи ризику НАСГ.
- Швидкість прогресування фіброзу й печінкової декомпенсації значно варіює залежно від вихідного рівня тяжкості захворювання, генетичних/індивідуальних чинників, впливу довкілля та супутніх захворювань.
- ССЗ і позапечінкові злоякісні новоутворення є найчастішими причинами смертності хворих на НАЖХП без прогресивного фіброзу; смерть від захворювань печінки домінує серед пацієнтів
із прогресивним фіброзом.
Молекулярний і клітинний патогенез
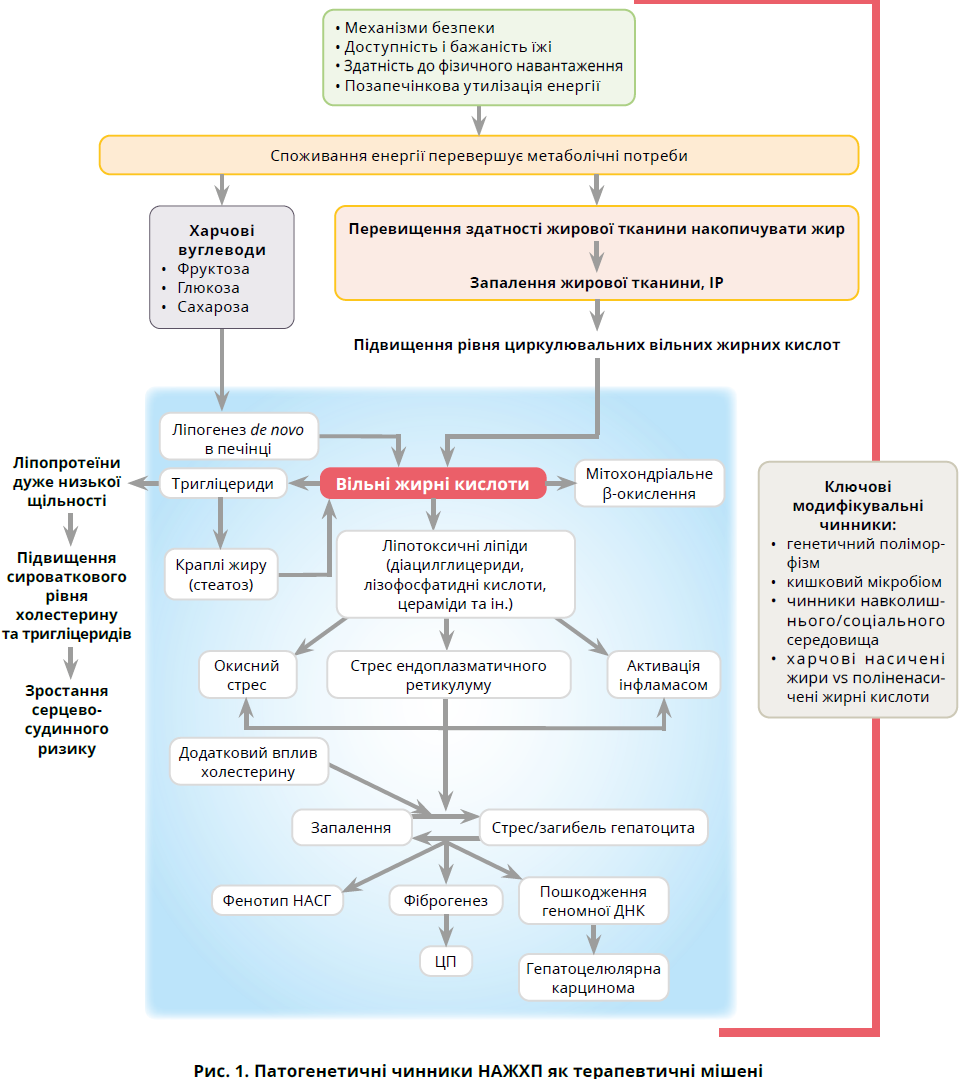
Наявність і тяжкість НАЖХП, НАСГ значною мірою визначаються чинниками, які регулюють надходження та розподіл жирних кислот, діацилгліцеринів, церамідів, холестерину, фосфоліпідів та інших внутрішньопечінкових ліпідів. Надлишок енергії й обмежене розростання жирової тканини спричиняють розвиток ІР і МЗ [39]. Коли споживання енергії перевищує метаболічні потреби та здатність до утилізації, вуглеводи у вигляді харчових цукрів (фруктоза, сахароза, глюкоза) спричиняють утворення й накопичення внутрішньопечінкового жиру внаслідок ліпогенезу de novo [40, 41]. Крім того, тип споживаного жиру відіграє певну роль у розвитку НАСГ: вищий ризик спостерігають у разі споживання насичених і ненасичених жирів (рис. 1) [44-46].
На рисунку 1 наведено огляд основних механізмів, що визначають фенотип НАСГ та його наслідки; велика кількість із них може бути використана з терапевтичною метою. Первинним чинником ризику НАСГ є надходження великої кількості жиру в адипоцити, яке перевищує їхню здатність накопичувати тригліцериди, не спричиняючи клітинного стресу; це призводить до активації запальних шляхів і провокує виникнення ІР. Розуміння основних рушійних сил НАСГ полегшує розроблення раціональної терапії для пацієнтів із НАСГ. Специфічні втручання, котрі можуть запобігти НАСГ / нівелювати його, включають ті, що модулюють споживання їжі (розмір порцій, баріатричні операції, регулятори ситості), збільшують утилізацію енергії (фізичні вправи, термогенез), покращують чутливість адипоцитів до інсуліну (ліганди рецепторів, що активуються проліфераторами пероксисом – PPAR-γ), погіршують ліпогенез de novo (інгібітори карбоксилази ацетилкоензиму А та синтази жирних кислот), посилюють окислювальний метаболізм у печінці (ліганди PPAR-α та β-агоністи рецепторів тиреоїдних гормонів), а також послаблюють запалення, загибель клітин і фіброгенез.
До терапевтичних засобів, здатних впливати на численні метаболічні шляхи в організмі з потенційним позитивним впливом на печінку, відносять пептидні аналоги гормонів (аналоги фактора росту фібробластів-19, -21, глюкагоноподібного пептиду-1, шлункового інгібувального пептиду, глюкагон) і ліганди ядерних рецепторів, які впливають на PPAR-α, PPAR-δ, PPAR-γ, β-рецептор тиреоїдного гормону та фарнезоїдний X-рецептор.
Ключові моменти
- Фундаментальні ланки патогенезу НАСГ включають дисбаланс між доставкою поживних речовин до печінки та їх утилізацією в поєднанні з дисфункцією жирової тканини. Міжіндивідуальні генетичні/дієтичні/поведінкові/екологічні відмінності впливають на перебіг захворювання.
- Системне запалення, особливо спричинене дисфункцією жирової тканини, призводить до прогресування захворювання.
- ІР спричиняє розвиток НАЖХП та прогресування захворювання.
Коморбідні стани, асоційовані з НАЖХП
НАЖХП тісно пов’язана з розвитком метаболічних порушень і часто передує розвитку МЗ (ІР, дисліпідемія, центральне ожиріння, артеріальна гіпертензія) [47, 61, 75-77]. Наявність декількох метаболічних порушень підвищує ризик гістологічного прогресування НАСГ та смертності від усіх причин [8, 47, 78-81]. Зв’язок між НАЖХП та супутніми МЗ може також відображати двоспрямовану взаємодію між печінкою й іншими ендокринними органами (підшлунковою залозою, жировою тканиною, м’язами) шляхом секреції гепатокінів, які регулюють метаболізм жирних кислот, дію інсуліну, метаболізм глюкози [82-88], адипокінів і міокінів [39, 89, 90].
Положення настанови
1. Статини безпечні та рекомендовані для зниження серцево-судинного ризику в пацієнтів із НАЖХП (увесь спектр захворювання), включаючи компенсований ЦП.
2. Існують обмежені дані щодо безпеки й ефективності статинів у пацієнтів із декомпенсованим ЦП, хоча можна розглядати доцільність застосування статинів під ретельним моніторингом у пацієнтів
із високим ризиком ССЗ.
3. Гіпертригліцеридемію можна контролювати за допомогою зміни способу життя та доповнення раціону харчування ω3-жирними кислотами, ікосапент етилом або фібратами.
4. Пацієнти з цукровим діабетом (ЦД) мають вищий ризик розвитку НАСГ, прогресивного фіброзу та мають проходити скринінг на наявність прогресивного фіброзу.
5. Пацієнти з НАЖХП мають проходити скринінг на наявність ЦД 2 типу.
Ключові моменти
- Поширеність і захворюваність на хронічну хворобу нирок вища серед пацієнтів із НАСГ та прогресивним фіброзом.
- Смерть від позапечінкових злоякісних новоутворень є поширеною причиною смерті пацієнтів із НАЖХП; отже, дотримання вікових норм онкоскринінгу має потенціал у покращенні виживання.
Первинне обстеження пацієнтів із НАЖХП
Пацієнти з НАЖХП найчастіше звертаються після випадково виявленого стеатозу печінки під час проведення візуалізаційного обстеження або визначення підвищеного вмісту печінкових проб. Важливо зазначити, що нормативні значення, котрі наводяться переважною більшістю лабораторій, є вищими, ніж ті, які варто дійсно вважати нормальними при НАЖХП; наприклад, справжній нормальний уміст аланінамінотрансферази (АЛТ) становить 29-33 Од/л у чоловіків і 19-25 Од/л у жінок [177]. Початкове обстеження таких пацієнтів має включати скринінг супутніх МЗ, оцінку вживання алкоголю та виключення інших причин захворювання печінки, а також фізикальне обстеження для виявлення ознак ІР і прогресивного захворювання печінки (табл.).
Роль уживання алкоголю
Уживання алкоголю може бути важливим чинником, який спричиняє прогресування жирової дистрофії печінки, його слід кількісно оцінювати в усіх пацієнтів [211]. Уживання алкоголю можна класифікувати як легке (до 20 г (жінки) та 30 г (чоловіки) на добу), помірне (21-39 г (жінки) та 31-59 г (чоловіки) на добу) або тяжке (≥40 г (жінки) та ≥60 г (чоловіки) на добу). Помірне вживання алкоголю збільшує ймовірність прогресивного фіброзу [212], особливо в пацієнтів з ожирінням або ЦД 2 типу, що вказує на потенційний синергічний вплив ІР й алкоголю на прогресування захворювання печінки. Ожиріння та вживання алкоголю синергічно підвищують ризик пошкодження печінки, ЦП, гепатоцелюлярної карциноми та смерті від захворювань печінки [213-215]. Зловживання алкоголем прискорює пошкодження печінки та прогресування фіброзу; його слід уникати пацієнтам із НАЖХП/НАСГ [211].
Положення настанови
6. У пацієнтів із НАЖХП алкоголь може прискорювати прогресування захворювання печінки; його вживання слід регулярно оцінювати.
7. Пацієнти з клінічно значущим фіброзом печінки (≥F2) мають утримуватися від уживання
алкоголю.
Ключові моменти
• Абстиненція, особливо для пацієнтів із помірним/значним уживанням алкоголю, може знизити ризик прогресування фіброзу, розвитку печінкових і позапечінкових злоякісних новоутворень
у пацієнтів із НАЖХП.
Супутні ендокринні захворювання
На додаток до тісного зв’язку з ожирінням та іншими метаболічними чинниками ризику високу поширеність НАЖХП зафіксовано в пацієнтів із гіпотиреозом, гіпогонадизмом, дефіцитом гормону росту, синдромом полікістозних яєчників.
Положення настанови
8. НАЖХП частіше трапляється в чоловіків із дефіцитом андрогенів, але сучасні дані не підтримують доцільності рутинного вимірювання рівня тестостерону. За наявності гіпогонадизму, на що вказують клінічні ознаки або симптоми, захворювання слід лікувати відповідно.
Ключові моменти
• Хоча дефіцит гормону росту та пангіпопітуїтаризм можуть бути пов’язані зі стеатозом печінки, їхня незалежна роль у розвитку та прогресуванні стеатогепатиту/фіброзу залишається невстановленою.
• Надлишок андрогенів здатний погіршити ІР у жінок із синдромом полікістозних яєчників, що разом з ожирінням і ЦД 2 типу може спричиняти розвиток НАЖХП і потенційно більш прогресивний перебіг захворювання в цій популяції.
Які пацієнти мають бути обстежені на наявність клінічно значущого фіброзу?
Рекомендується проводити цілеспрямований скринінг популяцій із підвищеним ризиком розвитку прогресивного захворювання печінки для виявлення та лікування осіб із клінічно вираженим фіброзом (≥F2) [36, 172, 280]. Скринінг у групах високого ризику, а саме в пацієнтів із ЦД 2 типу [112, 113, 116, 281-285], ожирінням і метаболічними ускладненнями [286-292], обтяженим сімейним анамнезом щодо ЦП [293, 294] або в тих, які зловживають алкоголем [211, 295-297], допоможе виявити осіб із безсимптомним, але клінічно значущим фіброзом. Раннє виявлення пацієнтів із груп ризику дає змогу проводити втручання, що здатні запобігти розвитку гепатологічних ускладнень [298]. Ретельна оцінка сімейного анамнезу важлива, оскільки родичі першого ступеня спорідненості пробандів із НАСГ-асоційованим ЦП мають у 12 разів вищий ризик прогресивного фіброзу [293].
Пацієнти з підозрою на НАЖХП через наявність метаболічних чинників ризику або випадково виявлені під час візуалізаційних методів досліджень за відсутності інших причин стеатозу печінки (хвороба Вільсона, целіакія, вірусний гепатит С, зловживання алкоголем) мають пройти первинну оцінку ризику (рис. 2).
Положення настанови
9. Загальнопопуляційний скринінг НАЖХП не рекомендується.
10. Усі пацієнти зі стеатозом печінки або клінічною підозрою на НАЖХП на підставі наявності ожиріння та метаболічних чинників ризику мають пройти первинну оцінку ризику за допомогою індексу фіброзу-4 (FIB-4).
11. Хворі з високим ризиком, тобто ті, які мають ЦД 2 типу, ускладнений перебіг ожиріння, обтяжений сімейний анамнез щодо ЦП, особи з більш ніж помірним уживанням алкоголю, мають бути обстежені на наявність прогресивного фіброзу.
12. У пацієнтів із пре-ЦД, ЦД 2 типу та ≥2 метаболічними чинниками ризику (або ознаками печінкового стеатозу за даними візуалізаційних методів дослідження) первинну оцінку ризику за допомогою FIB-4 потрібно повторювати що 1-2 роки.
13. Пацієнти з НАСГ-асоційованим ЦП мають найвищий ризик печінкових ускладнень і потребують рутинного спостереження щодо гепатоцелюлярної карциноми, варикозного розширення вен стравоходу та моніторингу декомпенсації.
14. Пацієнтів із підозрою на прогресивний НАСГ або дискордантними результатами неінвазивних тестів варто скеровувати до спеціаліста задля обстеження, лікування та/або поглибленого діагностичного обстеження.
15. Рівні амінотрансфераз часто є нормальними в пацієнтів із НАСГ-асоційованим прогресивним захворюванням печінки; вони не мають використовуватися ізольовано для виключення наявності НАСГ за клінічно значущого фіброзу.
16. Родичів першого ступеня спорідненості пацієнтів із НАСГ-асоційованим ЦП варто проконсультувати щодо їхнього підвищеного індивідуального ризику та запропонувати скринінг прогресивного фіброзу печінки.
Ключові моменти
• Хворі на НАСГ із групи високого ризику (НАСГ із фіброзом принаймні F2) мають підвищений ризик розвитку ЦП та гепатологічних ускладнень.
Пацієнти зі стеатозом, виявленим під час візуалізаційних досліджень, або з клінічною підозрою на НАЖХП (метаболічні чинники ризику або незрозуміле підвищення рівня печінкових проб) мають пройти подальше обстеження. В умовах низької поширеності прогресивного фіброзу, наприклад в умовах первинної медичної допомоги, акцент робиться на виключення прогресивного фіброзу за допомогою тесту з високим негативним прогностичним значенням. Якщо FIB-4 становить <1,3, то пацієнти можуть спостерігатися в установах первинної медичної допомоги та періодично проходити переоцінку.
Пацієнти без предіабету / ЦД 2 типу та з 1-2 метаболічними чинниками ризику можуть підлягати повторній оцінці що 2-3 роки. Пацієнти з предіабетом / ЦД 2 типу та ≥2 метаболічними чинниками ризику мають вищий ризик прогресування захворювання та потребують частішого моніторингу FIB-4 (що 1-2 роки).
У пацієнтів >65 років слід використовувати граничне значення FIB-4 >2,0. FIB-4 має низьку точність у пацієнтів віком <35 років; отже, в пацієнтів <35 років із підвищеними метаболічним ризиком або показниками печінкових проб слід розглянути можливість проведення вторинної оцінки. FIB-4 не слід використовувати в пацієнтів, які гостро захворіли. В осіб із FIB-4 ≥1,3 варто провести вторинну оцінку (переважно спочатку вібраційну еластографію (ВЕ) чи спочатку виконати тест на значний фіброз печінки – ELF-тест) або скерувати пацієнта для подальшої стратифікації ризику (якщо він спостерігається не в гастроентеролога / гепатологічному закладі). Пряме скерування до гастроентеролога/гепатолога слід розглядати в пацієнтів зі стійкими (>6 місяців) підвищеними рівнями амінотрансфераз із метою виключення інших причин захворювання печінки або коли FIB-4 >2,67 через підвищений ризик клінічно значущого фіброзу.
Біомаркери / неінвазивні тести для діагностики й оцінки НАЖХП
Незважаючи на те що біопсія печінки залишається еталонним стандартом визначення стадії та тяжкості НАСГ, вона має важливі обмеження, пов’язані з ризиком, вартістю та використанням ресурсів. Тому біопсія печінки широко не застосовується для визначення стадії/тяжкості НАСГ у клінічній практиці; її слід зарезервувати для тяжких клінічних випадків (рис. 2) [317]. Неінвазивні біомаркери стають цінними інструментами для прогнозування розвитку несприятливих гепатологічних наслідків. Валідація неінвазивних біомаркерів відповідно до рекомендацій Управління з контролю продуктів харчування та лікарських засобів США (FDA) [318] полегшить діагностику пацієнтів із клінічно значущими захворюваннями й оцінку їхньої відповіді на лікування без проведення біопсії печінки.
Положення настанови
17. Незважаючи на те що стандартне ультразвукове дослідження здатне виявити стеатоз печінки, його не рекомендують як спосіб ідентифікації печінкового стеатозу через низьку чутливість до всього спектра НАЖХП.
18. Контрольований параметр згасання (САР) ультразвукового сигналу – метод дослідження, що може бути виконаний біля ліжка хворого та використовуватися для ідентифікації стеатозу.
МРТ-визначення протонної щільності жирової тканини може додатково використовуватися для кількісної оцінки стеатозу.
19. Якщо FIB-4 ≥1,3, то для виключення прогресивного фіброзу можуть бути використані ВЕ, МРТ-еластографія або ELF-тест.
Ключові моменти
• Високі показники жорсткості печінки, FIB-4 та ELF-тест можуть прогнозувати високий ризик печінкової декомпенсації та смертності.
Лікування
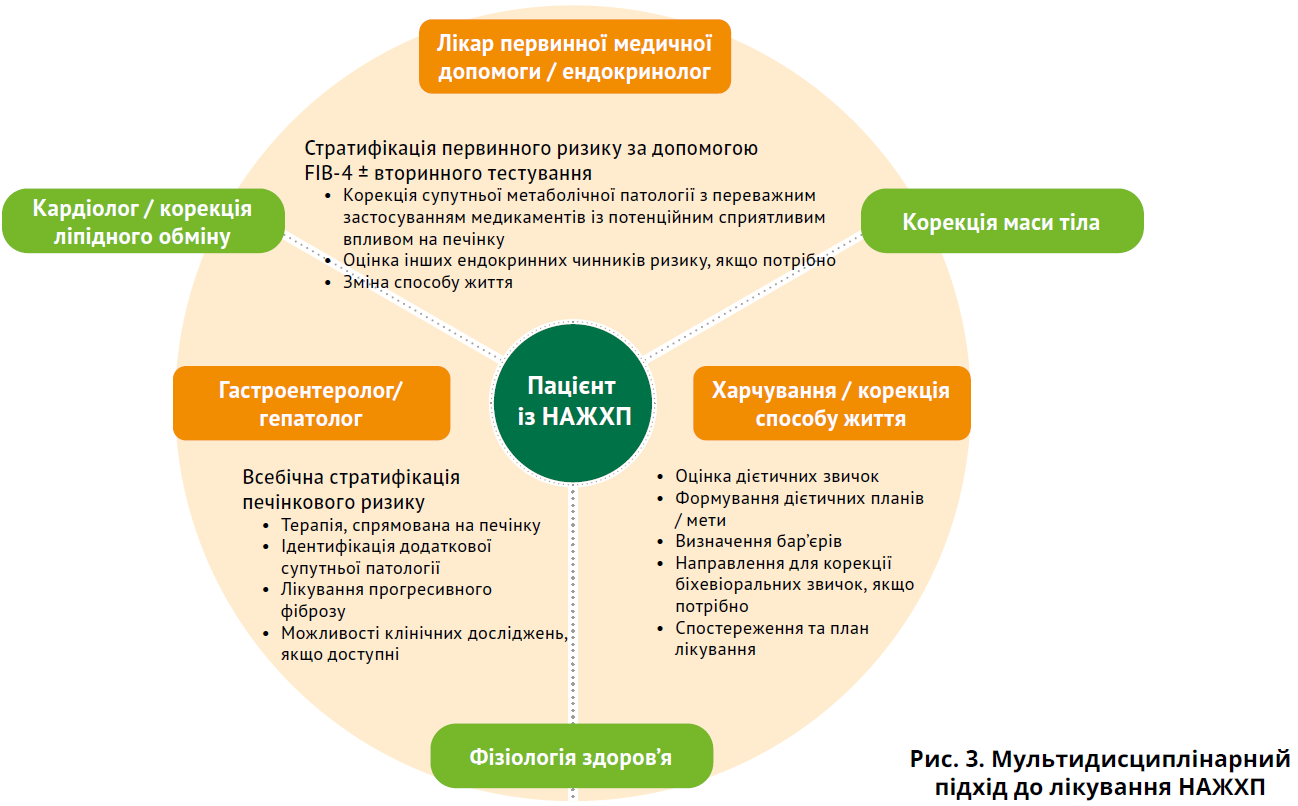
Здорова дієта та регулярні фізичні вправи є основою лікування переважної більшості хворих на НАЖХП [365]. Навіть якщо втрата ваги не є необхідною, покращення раціону та збільшення фізичної активності сприяють покращенню серцево-судинного здоров’я на додаток до поліпшення стану печінки / супутніх МЗ. Для оптимізації перебігу НАЖХП-асоційованих супутніх МЗ слід використовувати мультидисциплінарний підхід: команда багатопрофільних клініцистів забезпечує досягнення найкращих шансів на успіх у зниженні захворюваності та смертності від хвороб печінки, ССЗ у пацієнтів із НАЖХП (рис. 3) [173, 366]. Деякі препарати, схвалені для лікування асоційованих супутніх захворювань (ЦД 2 типу, ожиріння), вивчали в контексті НАЖХП; встановлено, що вони можуть знижувати рівні печінкових ферментів, зменшувати стеатоз або покращувати гістологію печінки. Тому при лікуванні супутніх захворювань слід розглянути доцільність застосування препаратів із можливим позитивним впливом на печінку [2].
Оптимальний догляд за хворими на НАЖХП потребує мультидисциплінарного підходу. Більшість пацієнтів перебувають у закладах первинної допомоги / ендокринологічних відділеннях, де слід оптимізувати лікування супутніх захворювань із відданням переваги терапії ЦД 2 типу, артеріальної гіпертензії або ожиріння, що, ймовірно, також чинить сприятливий вплив на перебіг НАЖХП. У цих умовах слід ідентифікувати пацієнтів із групи ризику та провести початкову стратифікацію ризику (FIB-4 ± ВЕ або ELF-тест). Роль гастроентеролога/гепатолога передбачає комплекснішу стратифікацію ризику ураження печінки, виключення інших захворювань печінки та зосередження на терапії, спрямованій на підтримання печінки. Тісна комунікація між гастроентерологами/гепатологами та лікарями первинної медичної допомоги / ендокринологами сприяє мультидисциплінарній корекції супутніх МЗ, а також визначенню пріоритетності лікарських засобів/утручань, які можуть бути корисними для печінки.
Усі пацієнти мають пройти оцінку дієти/харчування та скласти план регулярного спостереження незалежно від візитів до гастроентеролога/гепатолога. Потребу в більш спеціалізованому лікуванні ожиріння, включаючи баріатричну хірургію, психологічну підтримку та додаткову кардіологічну/ліпідну підтримку, слід оцінювати індивідуально (пунктирні стрілки).
Положення настанови
20. Пацієнтам із НАЖХП, які мають надлишкову масу тіла чи ожиріння, варто призначити дієту, котра сприяє виникненню калорійного дефіциту. Якщо це можливо, слід застосовувати дієти з обмеженим умістом вуглеводів і насичених жирів і збагачені клітковиною, ненасиченими жирами (середземноморська дієта); потрібно заохочувати пацієнтів слідувати ним завдяки додатковим перевагам для серцево-судинної системи.
21. Хворих на НАЖХП слід наполегливо заохочувати підвищувати рівень своєї активності, наскільки
це можливо. Індивідуальні рекомендовані фізичні вправи здатні підвищити стійкість і мають переваги незалежно від втрати маси тіла.
22. Баріатричну хірургію слід розглядати як спосіб лікування для пацієнтів, які відповідають критеріям метаболічного оперативного втручання з метою зниження маси тіла, оскільки воно ефективно усуває НАЖХП/НАСГ у більшості пацієнтів без ЦП та знижує смертність від ССЗ і злоякісних новоутворень.
23. Натепер не існує ліків для лікування НАЖХП, схвалених FDA, проте препарати, схвалені для лікування супутніх захворювань із потенційною користю при НАЖХП, можуть розглядатися у відповідних клінічних умовах.
24. Семаглютид може призначатися згідно з його схваленими показаннями (ЦД 2 типу / ожиріння)
в пацієнтів із НАСГ, оскільки він надає серцево-судинні переваги та поліпшує перебіг НАСГ.
25. Піоглітазон покращує НАСГ і може призначатися хворим на НАСГ та ЦД 2 типу.
26. Вітамін Е може призначатися окремим особам, оскільки він покращує НАСГ у деяких пацієнтів
без ЦД 2 типу.
27. Наявні дані щодо семаглютиду, піоглітазону, вітаміну Е не демонструють їхньої протифіброзної
активності, жоден із них не був ретельно вивчений у пацієнтів із ЦП.
28. Метформін, урсодезоксихолева кислота, дипептидилпептидаза-4, статини та силімарин добре вивчені при НАСГ і не мають використовуватися для лікування НАСГ, оскільки не забезпечують досягнення значущих гістологічних переваг.
29. Зменшення рівня АЛТ або зниження вмісту жиру в печінці, підтверджене даними візуалізаційних досліджень, у відповідь на лікування можна використовувати як сурогатний маркер зниження гістологічної активності захворювання.
Ключові моменти
- Втрата маси тіла зменшує стеатоз печінки, НАСГ, фіброз печінки дозозалежно.
- Необхідна підтримка для лікування коморбідних захворювань і адаптації до поведінки, безпечної для печінки, найкраще досягається за допомогою мультидисциплінарного підходу.
- Споживання кави (з кофеїном чи без) щонайменше 3 чашки на добу асоціюється з меншим прогресуванням патології печінки.
- Зниження вмісту АЛТ на ≥17 Од/л асоціюється з гістологічним покращенням; але порогові значення можуть бути різними за різних типів гістологічної відповіді (нівелювання НАСГ або покращення фіброзу) та залежати від механізму дії.
Коротка довідка від редакції
- Наведені рекомендації AASLD були опубліковані раніше за проведення конференції EASL-2023, у ході якої прийнято рішення щодо модифікації дефініції НАЖХП та застосування терміна «метаболічно-асоційована хвороба печінки».
- При розрахунку FIB-4 оцінюються чотири показники: вік (роки), рівні АЛТ, АСТ і тромбоцитів.
Література
Rinella M., et al. AASLD Practice Guidance on the clinical assessment and management of nonalcoholic fatty liver disease. Hepatology. 2023; 77 (5): 1797-1835. doi: 10.1097/HEP.0000000000000323.
Освітньо-практичний журнал Gastro Practice №1 2023р.