Оптимальне ведення ерозивного езофагіту: заснований на доказах прагматичний підхід
Переклала й адаптувала канд. мед. наук Світлана Опімах
Гастроезофагеальна рефлюксна хвороба (ГЕРХ) є поширеною патологією шлунково-кишкового тракту. Близько 20% пацієнтів з ГЕРХ мають серйозні стравохідні ускладнення, як-от ерозивний езофагіт (ЕЕ), стравохід Барретта, стриктура чи аденокарцинома стравоходу. ЕЕ є найпоширенішим ускладненням ГЕРХ, що характеризується надмірним рефлюксом, некрозом слизової оболонки, ерозіями, виразками та в тяжких випадках крововиливами.
ПАТОГЕНЕЗ
ЕЕ спричиняється пошкодженням стравоходу шлунковою кислотою й пепсином при pH <4, а в деяких випадках – дуоденогастральним рефлюксом жовчі та ліків. Патогенез ЕЕ можуть зумовлювати дефект нижнього стравохідного сфінктера (НСС), аномальний стравохідний кліренс через наявність кили стравохідного отвору діафрагми, знижена амплітуда перистальтичних скорочень, підвищена частота непропульсивних скорочень, зниження вироблення слини та вмісту бікарбонату в ній, зниження опору слизової оболонки стравоходу й уповільнене спорожнення шлунка.
ЕЕ проявляється видимими ендоскопічними знахідками (аномальної форми або лінійними ураженнями в дистальному відділі стравоходу) та гістологічними ознаками пошкодження стравоходу.
КЛІНІЧНА КАРТИНА
Крім печії та кислотної регургітації, ЕЕ може проявлятися відчуттям грудки в шлунку, виділенням надмірної кількості слини, відрижкою й нудотою. Тривожні симптоми, які можуть свідчити про серйозніше захворювання, включають появу ГЕРХ уперше у віці понад 60 років, дисфагію, болісне ковтання, блювання, анемію, незрозумілу втрату ваги та шлунково-кишкову кровотечу (ШКК).
Ці симптоми можуть бути пов’язані з іншими стравохідними ускладненнями ГЕРХ, як-от стравохід Барретта, стриктура чи аденокарцинома.
ДІАГНОСТИКА
Існує кілька діагностичних тестів для обстеження пацієнтів з ЕЕ. Езофагогастродуоденоскопія (ЕГДС) необхідна для встановлення діагнозу ЕЕ.
ЕГДС особливо важлива для пацієнтів з рефрактерним перебігом або атиповими симптомами, як-от біль у грудях, проблеми з ЛОР-органами або легенями, тривожними симптомами (наприклад, дисфагія, болісне ковтання, безпричинна втрата ваги, ШКК, анемія) та перед проведенням хірургічного втручання (табл. 1).
До того ж ЕГДС дає змогу провести біопсію для оцінювання еозинофільного езофагіту, стравохідної метаплазії та дисплазії, а також лікування таких ускладнень ЕЕ, як ШКК чи стриктура стравоходу.
Для ендоскопічного оцінювання тяжкості ЕЕ найширше використовують Лос-Анджелеську класифікацію. Вона поділяє тяжкість ЕЕ на чотири ступені. Езофагіт ступеня А може бути настільки легким, що потребує підтвердження за допомогою 96-годинного pH-моніторингу або 24-годинного імпедансного pH-моніторингу зі скасуванням кислотосупресивних препаратів. Для пацієнтів з ЕЕ зі ступенями B, C та D pH-тестування зі скасуванням кислотосупресивних препаратів зазвичай не потрібне. Однак у пацієнтів з рефрактерним ЕЕ зі ступенями B, C та D рекомендується 24-годинне імпедансне pH-тестування з прийманням кислотосупресивних препаратів для оцінювання наявності кислотного та слабкого кислотного рефлюксу.
У більшості пацієнтів з ЕЕ ступеня B, C або D біопсія стравоходу не рекомендується.
Існує кілька методів оцінювання ступеня кислотного та некислотного рефлюксу, а також моторики стравоходу. Ці методи переважно використовуються для пацієнтів з рефрактерним перебігом ЕЕ та не є обов’язковими для більшості випадків ЕЕ. Кислотний рефлюкс оцінюється або за допомогою 96-годинної некаліброваної системи тестування рефлюксу Bravo™ від Medtronic, або за допомогою 24-годинного імпедансного pH-тесту з урахуванням кислотної супресії.
Амбулаторний моніторинг pH за допомогою різних методів корисний у пацієнтів з рефрактерним перебігом ЕЕ або атиповими симптомами для кількісного оцінювання типу та ступеня ГЕР. Багатоканальний внутрішньостравохідний імпедансний рН-моніторинг може виявляти епізоди зміни pH незалежно від рівня pH.
Стравохідна манометрія не потрібна для обстеження більшості пацієнтів з ЕЕ. Однак вона може бути корисною в рефрактерних випадках для виявлення порушень моторики стравоходу, як-от ахалазія, забезпечення правильного розміщення pH-сенсора багатоканального внутрішньопросвітного імпедансу та для обстеження пацієнтів перед оперативним утручанням.
ЛІКУВАННЯ
Фармакологічна терапія
Мета лікування EE полягає в усуненні симптомів, загоєнні ерозій, веденні та/або запобіганні ускладненням, а також підтриманні ремісії. У більшості випадків для цього достатньо зміни способу життя та медикаментозного лікування (табл. 2).
Однієї лише зміни способу життя недостатньо для контролю хвороби, її слід рекомендувати як доповнення до медикаментозного лікування. Засоби, що покращують моторику, мають обмежений успіх і є недостатніми для лікування ЕЕ. Їх використання показано лише при ознаках гастропарезу або поганому кліренсі стравоходу.
Сукральфат – це засіб для захисту слизової оболонки, ефективний лише при загоєнні ЕЕ та рекомендований лише вагітним з ГЕР. Секвестранти жовчних кислот, як-от холестирамін і колесевелам, не довели свою ефективність при ЕЕ.
Засоби, що знижують кислотність
До засобів, які знижують кислотність, належать антациди, антагоністи H2-рецепторів гістаміну (АН2Р), інгібітори протонної помпи (ІПП) та калій-конкурентні блокатори секреції соляної кислоти (К-КБК). Антациди майже не відіграють жодної ролі в лікуванні ЕЕ. АН2Р корисні при лікуванні ЕЕ й однаково ефективні в еквівалентних дозах.
ІПП дуже ефективні для лікування ЕЕ, забезпечують чудове пригнічення кислотності й ефективне полегшення симптомів. ІПП однаково ефективні при ЕЕ. Існує значний ризик кислотного рикошету після припинення терапії, тому потрібно дотримуватися схеми поступового зниження дози, щоб уникнути рецидиву симптомів і загострення.
Близько 15% пацієнтів можуть бути резистентними до лікування без повної ремісії після 8 тижнів терапії ІПП. Оптимізація терапії ІПП за резистентності до стандартного лікування передбачає правильне дозування за 30 хвилин до їди. Для пацієнтів, які залишаються резистентними, може бути корисним перехід на інший ІПП. У резистентних пацієнтів дозування ІПП двічі на день перед сніданком і вечерею може покращити симптоми. Було показано, що додавання АН2Р на ніч до терапії ІПП двічі на день зменшує нічний кислотний прорив і симптоми ГЕРХ. Однак тахіфілаксія H2-рецепторів може обмежувати їхню корисність.
К-КБК є новим і вагомим доповненням до лікування EE. На відміну від ІПП, К-КБК конкурентно пригнічують стимульоване калієм дефосфорилювання та секрецію кислоти шляхом зворотного зв’язку з E2P-формою протонного насоса H+/K+-АТФази. К-КБК швидше підвищують внутрішньошлунковий pH і забезпечують такий самий ступінь блокування кислоти, як й ІПП. Пригнічення кислотності не є надмірно тривалим, що потенційно знижує ризик рикошетної гіперсекреції кислоти після припинення терапії. Високоефективними для лікування EE є фумарат вонопразану та тегопразан.
Оскільки рецидиви є поширеними в пацієнтів з EE, оптимальне лікування часто потребує тривалої підтримувальної терапії, особливо в пацієнтів з ЕЕ ступеня C та D. За належного моніторингу та дозування тривале лікування є безпечним.
Потенційні ускладнення тривалого застосування кислотосупресивних препаратів
Тривале пригнічення кислотності може впливати на всмоктування вітаміну B12, заліза та кальцію, проліферацію бактерій і метаболізм ліків. Остеопороз і переломи кісток є потенційними проблемами при застосуванні ІПП, АН2Р і К-КБК. Розмноження бактерій може призводити до позалікарняної пневмонії та шлунково-кишкових інфекцій, як-от коліт, пов’язаний із Clostridium difficile. ІПП, АН2Р і К-КБК також можуть впливати на всмоктування та метаболізм деяких ліків через шляхи P-450 CYP2C19 і P-450 3A4. Утім, ці препарати є безпечними й ефективними для тривалого лікування EE.
Лікування EE під час вагітності
У вагітних ЕГДС для підтвердження діагнозу EE не є необхідною. Її варто проводити лише за наявності вагомих показань і, якщо можливо, відкласти до другого триместру. АН2Р та ІПП, ймовірно, безпечні для вагітних і жінок, що годують груддю, К-КБК для них небезпечні. Усі АН2Р належать до категорії B за класифікацією Управління США з контролю продовольства та медикаментів (FDA), ІПП належать до категорії B за класифікацією FDA, за винятком омепразолу, який належить до категорії C. При лікуванні вагітних з EE сукральфат, АН2Р та ІПП можна використовувати після консультації з акушером-гінекологом.
Процедурна терапія
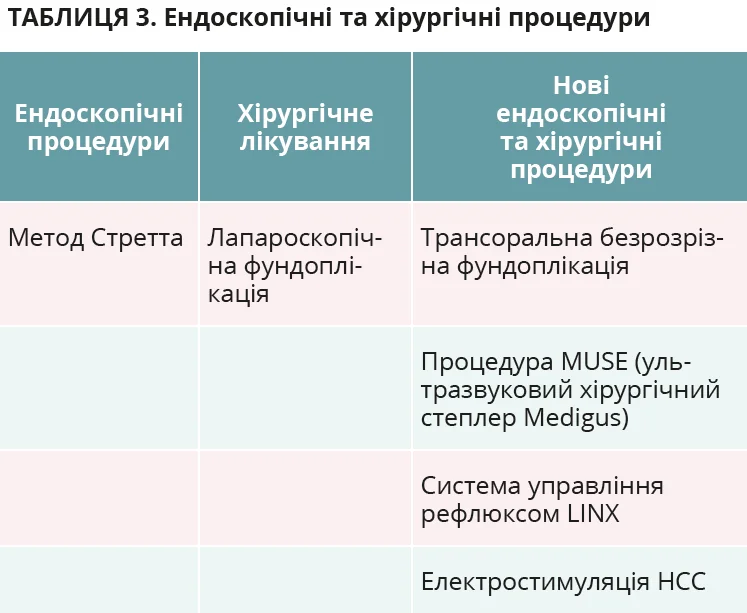
Більшість пацієнтів з ЕЕ можна успішно лікувати медикаментами. Однак у деяких випадках необхідне інвазивне хірургічне або ендоскопічне лікування (табл. 3).
Ендоскопічне та хірургічне лікування
Процедура Стретта
Процедура Стретта використовує радіочастотну енергію для підвищення базального тиску та зниження податливості НСС. Успіх процедури обмежений і не має значної переваги над плацебо.
Лапароскопічна фундоплікація
Антирефлюксна хірургія є варіантом для окремих пацієнтів з ЕЕ, які є резистентними або не можуть переносити чи дотримуватися тривалої фармакотерапії. Хірургічні результати перевершують медикаментозну терапію для пацієнтів з типовими симптомами або об’єктивними ознаками кислотного рефлюксу. Ускладнення лапароскопічної фундоплікації охоплюють диспепсію, дисфагію та синдром здуття живота з можливістю рецидиву симптомів.
Трансоральна безрозрізна фундоплікація (ТБФ)
ТБФ – ендоскопічна процедура, що виконується за допомогою пристрою EsophyX для ендоскопічної фундоплікації. Ефективність ТБФ подібна до такої лапароскопічної фундоплікації за Ніссеном і краща за терапію високими дозами ІПП. ТБФ можна розглядати для пацієнтів з килою стравохідного отвору діафрагми.
Система управління рефлюксом (LINX)
Система управління рефлюксом LINX – це пристрій для магнітної аугментації, який хірургічно розміщується навколо НСС, безпечний та ефективний за рефрактерного ЕЕ.
Електростимуляція НСС
Електростимуляція НСС – це створення електричної стимуляції для збільшення тиску НСС у стані спокою за допомогою імплантованого генератора імпульсів. Вона видається безпечною й ефективною для EE, але потребує подальшого оцінювання.
Процедура MUSE
MUSE – це процедура виконання трансоральної фундоплікації за допомогою хірургічного степлера під відео- й ультразвуковим контролем. Проте цей пристрій потребує подальшого оцінювання.
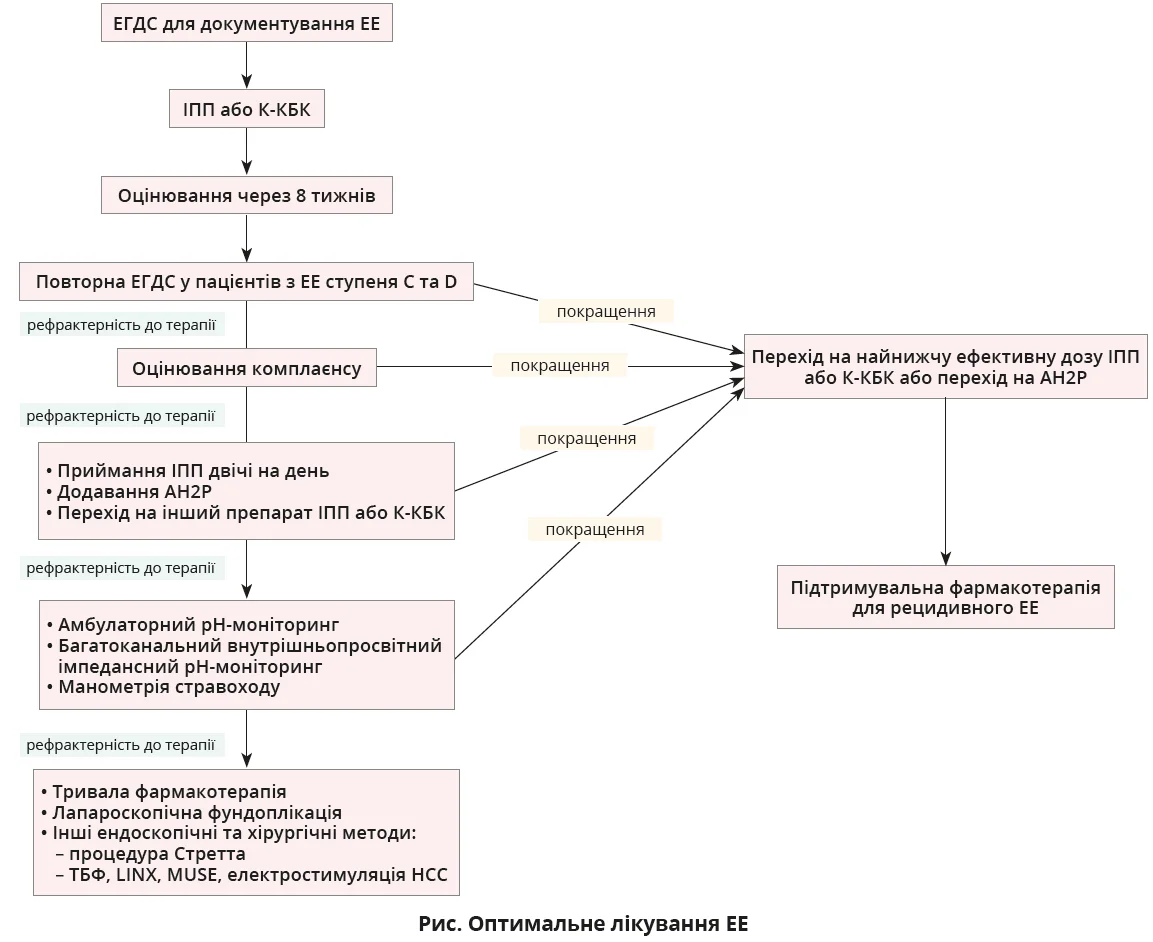
ОПТИМАЛЬНЕ ЛІКУВАННЯ ЕЕ
При ЕЕ терапію оптимізують поступово (рис.). Поетапна терапія ЕЕ починається із щоденного приймання ІПП або К-КБК протягом 8 тижнів.
ІПП та К-КБК забезпечують ендоскопічне загоєння ЕЕ в близько 86% пацієнтів. Якщо спостерігається покращення, супресію кислотності можна ослабити, знизивши дозу ІПП або К-КБК чи перейшовши на АН2Р. Пацієнтам з ЕЕ ступеня C та D за даними первинної ЕГДС треба пройти контрольну ЕГДС після 8 тижнів терапії для оцінювання загоєння та виключення стравоходу Барретта.
При легкому ЕЕ ІПП та К-КБК варто призначати лише за потребою. Терапія за потребою не рекомендується при тяжчому ЕЕ (ступінь C та D).
Пацієнтам з EE найчастіше потрібна підтримувальна супресія кислотності за допомогою ІПП або К-КБК через рецидив хвороби та потенційні ускладнення при зменшенні дози або припиненні приймання ліків. ІПП та К-КБК треба призначати в найнижчій дозі протягом найкоротшого періоду. Пацієнтам, які приймають ІПП довше 6 місяців, перед припиненням їх приймання дозу треба зменшувати поступово. АН2Р можуть використовуватися при легких або періодичних симптомах EE.
Хірургічне втручання й ендоскопічну терапію слід розглядати для рефрактерних пацієнтів або тих, хто довгостроково лікується ІПП або К-КБК і потребує припинення приймання ліків.
ВИСНОВКИ
Лікування ЕЕ найчастіше успішне за допомогою фармакологічних методів, особливо з використанням ІПП та К-КБК. У рефрактерних випадках можуть розглядатися хірургічне втручання й ендоскопічна терапія.
Література
Chait M.M. Optimal management of erosive esophagitis: an evidence-based and pragmatic approach. J. Transl. Gastroenterol. 2025; 3 (1): 39-46. doi: 10.14218/JTG.2025.00006.