Клінічні рекомендації Європейської асоціації з вивчення печінки (EASL) щодо «гостра-на-хронічну» печінкової недостатності
Переклала й адаптувала канд. мед. наук Тетяна Можина
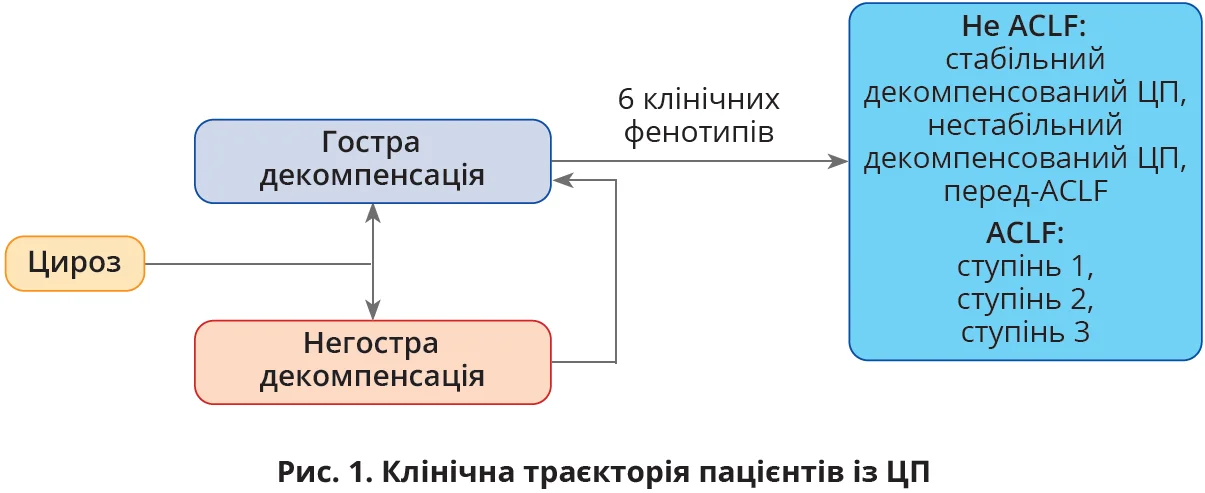
Під гострою декомпенсацією цирозу печінки (ЦП) розуміють розвиток асциту, енцефалопатії, шлунково-кишкової кровотечі (ШКК) або будь-якої комбінації зазначених розладів у хворих на ЦП (рис. 1). Гостра декомпенсація ЦП може виникати в будь-який час і зазвичай призводить до госпіталізації [1]. «Гостра-на-хронічну» печінкова недостатність (аcute-on-chronic liver failure, ACLF) є тяжкою формою гострої декомпенсації ЦП; вона асоціюється з високим рівнем 28-денної смертності – ≥20% (в осіб із гострою декомпенсацією ЦП без ACLF цей показник становить лише ≤5%) [2]. ACLF характеризується функціональною недостатністю ≥1 з 6 основних органів і систем (печінка, нирки, мозок, системи коагуляції, кровообігу та дихання) (рис. 2), а також системним запаленням, яке може бути індуковане провокувальними чинниками (внутрішньопечінковим та/або позапечінковим ураженням) [2, 3]. Це загальне визначення, що ґрунтується на доказах, розроблено під егідою EASL і консорціуму з хронічної печінкової недостатності (CLIF-С), яке прийнято та діє у великій кількості країн на різних континентах [4].
Метою цієї клінічної настанови є представлення рекомендацій, які допоможуть клініцистам розпізнавати ACLF, приймати рішення щодо госпіталізації (у відділення інтенсивної терапії (ВІТ) або не у ВІТ), ідентифікувати та корегувати провокувальні чинники, визначати органи й системи, які потребують підтримки або заміни (трансплантації), встановлювати потенційні критерії інтенсивної терапії та потенційні показання для трансплантації печінки.
Дефініція ACLF
Чи слід застосовувати поняття ACLF у пацієнтів із раніше перенесеними епізодами декомпенсації ЦП?
Рекомендації
У всіх пацієнтів незалежно від того, чи мали вони раніше епізоди декомпенсації, слід застосовувати термін ACLF (рівень доказовості (РД) 2, сильна рекомендація (СР), сильна згода).
Органи та системи, на які варто звернути увагу
Чи шкала CLIF-C OF, запропонована для оцінювання органної недостатності, перевершує інші шкали в ідентифікації тяжкої органної недостатності?
Рекомендації
• Різні види органної недостатності, які включені в критерії EASL-CLIF-C, слід використовувати для діагностики ACLF (РД 2, СР, згода).
• Недостатність ≥1 з 6 основних органів і систем, згідно з критеріями EASL-CLIF-C, слід використовувати для визначення тяжкості ACLF, ризику 28-денної смертності (РД 2, СР, сильна згода).
• Ризик 28-денної смертності в пацієнтів з ACLF слід оцінювати послідовно з метою оцінювання відповіді на лікування (РД 2, СР, згода).
Положення
• Недостатність печінки, нирок, мозку, системи зсідання крові, кровообігу та/або дихання, виявлена за шкалою CLIF-C OF, асоційована з високим рівнем летальності протягом 28 днів у пацієнтів із гострою декомпенсацією ЦП (РД 2, сильна згода).
• Кількість одночасно наявної недостатності різних органів і систем за шкалою CLIF-C OF асоційована зі зростанням рівня смертності протягом 28 діб (РД 2, сильна згода).
• Шкала CLIF-C OF, яка є складовою частиною шкал CLIF-C ACLF і ступеня тяжкості ACLF, валідована для послідовного використання та може багаторазово застосовуватися для визначення ризику 28-денної смертності (РД 2, сильна згода).
• Шкала CLIF-C OF валідована в багатьох країнах (РД 2, сильна згода).
• Класифікація Північноамериканського консорціуму з вивчення термінальної хвороби печінки (NACSELD) для діагностики ACLF недооцінює ризик смерті пацієнтів із гострою декомпенсацією ЦП. Шкала NACSELD недооцінює 28-денну та 90-денну смертність пацієнтів із гострою декомпенсацією ЦП (РД 2, сильна згода).
• Шкала AARC (розроблена робочою групою Азійсько-Тихоокеанської асоціації з вивчення печінки (APASL) з дослідження ACLF) застосовується в пацієнтів, у яких діагностовано ACLF згідно з критеріями APASL. Критерії ACLF недооцінюють ризик смерті пацієнтів з ACLF порівняно з критеріями EASL-CLIF-C; шкала АARC недооцінює 28-денну та 90-денну смертність у цих хворих (РД 2, згода).
Провокувальні чинники, на які варто звернути увагу
Які провокувальні чинники слід ідентифікувати при ACLF?
Рекомендації
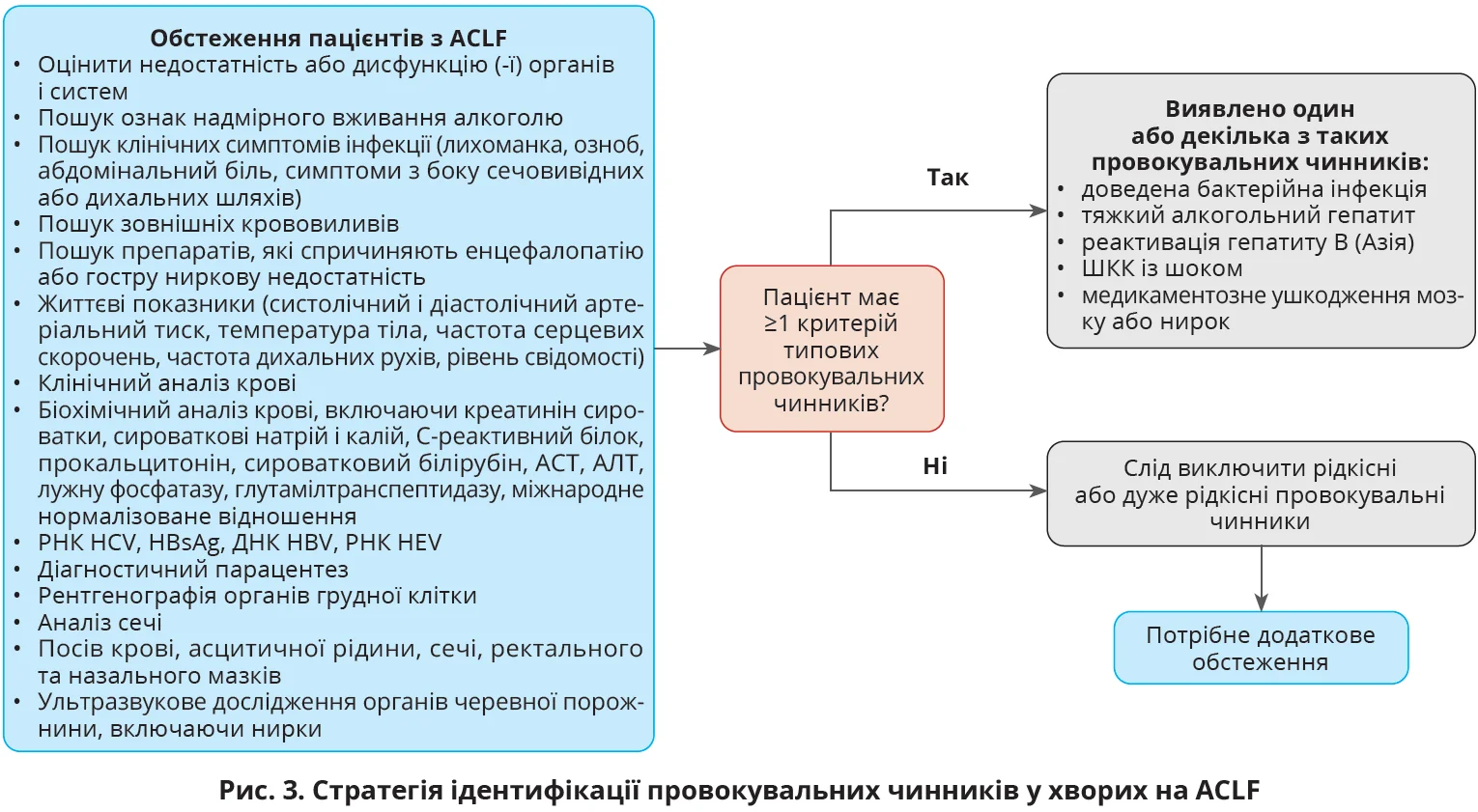
• Кожен пацієнт, госпіталізований із приводу ACLF, або хворі, в яких АCLF виникла під час перебування в лікарні, мають проходити системне обстеження, потрібне для виявлення типових провокувальних чинників, які включають підтверджену бактерійну інфекцію, алкогольний гепатит, ШКК з гемодинамічною нестабільністю, спалах HBV-інфекції, інфікування вірусом гепатиту Е, нещодавнє застосування лікарського засобу, здатного спричинити церебральну або ниркову недостатність (РД 2, СР, сильна згода).
• Пацієнтам, у яких системне обстеження не виявило провокувальних чинників, необхідно провести індивідуальну оцінку залежно від клінічної ситуації з виключенням усіх потенційних рідкісних провокувальних чинників (РД 5, СР, сильна згода).
Положення
• Предиктором АCLF є гостре внутрішньопечінкове або позапечінкове ураження, здатне спричинити дисфункцію органів (РД 2, сильна згода).
• Кількість одночасно наявних провокувальних чинників є основним показником, який визначає короткостроковий результат лікування хворих на АCLF (РД 2, сильна згода).
Прогнозування АCLF та смерті
Чи шкала CLIF-C AD, призначена для оцінювання гострої декомпенсації, є точнішою за інші прогностичні шкали в прогнозуванні ризику розвитку ускладнень із боку печінки, АCLF та 90-денної смертності без трансплантації печінки в пацієнтів без ACLF?
Рекомендації
• У пацієнтів без АCLF слід використовувати шкалу CLIF-C AD для оцінки прогнозу щодо 90-, 180- та 365-денної смертності (РД 2, СР, сильна згода).
• Шкали CLIF-C AD, MELD або MELD-Na можуть використовуватися для визначення ризику розвитку АCLF (РД 2, СР, згода).
Положення
• У пацієнтів із гострою декомпенсацією ЦП без ACLF шкала CLIF-C AD надає точнішу прогностичну інформацію щодо ризику 90-, 180- та 365-денної смертності, ніж шкали MELD, MELD-Na, Чайлд – П’ю (РД 2, згода).
• Шкали CLIF-C AD, MELD та MELD-Na подібні в прогнозуванні виникнення ACLF і перевершують шкалу Чайлд – П’ю (РД 2, згода).
Чи шкала CLIF-C ACLF є точнішою за інші прогностичні моделі в пацієнтів з ACLF?
Рекомендації
• У пацієнтів з ACLF шкалу CLIF-C ACLF слід використовувати послідовно для отримання прогностичної інформації (РД 2, СР, сильна згода).
Положення
• У хворих на ACLF шкала CLIF-C ACLF надає точнішу інформацію в прогнозуванні ризику 28-денної та 90-денної смертності, ніж шкали MELD, MELD-Na, Чайлд – П’ю (РД 2, сильна згода).
Лікування
Госпіталізація у ВІТ
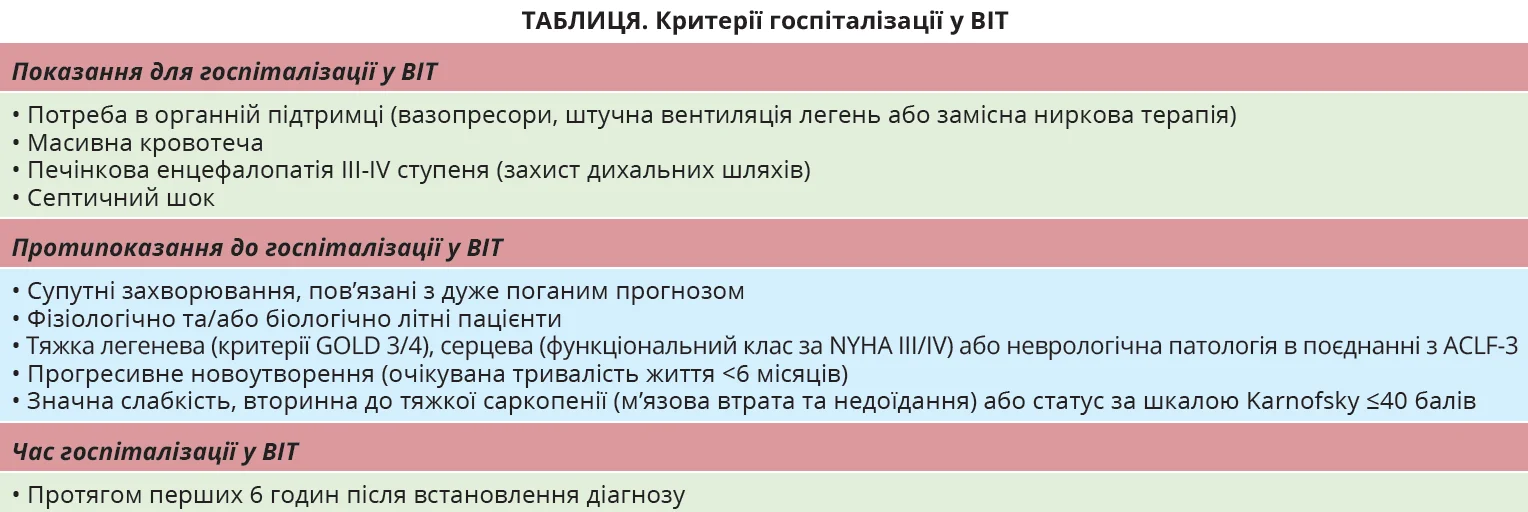
Чи застосування запропонованих критеріїв (табл.) корисне під час відбору пацієнтів, які потребують госпіталізації у ВІТ?
Рекомендації
• Пацієнтів з ACLF, які потребують ретельного моніторингу або підтримки життєздатності окремих органів, слід госпіталізувати у ВІТ (РД 3, СР, сильна згода).
• Госпіталізацію хворих на ACLF із тяжкими супутніми захворюваннями у ВІТ пропонується розглядати в індивідуальному порядку (РД 5, слабка рекомендація, згода).
• Прогноз у пацієнтів з ACLF слід визначати після 3-7 днів забезпечення повної органної підтримки (РД 4, СР, згода).
• Недостатність ≥4 органів і систем або кількість балів за шкалою CLIF-C ACLF >70 балів в осіб, у яких неможливо виконати трансплантацію печінки, є критеріями для розгляду питання щодо доцільності припинення підтримки органів / паліативної допомоги після 3-7 днів забезпечення повної підтримки органів (РД 4, СР, сильна згода).
Положення
• Критерії прийняття рішення щодо госпіталізації у ВІТ пацієнтів з ACLF подібні до тих, що застосовуються в популяції пацієнтів без ЦП; результати перебування у ВІТ зіставні за умови зіставності вихідних клінічних характеристик (РД 4, згода).
Гострі внутрішньопечінкові провокувальні чинники
Чи впливає лікування реактивації HBV на результати ACLF?
Рекомендації
• Аналоги нуклеозидів слід негайно призначити пацієнтам із HBV-асоційованою ACLF (РД 2, СР, сильна згода).
• У пацієнтів із HBV-асоційованою ACLF слід розглянути можливість трансплантації печінки за тяжкого перебігу хвороби (наприклад, оцінка за шкалою MELD >30; ACLF-2 або -3), незважаючи на ранню противірусну терапію, особливо за відсутності ранньої вірусологічної відповіді (зниження вірусного навантаження на <2 log) і відсутності клінічного поліпшення (РД 2, СР, згода).
Положення
• Призначення аналогів нуклеозидів пацієнтам із HBV-асоційованим ACLF сприяє зниженню смертності (РД 2, сильна згода).
Чи потрібно пацієнтам з автоімунним гепатитом (АІГ) й ACLF призначати кортикостероїди?
Рекомендації
• Співвідношення користь/ризик від лікування кортикостероїдами в пацієнтів з АІГ й ACLF слід оцінювати індивідуально в кожному конкретному випадку, але застосування кортикостероїдів слід уникати за наявності супутньої неконтрольованої інфекції (РД 5, СР, згода).
• Якщо кортикостероїди призначаються пацієнтам з АІГ й ACLF, потрібно ретельно моніторувати виникнення інфекційних ускладнень та ефективність кортикостероїдів (РД 2, СР, сильна згода).
Положення
• Докази ефективності кортикостероїдів у хворих на АІГ й ACLF значно обмежені (РД 5, сильна згода).
Чи потрібно хворим на алкогольний гепатит і ACLF-2/-3 призначати кортикостероїди?
Рекомендації
• Кортикостероїди не рекомендуються пацієнтам із тяжким алкогольним гепатитом і ACLF-3, а також пацієнтам із неконтрольованою бактерійною інфекцією (РД 3, СР, згода).
• Якщо кортикостероїди призначають пацієнтам із тяжким алкогольним гепатитом і ACLF, варто проводити ретельний моніторинг розвитку інфекційних ускладнень (РД 2, СР, згода).
Положення
• Зі збільшенням тяжкості ACLF відповідь на кортикостероїди прогресивно знижується, тоді як ризик інфікування збільшується (РД 2, сильна згода).
Гострі позапечінкові провокувальні чинники
Варикозна кровотеча
Чи покращує транс’югулярне внутрішньопечінкове портосистемне шунтування (TIPS) результати у хворих із варикозною кровотечою й ACLF?
Рекомендації
• Слід розглянути як профілактичне, так і рятувальне встановлення TIPS у пацієнтів з ACLF і варикозною кровотечою, які не мають протипоказань для встановлення TIPS (РД 3, СР, сильна згода).
Положення
• Варикозна кровотеча в пацієнтів з ACLF асоціюється з дуже високою ймовірністю повторної кровотечі (РД 3, сильна згода).
• У пацієнтів з ACLF наявність печінкової енцефалопатії не слід розглядати як абсолютне протипоказання до встановлення TIPS (РД 4, згода).
Бактерійні та грибкові інфекції
Чи впливають емпіричні стратегії призначення антибіотиків, адаптовані до тяжкості інфекції та місцевої епідеміології, на результати лікування хворих на ACLF?
Рекомендації
• Емпірична антибіотикотерапія хворих на ACLF із підозрою на інфекційну патологію має бути адаптована відповідно до місцевої епідеміології бактерійних інфекцій, наявності чинників ризику виникнення антибіотикорезистентності (РД 2, СР, сильна згода).
• Пацієнтам із септичним шоком або погіршенням ACLF слід емпірично призначити антибіотики широкого спектра дії, які охоплюють усі потенційні збудники (РД 4, СР, сильна згода).
Чи впливає рання емпірична антибіотикотерапія на прогноз інфікованих пацієнтів з ACLF?
• Пацієнти з ACLF і підозрою на бактерійну інфекцію мають отримати якомога швидше емпіричну антибіотикотерапію широкого спектра дії з урахуванням місцевої епідеміології (РД 3, СР, згода).
• У хворих на ACLF із підозрою на бактерійну інфекцію рекомендується швидко провести всебічне обстеження на інфекції (РД 5, СР, згода).
Чи варто проводити ранню деескалацію емпіричної антибіотикотерапії в пацієнтів з ACLF?
• Ранню деескалацію емпіричної антибіотикотерапії (протягом 24-72 годин) рекомендується застосовувати в пацієнтів з ACLF, які отримують антибіотики широкого спектра дії. Деескалація має ґрунтуватися на результатах швидких мікробіологічних тестів і даних щодо колонізації багаторезистентними мікроорганізмами (РД 5, СР, згода).
Чи впливає емпірична протигрибкова терапія на прогноз ACLF?
• Емпірична протигрибкова терапія може бути показана пацієнтам з ACLF, у яких розвивається нозокоміальний септичний шок, і хворим, які мають додаткові чинники ризику грибкової інфекції (РД 5, СР, сильна згода).
Екстракорпоральна підтримка печінки
Чи впливає штучна/біоштучна екстракорпоральна підтримка печінки на прогноз ACLF?
Рекомендації
• Рутинне використання штучної або біоштучної екстракорпоральної підтримки печінки чи плазмообміну при ACLF поза межами дослідницьких випробувань не рекомендується (РД 2, СР, сильна згода).
Положення
• Хоча альбуміновий діаліз може зменшити тяжкість печінкової енцефалопатії, немає жодних доказів того, що він покращує виживання пацієнтів з ACLF (РД 2, згода).
Модулятори імунітету
Чи гранулоцитарно-колонієстимулювальний фактор покращує результати лікування пацієнтів з ACLF незалежно від кількості лейкоцитів?
Рекомендації
• Рутинне введення гранулоцитарно-колонієстимулювального фактора хворим на ACLF не рекомендується (РД 3, СР, сильна згода).
Нутритивна підтримка, саркопенія й астенія
Чи покращують нутритивна підтримка та реабілітаційні заходи результати лікування хворих на ACLF?
Рекомендації
Застосування неселективних β-блокаторів (НСББ)
Чи варто продовжувати прийом НСББ у пацієнтів з ACLF?
Рекомендації
• У пацієнтів з ACLF рішення про продовження прийому НСББ пропонується приймати індивідуально в кожному конкретному випадку з ретельним титруванням дози на підставі ретельного моніторингу середнього артеріального тиску та функції нирок (РД 5, СР, згода).
• У пацієнтів, які одужують після епізоду ACLF, прийом НСББ слід розпочинати обережно з ретельним моніторингом артеріального тиску. Підвищувати дозу слід відповідно до середнього артеріального тиску; нижче порогового значення 65 мм рт. ст. корисні ефекти обмежені (РД 5, СР, згода).
Положення
• У жодному спеціальному дослідженні не вивчалися безпека й ефективність ініціації прийому НСББ у пацієнтів, які одужують після епізоду ACLF. Отже, вплив НСББ на результати невідомий (сильна згода).
Трансплантація печінки
Чи трансплантація печінки покращує виживання пацієнтів із тяжкою ACLF (ACLF-2/-3)?
Рекомендації
• Раннє обстеження щодо доцільності проведення трансплантації печінки варто пропонувати всім пацієнтам із тяжким перебігом ACLF (ACLF-2/-3) (РД 2, СР, сильна згода).
Положення
• Трансплантація печінки асоціюється зі значним покращенням виживання пацієнтів із тяжкою ACLF, але межі придатності пацієнтів до трансплантації печінки поки чітко не визначені (РД 2, сильна згода).
• Трансплантація печінки пацієнтам із тяжкою ACLF асоційована зі зростанням використання ресурсів (РД 3, сильна згода).
Чи повинні пацієнти з тяжкою ACLF (ACLF-2/-3) мати пріоритет у списку очікування?
Рекомендації
• Пацієнтів з ACLF-3 варто пріоритетно включати в список очікування, заснований на шкалі MELD (-Na), для зменшення надмірної смертності (РД 2, СР, згода).
• Ми рекомендуємо застосовувати пілотні програми пріоритизації пацієнтів з ACLF-3 у списку очікування (РД 5, СР, згода).
Положення
• Наявні системи розподілу недооцінюють смертність пацієнтів із тяжкою ACLF (ACLF-2/-3), які перебувають у списку очікування (РД 2, сильна згода).
• Відтермінування трансплантації печінки пацієнтам із тяжкою ACLF (ACLF-2/-3) збільшує ризик смертності під час перебування в списку очікування та після трансплантації (РД 3, сильна згода).
Чи слід застосовувати критерії безперспективності трансплантації печінки в пацієнтів із тяжкою ACLF (ACLF-2/-3)?
Рекомендації
• Безперспективність трансплантації печінки пацієнтам з ACLF-3 слід вирішувати в індивідуальному порядку з урахуванням незалежних предикторів післятрансплантаційної смертності (РД 5, СР, сильна згода).
Положення
• Визначення критеріїв безперспективності трансплантації печінки в пацієнтів з ACLF-3 є нагальною медичною потребою (сильна згода).
Чи слід розглядати живих донорів для трансплантації печінки пацієнтам з ACLF-3?
Рекомендації
• Трансплантація печінки від живого донора має розглядатися в пацієнтів з ACLF-3 та проводитися у високоспеціалізованих центрах (РД 2, СР, згода).
Висновки
ACLF тепер визнано окремою клінічною одиницею, пов’язаною з високим ризиком короткочасної смерті. Основними принципами ведення хворих на ACLF є своєчасна діагностика та лікування провокувальних чинників, забезпечення підтримки органів і систем.
Література
EASL Clinical Practice Guidelines on acute-on-chronic liver failure. J. Hepatol. 2023; 79 (2): 461-491. doi: 10.1016/j.jhep.2023.04.021.