Діагностика та лікування еозинофільного езофагіту: клінічні рекомендації Американського коледжу гастроентерологів
Переклала й адаптувала канд. біол. наук Олександра Демецька
Клінічна настанова Американського коледжу гастроентерологів (ACG) є оновленням документа 2013 року. Нові рекомендації створено для підтримання клінічної практики та пропонують доцільні підходи до типового пацієнта з еозинофільним езофагітом (ЕоЕ) на підставі наявної доказової бази.
Зміна парадигми в діагностиці та лікуванні ЕоЕ
За останнє десятиріччя відбулися зміни парадигми в діагностиці та лікуванні EoE, котрий визначено як адаптивне імунне, опосередковане Т-клітинами запальне захворювання стравоходу 2-го типу, спричинене алергенами, що характеризується симптомами дисфункції стравоходу та переважальним еозинофільним інфільтратом у стравоході.
У разі затримки діагностики або прогалин у лікуванні EoE прогресує від запального до фібростенозного фенотипу в більшості, але не в усіх пацієнтів. Із погляду діагностики попередні рекомендації ACG зосереджувалися на суперечках, пов’язаних з еозинофілією стравоходу, що реагує на інгібітори протонної помпи (ІПП), і вимагали «невдачі» випробування ІПП перед установленням остаточного діагнозу EoE. Однак нові дані змінили цей підхід, наслідком чого стала поява консенсусних рекомендацій, котрі уточнюють і оптимізують діагностичний алгоритм, усувають випробування ІПП, натомість позиціонуючи цю групу препаратів як терапію EoE, а не як діагностичний критерій.
Оскільки EoE є хронічним захворюванням, то лікування зазвичай має бути тривалим. Кульмінацією клінічних випробувань стало схвалення двох топічних стероїдів й одного біологічного препарату для лікування EoE, а також поява нових перспективних кандидатів на терапію та збільшення кількості даних щодо дієтичних утручань.
Діагностика
Незважаючи на зміни в діагностичних підходах, концептуальне визначення самої хвороби залишилося незмінним: EoE – це алергено-/ імуноопосередкований клініко-патологічний стан, що клінічно характеризується симптомами дисфункції стравоходу, а гістопатологічно – вираженим еозинофільним інфільтратом стравоходу. Усі симптоми EoE є неспецифічними та мають широку диференційну діагностику.
EoE діагностується за такими трьома критеріями: симптоми дисфункції стравоходу; принаймні 15 еозинофілів у полі зору (еоз/пз) при великому збільшенні; оцінювання розладів, не пов’язаних з EoE, які спричиняють або можуть спричиняти еозинофілію стравоходу.
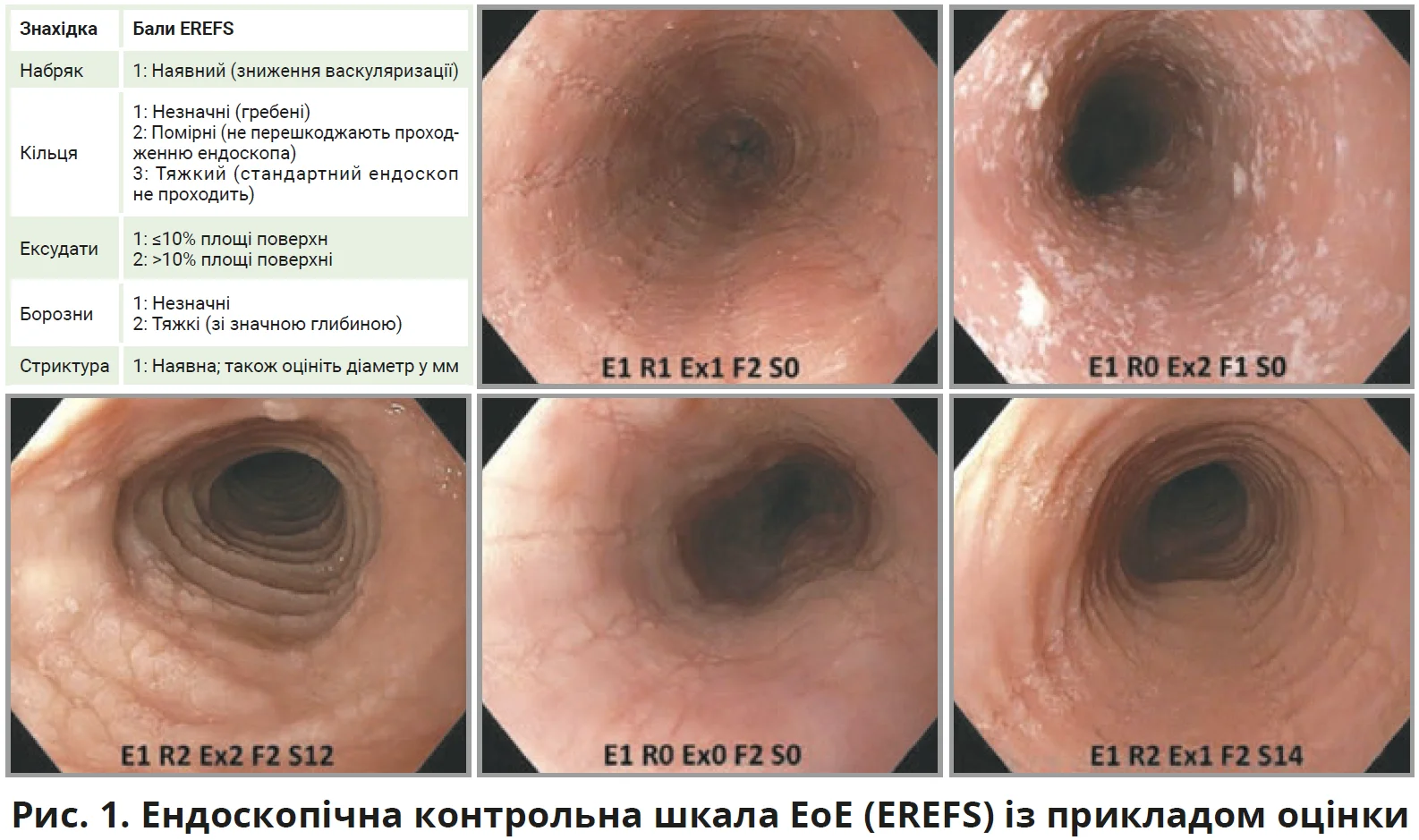
Критичним аспектом обстеження є оцінювання результатів EoE за допомогою ендоскопічної контрольної шкали (EREFS), яка класифікує 5 ключових ознак EoE за ступенем тяжкості, включно з набряками, кільцями, ексудатами, борознами та стриктурами, що дає змогу отримати оцінку в діапазоні від 0 до 9, при цьому кожна ознака оцінюється за найгіршим виглядом ділянки стравоходу (рис. 1).
Рекомендації
- Рекомендується діагностувати еозинофілію стравоходу на підставі наявності симптомів дисфункції стравоходу та не менш ніж 15 еоз/пз при великому збільшенні під час біопсії стравоходу після оцінювання порушень, не пов’язаних з еозинофілією, які спричиняють або можуть спричиняти еозинофілію стравоходу (якість доказів: низька; сила рекомендації: сильна).
- Рекомендовано використовувати систематичну ендоскопічну систему оцінювання, наприклад ендоскопічну контрольну шкалу EREFS для характеристики ендоскопічних знахідок EoE під час кожної ендоскопії (якість доказів: низька; сила рекомендації: сильна).
- Рекомендовано отримати щонайменше
6 біопсій стравоходу принаймні з 2 рівнів стравоходу (наприклад, проксимального/середнього та дистального), орієнтуючись на результати ендоскопії EoE, якщо можливо, для оцінювання гістологічних особливостей, які відповідають EoE (якість доказів: низька; сила рекомендації: сильна). - Рекомендовано визначати кількість еозинофілів за біопсії стравоходу під час кожної ендоскопії, що виконується для EoE (якість доказів: низька; сила рекомендації: сильна).
Ведення
Цілі лікування EoE полягають у покращенні симптомів і якості життя пацієнта, покращенні або нормалізації ендоскопічного та гістологічного вигляду стравоходу, нормалізації росту й розвитку дітей, підтриманні харчування та запобіганні ускладненням, як-от защемлення їжі, звуження стравоходу й перфорація.
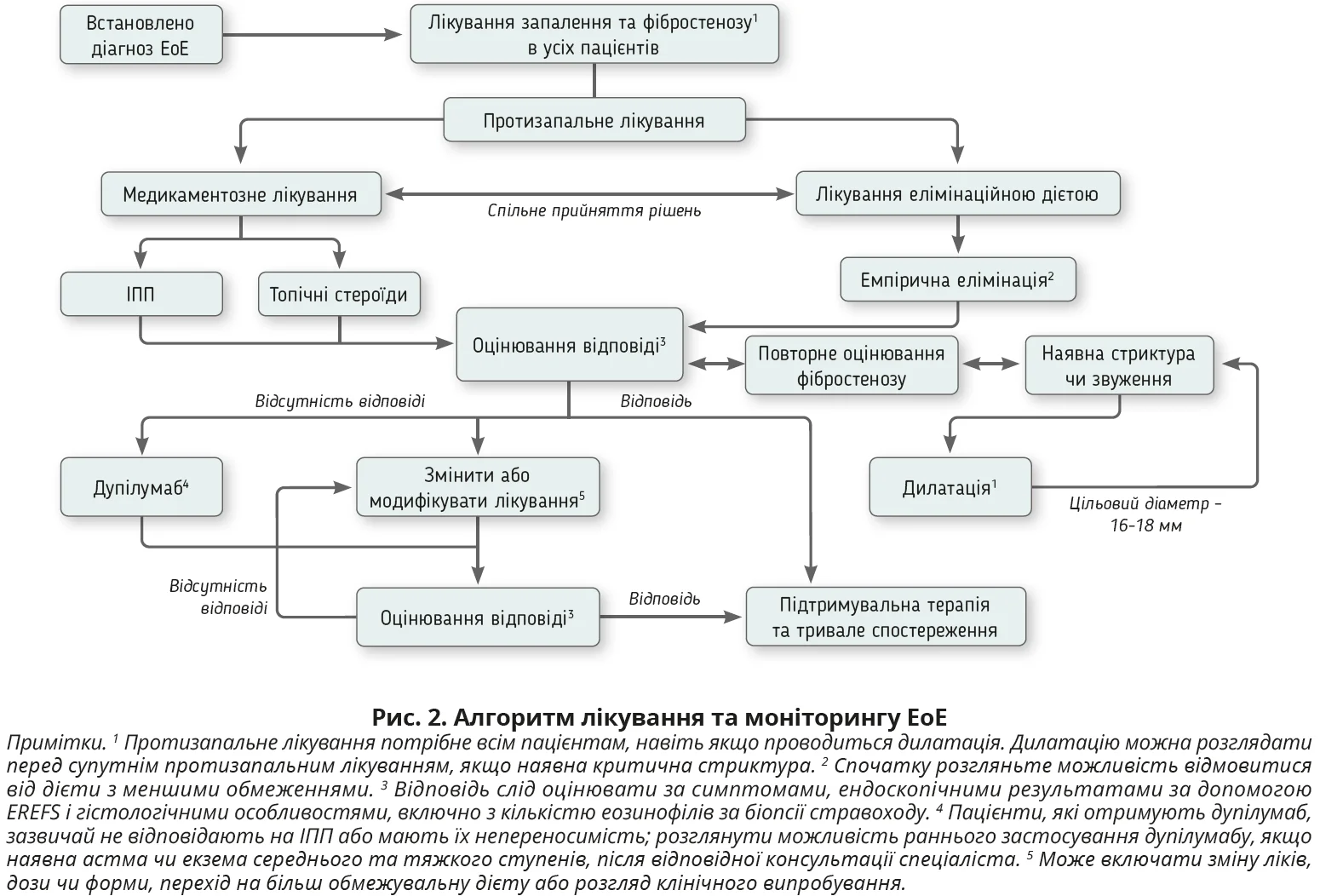
Для цього потрібно звернути увагу як на запальний, так і на фібростенозний аспекти хвороби. Фармакологічна чи дієтична терапія може лікувати запальний компонент, а також сприяти покращенню калібру стравоходу. Розширення (дилатація) стравоходу використовується для лікування стриктур і звуження просвіту. Рішення про вибір терапії приймається індивідуально на підставі характеристик захворювання та переваг пацієнта. Загалом доцільно спочатку обрати одну протизапальну терапію, а відповідь на лікування оцінювати за клінічною, ендоскопічною та гістологічною активністю хвороби (рис. 2).
Рекомендації
- ІПП рекомендовано для лікування EoE (якість доказів: низька; сила рекомендації: умовна).
Обґрунтування використання ІПП для лікування EoE виходить за межі антисекреторного ефекту. ІПП мають численні ефекти, крім блокування протонної помпи, і при EoE було описано кілька потенційних нових механізмів, включно зі зниженням експресії еотаксину-3 (основного цитокіну, який залучає еозинофіли до стравоходу), покращенням бар’єрної функції стравоходу й підтриманням транскрипційного гомеостазу епітелію стравоходу.
Із практичного погляду пропонується початкове лікування EoE «високими дозами» ІПП, які вдвічі перевищують затверджену рефлюксну дозу. ІПП можна застосовувати 1 або 2 рази на добу, виходячи з міркувань дотримання прихильності, оскільки дані про ефективність дозування є змінними: наприклад, гістологічна ремісія була значно вищою при застосуванні омепразолу 20-40 мг двічі на добу (53-54%), ніж 20-40 мг 1 раз на добу (10-12%; P<0,0001).
І навпаки, проспективне когортне дослідження показало, що >80% пацієнтів, які реагували на ІПП, підтримували гістологічну ремісію після переходу із 40 мг омепразолу 2 рази на день до 40 мг 1 раз на день і до 20 мг 1 раз на день. Отже, використання одноразових доз у пацієнтів з EoE є можливим. Зокрема, було виявлено 61% гістологічної відповіді на приймання езомепразолу 40 мг 1 раз на добу.
- Використання топічних стероїдів для внутрішнього застосування рекомендовано для лікування EoE (якість доказів: помірна; сила рекомендації: сильна).
- Пацієнтам з ЕоЕ, яким призначено топічні стероїди, запропоновано використовувати або флутиказону пропіонат, або будесонід (якість доказів: низька; сила рекомендації: умовна).
- Емпіричну елімінаційну дієту (ЕЕД) запропоновано як лікування EoE (якість доказів: низька; сила рекомендації: умовна).
За даними досліджень, частота гістологічної відповіді на елементарну дієту становила 93,6% порівняно з 13,3% у групі порівняння (плацебо). ЕЕД, що передбачає уникання продуктів, які найпевніше спричиняють EoE, є кращою як лікування першої лінії. З емпіричних дієтичних терапій, доступних для EoE, найкраще вивчена дієта з виключенням 6 продуктів, що передбачає відмову від загальних алергенів тваринного молока / молочних продуктів, пшениці, сої, яєць, горіхів/арахісу та риби/молюсків.
- Не пропонується використовувати наявні наразі алергопроби для прямого застосування ЕЕД при лікуванні ЕоЕ (якість доказів: дуже низька; сила рекомендації: умовна).
- Дупілумаб запропоновано для лікування EoE в осіб віком від 12 років, які не реагують на терапію ІПП (якість доказів: середня; сила рекомендації: умовна).
Дупілумаб – це моноклональне антитіло проти рецептора α інтерлейкіну-4 (ІЛ-4), котре блокує дію як інтерлейкінів (ІЛ-4, ІЛ-13), так і цитокінів, що є центральними для запального каскаду 2-го типу. Через спільні патогенетичні компоненти між атопічним дерматитом і EoE було проведено дослідження II фази, яке показало покращення при застосуванні дупілумабу порівняно з плацебо щодо симптомів дисфагії, гістологічної відповіді й ендоскопічної тяжкості після 12 тижнів лікування.
- Дупілумаб запропоновано для лікування EoE в педіатричних пацієнтів (віком від 1 до 11 років), які не реагують на терапію ІПП (якість доказів: низька; сила рекомендації: умовна).
- Немає можливості надати рекомендації за чи проти цендакімабу, бенралізумабу, лірентелімабу, меполізумабу або реслізумабу як лікування EoE.
Декілька цільових біологічних препаратів або вивчаються, або є експериментальними, або клінічно недоступними, або не мають достатніх доказів, щоб рекомендувати чи забороняти їх у разі EoE.
- Не рекомендовано використовувати омалізумаб як засіб лікування EoE (якість доказів: низька; сила рекомендації: умовна).
Омалізумаб є антитілом проти імуноглобуліну E (IgE), що схвалений для лікування астми та хронічної кропив’янки. Зважаючи на алергічний патогенез EoE, омалізумаб був протестований у рандомізованому плацебо-контрольованому клінічному дослідженні EoE, але не було відмінностей у результатах між активним препаратом і групою плацебо, хоча рівні IgE знизилися, як і очікувалося, під час лікування (це дослідження підтвердило, що EoE не є захворюванням, опосередкованим IgE).
- Не рекомендовано використовувати кромолін і монтелукаст для лікування EoE (якість доказів: дуже низька; сила рекомендації: умовна).
Дані, що підтверджують використання малих молекул при EoE, обмежені недостатнім розміром вибірки та відсутністю плацебо-контрольованих досліджень, хоча ця галузь швидко розвивається завдяки дослідженню кількох нових, але експериментальних агентів.
- Пропонується використовувати ендоскопічну дилатацію як доповнення до медикаментозної терапії для лікування стриктур стравоходу, що спричиняють дисфагію, в пацієнтів з EoE (якість доказів: низька; сила рекомендації: умовна).
Рекомендовано поєднувати дилатацію стравоходу з протизапальною терапією на підставі даних, що демонструють зниження потреби в дилатації стравоходу після гістологічної відповіді.
- Пропонується продовжувати ефективну дієтичну або фармакологічну терапію EoE, щоб запобігти рецидивам симптомів, гістологічному запаленню й ендоскопічним відхиленням (якість доказів: низька; сила рекомендації: сильна).
- Рекомендовано оцінювати відповідь на лікування EoE з огляду на симптоматичні, ендоскопічні та гістологічні результати (якість доказів: низька; сила рекомендації: сильна).
Повна нормалізація стравоходу відповідає EREFS 0, але було запропоновано й оцінено поріг ендоскопічної відповіді EREFS ≤2 (з використанням шкали 0-9). Для гістології кількість еозинофілів <15 еоз/пз (<60 еоз/мм2) є прийнятною метою для більшості пацієнтів, тому біопсію стравоходу слід виконувати під час кожної ендоскопії, де оцінюється EoE.
- У дітей з EoE та дисфагією запропоновано езофаграму для оцінювання фібростенозу (якість доказів: дуже низька; сила рекомендації: умовна).
- У дітей з ЕоЕ й порушенням харчової поведінки як додаткове терапевтичне втручання пропонується оцінювання лікарем-терапевтом з харчування та/або дієтологом (якість доказів: дуже низька; сила рекомендації: умовна).
Зростання (зріст, вага й індекс маси тіла), розвиток харчових навичок і харчування (правильне споживання поживних речовин) залишаються цілями лікування на додаток до симптоматичного, ендоскопічного та гістологічного покращення в дітей з EoE.
Майбутні напрями
Актуальні напрями охоплюють порівняльні дослідження ефективності терапевтичних агентів, вивчення біомаркерів для прогнозування відповіді на лікування з метою індивідуального вибору терапії (що також може включати використання генетичних, епігенетичних і негенетичних предикторів).
Крім того, необхідними є ідентифікація фенотипів і ендотипів, пов’язаних із прогресуванням фібростенозу, пошук нових методів ідентифікації харчових тригерів, а також ширше використання неінвазивних і мінімально інвазивних методів моніторингу.
Література
Dellon E.S. ACG clinical guideline: diagnosis and management of eosinophilic esophagitis. The American Journal of Gastroenterology. 2025; 120 (1): 31-59. doi: 10.14309/ajg.0000000000003194.