Рифаксимін як терапевтичний союзник у модуляції дисбіозу
Автор: Ігор Миколайович СКРИПНИК, доктор медичних наук, професор, президент ГО «Українська гастроентерологічна асоціація», проректор із науково-педагогічної роботи та післядипломної освіти, професор кафедри внутрішньої медицини № 1 Полтавського державного медичного університету
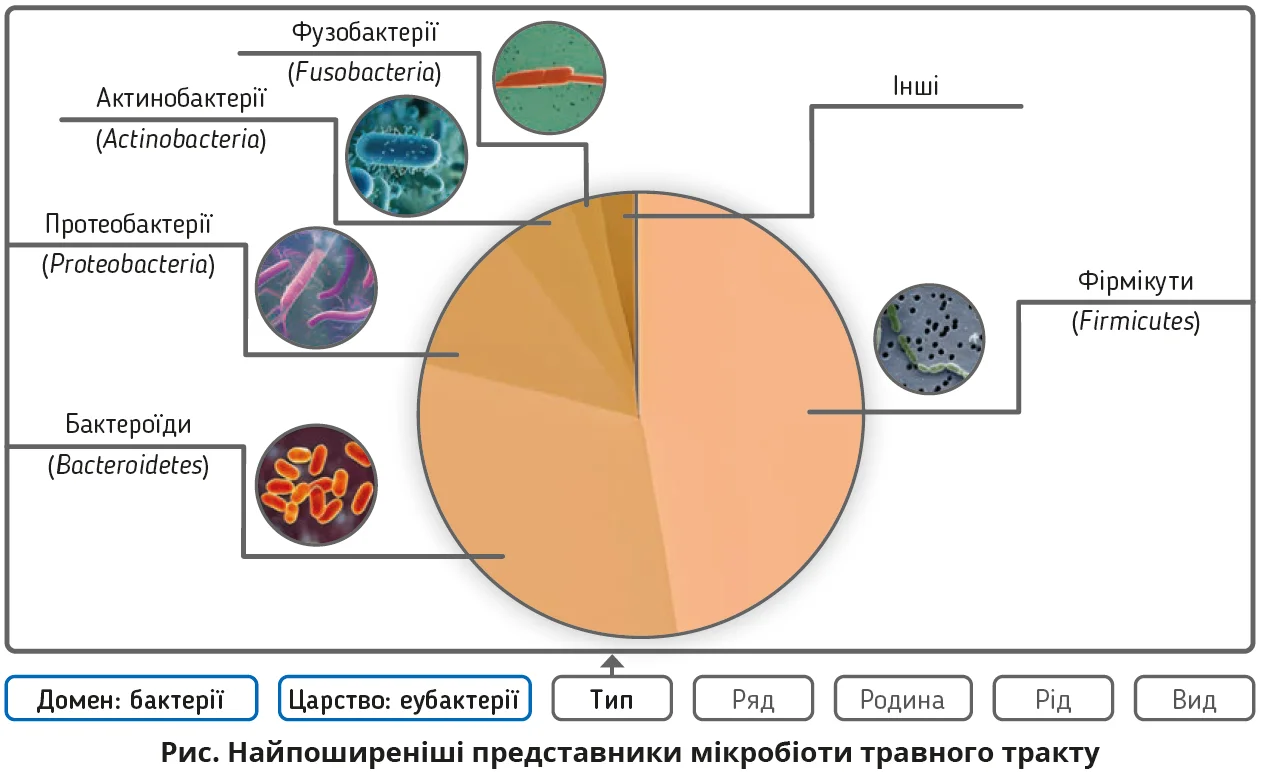
Кишкова мікробіота є складною динамічною екосистемою, що включає бактерії, археї, віруси (бактеріофаги), гриби, іноді найпростіших і відіграє ключову роль у травленні, метаболізмі поживних речовин, підтриманні імунітету та захисті від патогенів. Понад 90% мікробіоти кишківника людини належить до основних чотирьох типів: Firmicutes, Bacteroidetes, Proteobacteria й Actinobacteria; меншу частку становлять Fusobacteria й інші нечисленні групи (рис.).
Дисбіоз означає порушення балансу кишкової мікробіоти, коли склад і функції мікробної спільноти змінюються. Це може проявлятися як надмірне розмноження патогенів, зменшення кількості корисних видів або зниження загального мікробного різноманіття. Такі зміни спричиняють прозапальний стан, підвищену проникність кишкової стінки та посилення оксидативного стресу, призводячи до різних захворювань травної системи. Дисбіотичні зміни часто асоціюються із запальними захворюваннями кишківника (ЗЗК), синдромом подразненого кишківника (СПК), синдромом надмірного бактеріального росту (СНБР) і печінковою енцефалопатією (ПЕ).
Рифаксимін – невсмоктуваний антибіотик з переважною дією в шлунково-кишковому тракті – відіграє важливу роль у модулюванні дисбіозу. Механізм дії полягає в пригніченні синтезу бактеріальної РНК шляхом зв’язування з β-субодиницею ДНК-залежної РНК-полімерази, що блокує транскрипцію. Завдяки широкому спектру дії рифаксимін зменшує кількість патогенних бактерій у кишківнику, водночас зберігаючи корисні види. Селективна протимікробна активність сприяє відновленню балансу мікробіоти та полегшенню симптомів дисбіозу. Крім того, рифаксимін має протизапальні властивості, ймовірно, завдяки зниженню кишкового запалення, спричиненого бактеріальними ендотоксинами. Низьке системне всмоктування мінімізує ризик побічних ефектів, що робить препарат оптимальним для довготривалого лікування. Модулюючи кишкову мікробіоту, рифаксимін не лише усуває симптоми, а й впливає на їхню основну причину – мікробну дисфункцію, забезпечуючи комплексний терапевтичний підхід.
Ризик мікробної резистентності до рифаксиміну нижчий, аніж у більшості антибіотиків, через низьку водорозчинність і обмежену біодоступність у кишковому середовищі, що знижує негативні впливи на мікробіоту. Рифаксимін ефективно діє при низьких, субінгібуючих концентраціях, оскільки його механізми виходять за рамки простого знищення бактерій, впливаючи на вірулентність, метаболізм та прикріплення бактерій до епітеліальних клітин. Як антибіотик, що не всмоктується, він досягає високої локальної концентрації в кишечнику, проте його терапевтичні ефекти часто досягаються без необхідності високих системних або локалізованих концентрацій препарату, що знижує ризики резистентності.
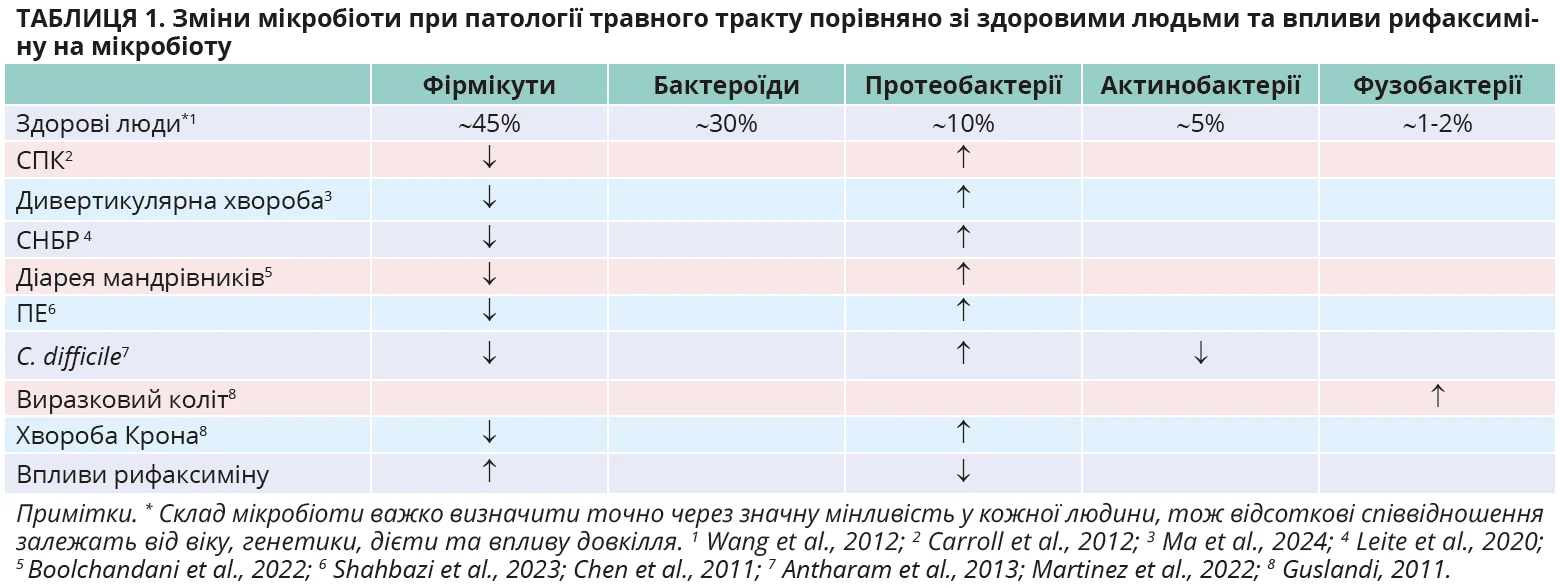
Отже, рифаксимін чинить селективну протимікробну дію, пригнічуючи надмірний ріст патогенних і прозапальних бактерій, зберігаючи або стимулюючи корисні популяції (табл. 1).
Синдром подразненого кишківника
Це функціональний розлад, який проявляється хронічним болем у животі та змінами характеру випорожнень. Виокремлюють СПК з діареєю (СПК-Д), СПК із закрепом, змішаний і некласифікований типи. Точна причина невідома, проте важливими чинниками вважають порушення взаємодії «кишківник – мозок», розлади моторики, вісцеральну гіперчутливість і зміни мікробіоти. Для СПК-Д характерне зниження різноманіття кишкових бактерій, зокрема збільшення протеобактерій і зменшення фірмікутів.
Рифаксимін широко досліджений у разі СПК-Д (табл. 2): значно зменшує здуття, діарею та біль у животі. Його ефективність було підтверджено великими рандомізованими контрольованими дослідженнями (РКД) TARGET 1 і TARGET 2, де рифаксимін у дозі 550 мг тричі на добу протягом 14 днів зменшував вираженість симптомів із тривалістю ефекту до 10 тижнів після припинення лікування. Метааналіз 19 РКД підтвердив ефективність і добрий профіль безпеки препарату: NNT=10 для загального покращення симптомів; побічні ефекти (нудота, головний біль) були подібні до таких на тлі плацебо.
Дослідження TARGET 3 підтвердило безпеку повторного застосування рифаксиміну в пацієнтів з рецидивами симптомів СПК-Д, демонструючи подібну ефективність і профіль безпеки при різних циклах лікування. Рекомендований курс – два цикли по 14 днів з перервою принаймні 10 тижнів.
Отже, рифаксимін рекомендований пацієнтам з СПК-Д, особливо за помірних-тяжких симптомів, але для інших типів СПК доказів недостатньо. Поряд з рифаксиміном як терапію першої лінії розглядають немедикаментозні втручання для комплексного ведення.
Крім того, препарат є перспективним за інших розладів, зокрема при здутті живота й функціональній диспепсії. Метааналіз 9 досліджень за участю 3326 пацієнтів показав значне покращення симптомів здуття (коефіцієнт ризику 1,22; 95% довірчий інтервал (ДІ) 1,11-1,35). Проте дослідження включали також пацієнтів з СПК, тому остаточні висновки щодо ефективності в окремих підгрупах важко зробити, адже досліджень саме для ізольованого здуття живота наразі немає. Щодо функціональної диспепсії, лише одне РКД оцінювало рифаксимін, показавши значне покращення симптомів (відрижка, переповненість після їжі), що вказує на потенційні переваги рифаксиміну.
Дивертикулярна хвороба
Дуже поширена в західних країнах, особливо серед людей віком понад 60 років. Охоплює спектр станів від безсимптомного дивертикульозу, який випадково виявляють під час колоноскопії, до гострого дивертикуліту внаслідок запалення чи інфекції дивертикулів.
Патофізіологія гострого дивертикуліту залишається дискусійною. Раніше вважали, що причиною є блокада дивертикулу каловим каменем з подальшим приєднанням інфекції, але нині основною теорією є хронічне запалення низького ступеня, ймовірно, пов’язане з дисбіозом. Важливими чинниками також є вісцеральна гіперчутливість, порушення моторики та дефекти стінки кишки.
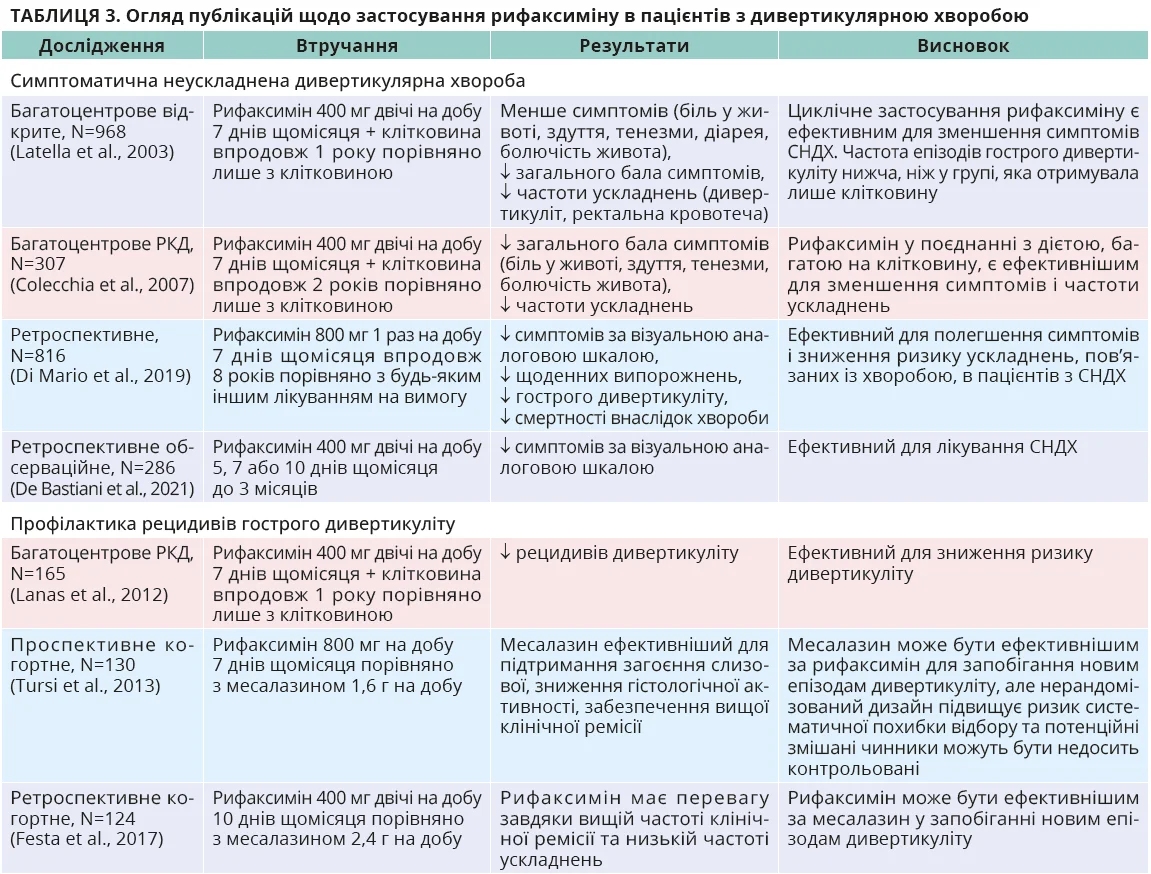
Рифаксимін застосовують для модифікації мікробіоти та зменшення запалення в разі симптоматичної неускладненої дивертикулярної хвороби (СНДХ) – поєднання дивертикулів і рецидивів болю в животі (табл. 3).
Близько 4% випадків СНДХ можуть прогресувати до гострого дивертикуліту. Поєднання рифаксиміну з клітковиною полегшувало симптоми шляхом обмеження розмноження патогенної кишкової флори та зниження вироблення бактеріями водню/метану; покращення об’єму калових мас завдяки зменшенню бактеріальної деградації клітковини зменшувало біль і прискорювало кишковий транзит, усуваючи закрепи. Метааналіз показав, що однорічний курс лікування рифаксиміном у дозі 400 мг двічі на добу 7 днів щомісяця в поєднанні з клітковиною забезпечував відсутність симптомів у 64,0% пацієнтів порівняно з 34,9% у групі, яку лікували лише клітковиною (Bianchi et al., 2011). Ретроспективне дослідження також підтвердило ефективність циклічного застосування рифаксиміну: 47,2% пацієнтів не мали болю протягом 3 місяців (De Bastiani et al., 2021). Ґрунтуючись на таких доказах, клінічні настанови Італійського товариства гастроентерології 2017 року та Польського міждисциплінарного консенсусу 2015 року рекомендують застосування рифаксиміну для лікування пацієнтів з СНДХ.
Користь від рифаксиміну в пацієнтів з СНДХ полягає не лише в полегшенні симптомів, а й охоплює первинну та вторинну профілактику гострого дивертикуліту. Метааналіз показав статистично значуще зниження частоти дивертикуліту на 2% у пацієнтів, які отримували рифаксимін у дозі 400 мг двічі на добу 7 днів щомісяця впродовж 1 року разом із клітковиною порівняно лише з клітковиною (Bianchi et al., 2011). Інший метааналіз підтвердив, що циклічне призначення рифаксиміну по 800 мг на добу 7-10 днів щомісяця знижує ризик виникнення дивертикуліту на 1,9%, а ризик рецидиву – на 24% (Koch et al., 2023).
Дані щодо профілактики рецидивів гострого дивертикуліту суперечливі: низка досліджень не підтверджує ефективності, інші демонструють потенційні переваги рифаксиміну. З патофізіологічного погляду застосування видається обґрунтованим, але, щоб остаточно підтвердити чи спростувати ефективність, доказів недостатньо. Наразі настанови Американської гастроентерологічної асоціації 2021 року не рекомендують рифаксимін для профілактики гострого дивертикуліту.
Синдром надмірного бактеріального росту
Синдром НБР характеризується надмірною кількістю бактерій, що спричиняє здуття, діарею та мальабсорбцію. Діагноз ґрунтується на клінічних симптомах і підтверджується дихальними тестами чи культурами аспірату з тонкої кишки. Зазвичай переважають факультативні анаероби й бактерії, зокрема Proteobacteria, які практично не трапляються в здоровій тонкій кишці. Це призводить до декон’югації жовчних кислот, порушення всмоктування жирів і запалення слизової оболонки.
Завдяки широкому спектру дії та мінімальній системній абсорбції рифаксимін є ефективним засобом лікування СНБР. Метааналіз показав успішність ерадикаційної терапії рифаксиміном у 70,8% випадків СНБР (Gatta, Scarpignato, 2017). Зазвичай застосовують дозу 550 мг тричі на добу 14 днів. Препарат знижує бактеріальне навантаження без значних побічних ефектів і може використовуватися емпірично, а також повторно, якщо симптоми хронічні.
Існує дискусія щодо зв’язку СНБР і СПК, особливо СПК-Д. Пацієнти з СПК мають вищу частоту СНБР (відношення шансів 3,7; 95% ДІ 2,3-6,0), але близько 20% здорових осіб також можуть мати позитивні тести на СНБР, що ускладнює інтерпретацію. Ранні дослідження з використанням водневих дихальних тестів виявили асоціацію, проте нині вважається, що ці тести більше відображають час транзиту й активність бактерій у товстій кишці. Докази свідчать, що СНБР не є основною причиною СПК. Усунення СНБР не завжди зменшує симптоми СПК, а лікування СНБР зазвичай поступається стандартним методам лікування СПК антидепресантами та спазмолітиками. Крім того, ситуацію ускладнюють додаткові чинники, зокрема застосування інгібіторів протонної помпи, які спричиняють СНБР і мають схожі побічні ефекти. Отже, бактерії можуть частково пояснювати симптоми СПК, але прямий причинний зв’язок між СПК і СНБР не доведений.
Діарея мандрівників (ДМ)
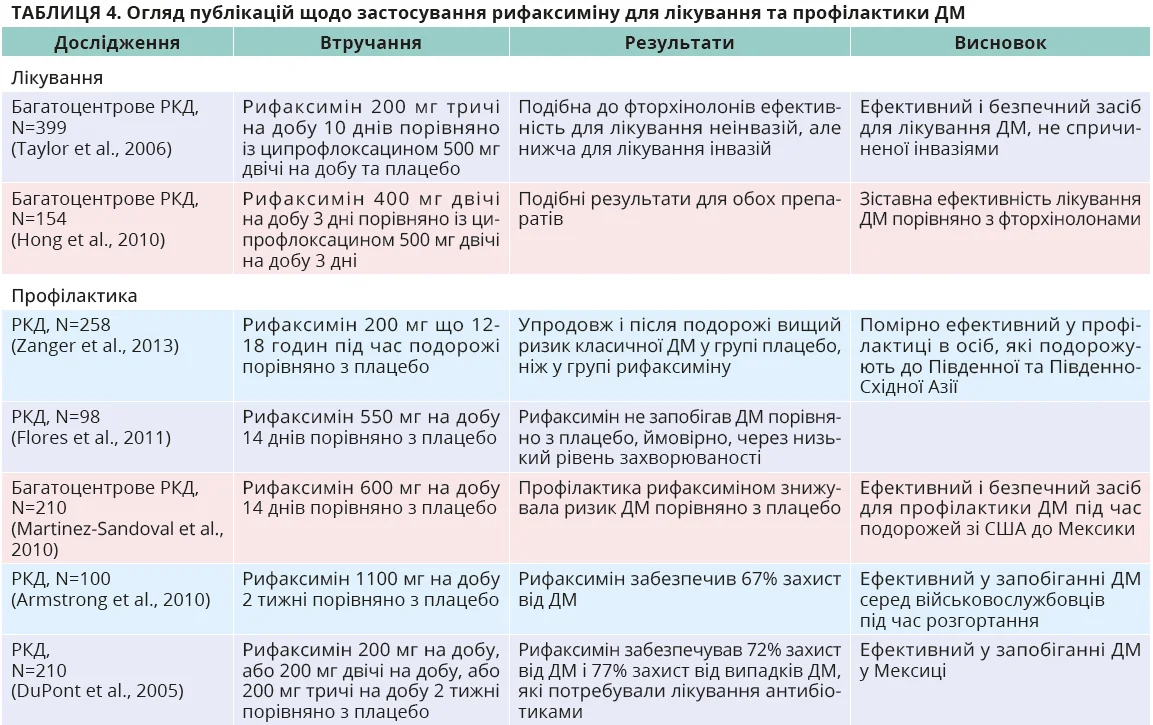
ДМ – поширений стан, який виникає після вживання забрудненої їжі чи води, найчастіше зумовлений ентеротоксигенною кишковою паличкою. Характеризується надмірним ростом патогенних бактерій у кишківнику, що спричиняє нудоту, діарею та спастичний біль у животі. Дисбіоз погіршує перебіг хвороби та сповільнює процес одужання. Хоча більшість випадків є самообмежувальними, антибіотики здатні скоротити тривалість ДМ. Через ризик антибіотикорезистентності їх рекомендується застосовувати лише у випадках, коли діарея зумовлює дискомфорт, заважає запланованим заходам або цілком унеможливлює діяльність, супроводжується появою кров’янистих виділень, а також у пацієнтів з високим ризиком тяжкого перебігу (наприклад, імунокомпрометованих осіб). Рифаксимін є ефективним і безпечним варіантом лікування недизентерійних випадків ДМ, які становлять більшість. Дослідження показують, що рифаксимін може скоротити тривалість діареї та зменшити тяжкість симптомів (табл. 4).
Для профілактики гострого гастроентериту під час подорожей важливо ретельно мити руки, вживати добре термічно оброблену їжу, пити бутильовану або очищену воду, уникати напоїв з льодом. Протимікробна профілактика зазвичай не рекомендується, крім випадків високого ризику: люди з клінічно значущими хворобами внаслідок кишкових інфекцій (реактивні артрити) чи тяжкими хронічними хворобами з ризиком ускладнень унаслідок ДМ. У таких ситуаціях препаратом першого вибору є рифаксимін, хоча тривалість і дозування залишаються невизначеними.
Подорожі часто супроводжуються стресом, зміною харчування та ризиком інфекцій, що провокує загострення симптомів СПК. Профілактика ДМ в осіб з СПК є складною та суперечливою: потрібно зважати на користь антибіотиків і ризики резистентності й ускладнень. Тому стратегії профілактики мають бути індивідуалізованими.
Печінкова енцефалопатія
ПЕ – нейропсихіатричний синдром, пов’язаний з дисфункцією печінки, що характеризується когнітивними порушеннями та змінами свідомості, аж до коми. Патогенез ПЕ складний. Унаслідок гепатоцелюлярної дисфункції знижується здатність метаболізувати токсини й азотисті сполуки з кишково-печінкового кровообігу, утворені кишковою мікрофлорою. Роль кишкової мікробіоти реалізується також через вісь «кишківник – печінка – мозок». У пацієнтів із цирозом печінки спостерігається надмірний ріст шкідливих бактерій родини Enterobacteriaceae, що виробляють аміак, з одночасним зменшенням корисних бактерій з родин Lachnospiraceae та Ruminococcaceae (тип Firmicutes), які відіграють ключову роль у підтриманні цілісності кишкового бар’єра. Такий дисбаланс посилює кишкову проникність і системну абсорбцію нейротоксинів.
Клінічні настанови щодо ведення печінкової енцефалопатії Європейської асоціації з вивчення печінки (2022) рекомендують обов’язкове призначення лактулози пацієнтам з першим епізодом ПЕ для вторинної профілактики, а також рифаксимін (Journal of Hepatology. 2022; 77(3): 807-24). Рифаксимін ефективно запобігає рецидиву ПЕ, зменшуючи вироблення та всмоктування аміаку й інших токсинів у кишківнику. Було встановлено, що в комбінації з лактулозою рифаксимін сприяє значущому зниженню ризику рецидиву ПЕ та госпіталізацій через ПЕ порівняно з монотерапією лактулозою (Bass et al., 2010). Рекомендована доза рифаксиміну пацієнтам з ПЕ – 550 мг двічі на добу, вона добре переноситься та підходить для довготривалого лікування. Безпека й ефективність препарату обґрунтовують його включення до клінічних рекомендацій щодо лікування ПЕ, особливо для пацієнтів з рецидивами ПЕ в анамнезі.
Крім того, рифаксимін продемонстрував користь у пацієнтів із цирозом печінки та його ускладненнями, а також у пацієнтів зі стеатотичною хворобою печінки, асоційованою з метаболічною дисфункцією (СХПМД). У разі цирозу рифаксимін значно знижував портальний тиск шляхом зменшення бактеріальної транслокації та запальних реакцій і рівень ендотоксинів у плазмі крові; покращував виживаність без трансплантації в декомпенсованих випадках. Рифаксимін почали широко застосовувати при спонтанному бактеріальному перитоніті (СБП) через появу полірезистентних мікробів, нечутливих до більшості антибіотиків, зокрема норфлоксацину. Рифаксимін виявився ефективнішим за норфлоксацин у вторинній профілактиці СПБ: частота рецидивів – 3,88 проти 14,13%; рівень смертності – 13,74 проти 24,43% (Elfert et al., 2016). При рефрактерному асциті рифаксимін у комбінації з мідодрином покращував циркуляцію й функцію нирок, подовжуючи період виживання пацієнтів (Hanafy et al., 2016). Рифаксимін продемонстрував ефективність для вторинної профілактики кровотечі з варикозних вен: нижчий ризик повторної кровотечі та ПЕ в пацієнтів, які продовжували приймати рифаксимін після виписки зі стаціонару (Zubieta-Rodeíguez et al., 2017). У разі СХПМД рифаксимін знижує запалення, ендотоксини й метаболічні маркери, але його довготривала ефективність потребує подальшого вивчення.
Інфекція Clostridioides difficile
С. difficile – грампозитивна анаеробна паличка, що утворює спори й виробляє токсин. Прояви інфекції коливаються від легкої діареї до загрозливого для життя коліту. Зазвичай виникає внаслідок дисбіозу через застосування антибіотиків широкого спектра дії. Здебільшого в таких випадках зменшується кількість корисних бактерій (Firmicutes, Actinobacteria) та збільшується кількість патогенних видів протеобактерій.
Лікування початкового епізоду інфекції C. difficile включає антибіотики – фідаксоміцин, ванкоміцин або метронідазол. Рифаксимін продемонстрував особливу ефективність у разі рецидивів інфекції завдяки здатності пригнічувати C. difficile, не впливаючи на корисну мікробіоту. Пілотне дослідження показало зниження повторної діареї в пацієнтів, які приймали рифаксимін після стандартної терапії (Garey et al., 2011). На сьогодні лише одне дослідження вивчало рифаксимін як терапію першої лінії інфекції C. difficile в дітей із ЗЗК; у цій особливій популяції рифаксимін не показав істотної різниці щодо рівнів вилікування та рецидивів порівняно з метронідазолом (Gawronska et al., 2017). Отже, щоб рекомендувати його як лікування першої лінії, наразі доказів недостатньо.
Ефективність рифаксиміну в дозі 400 мг тричі на добу протягом 14 днів, потім 200 мг тричі на добу ще 14 днів для вторинної профілактики інфекції C. difficile після стандартної терапії (ванкоміцин або метронідазол) вивчали в РКД порівняно з плацебо. Частота рецидиву протягом 12 тижнів становила 29,5% у групі плацебо та 15,9% у групі рифаксиміну (різниця 13,7%; 95% ДІ від -28,1 до 0,7%; p=0,06). Автори дійшли висновку, що рифаксимін може знизити ризик рецидиву, але ДІ не виключає можливості відсутності ефекту (Major et al., 2019).
Отже, рифаксимін продемонстрував багатонадійні результати щодо лікування та профілактики інфекції C. difficile, але рекомендації в різних настановах суперечливі. Зокрема, клінічні рекомендації Американської колегії гастроентерологів 2021 року визнають ефективність рифаксиміну, але не радять його рутинного використання. Натомість настанови Товариства інфекційних хвороб Америки та Товариства епідеміології охорони здоров’я Америки 2021 року, а також Європейського товариства клінічної мікробіології й інфекційних хвороб 2021 року рекомендують його використання як додаткову терапію в пацієнтів із множинними рецидивами після стандартної антибіотикотерапії.
Запальні захворювання кишківника
ЗЗК включають хворобу Крона та виразковий коліт і характеризуються хронічним запаленням. Ключову роль у патогенезі ЗЗК відіграє мікробіота. Хвороба Крона асоціюється з генетичними поліморфізмами, які впливають на вроджену імунну відповідь і функцію клітин Панета, що є критично важливими для мікробного захисту. Генетичні чинники можуть зумовлювати хронічне запалення, запускаючи імунні реакції в схильних осіб. У разі хвороби Крона збільшується кількість Campylobacter concisus й Escherichia coli, але зменшується кількість коменсальних протизапальних бактерій, як-от Faecalibacterium prausnitzii. Ймовірно, Fusobacterium varium може спричиняти розвиток виразкового коліту. Крім того, добре відомо, що пацієнти із ЗЗК часто страждають на СПК. Незважаючи на потенційну роль дисбіозу в патогенезі ЗЗК, спроби впливу на кишкову мікробіоту дали суперечливі результати (табл. 5).
Запалення клубової кишені (резервуару) – це запальне ускладнення, що виникає після накладання ілеоанального анастомозу з формуванням резервуару при ВК приблизно в половини випадків упродовж 10 років. Симптоми охоплюють біль у животі, збільшення кількості випорожнень і терміновість дефекації. У таких пацієнтів часто виникає антибіотикозалежна форма хвороби, яка потребує довготривалої антибіотикотерапії для підтримання ремісії. Хвороба вважається хронічною, якщо симптоми тривають понад 4 тижні. Рифаксимін виявився ефективним у лікуванні запалення клубової кишені. Відкрите когортне дослідження показало підтримання ремісії в 65% пацієнтів через 3 місяці лікування рифаксиміном зі збереженням ефективності через 6 і 12 місяців (Shen et al., 2008). Європейський консенсус 2008 року щодо ведення виразкового коліту в особливих ситуаціях рекомендує рифаксимін у дозі 2 г на добу протягом 4 тижнів як альтернативне лікування хронічного запалення клубової кишені, підкреслюючи його ефективність у контролі симптомів і підтриманні ремісії.
ВИСНОВКИ
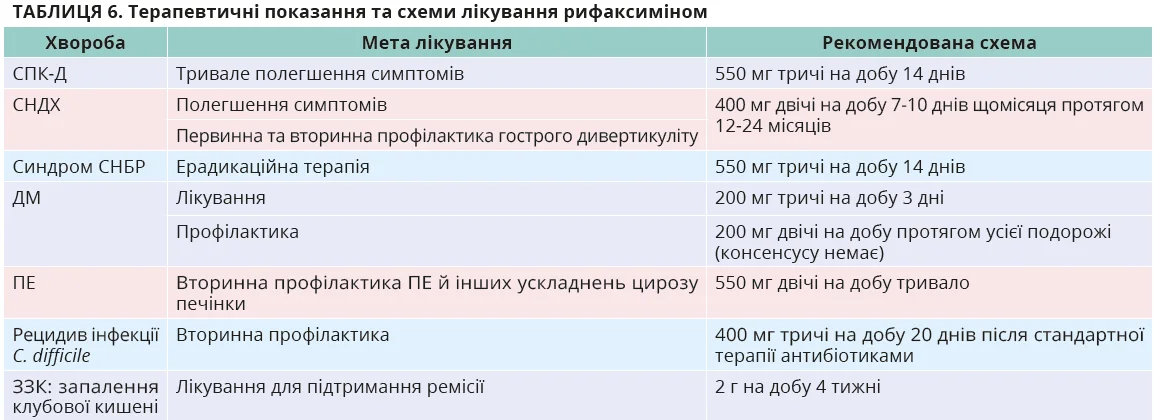
Завдяки модулювальній дії з мінімальним ризиком побічних ефектів рифаксимін є цінним препаратом для лікування низки захворювань травного тракту, патогенетично пов’язаних з дисбіозом кишківника. Зважаючи на значну поширеність цієї патології, гастроентерологам украй важливо знати, коли, як і кому призначати лікування рифаксиміном (табл. 6).
Література
Frias J., Martins M., Peixoto A., Macedo G. Rifaximin as a therapeutic ally in the modulation of dysbiosis: a narrative review of its applicability in gastrointestinal disorders. GE Port. J. Gastroenterol. 2025 Apr 21; 32 (6): 423-437. doi: 10.1159/000545926.
Повний список літератури знаходиться в редакції.