Системне запалення при МАСХП: прихований механізм мультиорганного пошкодження в умовах коморбідності
 Автор: Олександра Юріївна ФІЛІППОВА, докторка медичних наук, професорка, кафедра внутрішньої медицини 2, фтизіатрії, професійних хвороб і клінічної імунології Дніпровського державного медичного університету
Автор: Олександра Юріївна ФІЛІППОВА, докторка медичних наук, професорка, кафедра внутрішньої медицини 2, фтизіатрії, професійних хвороб і клінічної імунології Дніпровського державного медичного університету
Нині розуміння метаболічно-асоційованої стеатотичної хвороби печінки (МАСХП) виходить за межі ізольованого стеатозу: в центрі патологічних змін розглядають системне низькоінтенсивне запалення (СНЗ) та мітохондріальну дисфункцію, які визначають прогресування хвороби й терапевтичні стратегії.
Тактика ведення пацієнта з МАСХП формується послідовно, від пошуку відповіді на запитання «Чому це важливо?» до «Що потрібно призначити?». Саме тому в цій статті представлено відповіді на найпоширеніші клінічні запитання з огляду на дані доказової медицини.
Чому МАСХП сьогодні розглядають як одну з ключових хвороб, що визначатимуть структуру хронічної патології найближчими десятиліттями?
Масштаб поширення МАСХП і її системні наслідки роблять це захворювання однією із центральних проблем сучасної медицини. За прогнозами, 2040 року глобальна поширеність МАСХП становитиме 55,7% [8]. Разом з тим сучасна концепція МАСХП вийшла за межі ізольованої печінкової патології.
Доведено, що це захворювання тісно пов’язане з ожирінням, інсулінорезистентністю (ІР), артеріальною гіпертензією, атерогенною дисліпідемією, формуючи спільний кардіометаболічний континуум. У цих умовах печінка стає джерелом СНЗ, яке впливає на ендотелій судин, міокард, нирки й інші органи [12]. Перебіг МАСХП супроводжується високим ризиком розвитку серцево-судинних подій, цукрового діабету (ЦД) 2-го типу, прогресування фіброзу печінки, виникнення гепатоцелюлярної карциноми [11] та зростанням загальної смертності. Нині МАСХП вважають маркером системної метаболічної дисфункції й одним із ключових чинників формування сучасної коморбідності.
Які механізми лежать в основі розвитку СНЗ при МАСХП? Які фактори запускають цей процес?
СНЗ при МАСХП формується внаслідок взаємодії різноманітних факторів, які діють водночас і підсилюють один одного. Надлишкове калорійне харчування, гіпокінезія, психосоціальний стрес, інфекційні чинники, дисбіоз кишківника, генетичні особливості імунної відповіді, куріння, алкоголь у поєднанні з ожирінням та ІР створюють метаболічне середовище, в якому запускається хронічне СНЗ.
Ключовою ланкою виникнення СНЗ при МАСХП є запалення жирової тканини. Гіпертрофовані адипоцити активують макрофаги та змінюють профіль адипокінів: зростає вивільнення прозапальних адипокінів (лептин, резистин) і знижується вміст захисного адипонектину [5]. Зазначені зміни стимулюють ІР і надходження вільних жирних кислот до печінки. Їхній надлишок спричиняє ліпотоксичність, оксидативний стрес у гепатоцитах, активацію клітин Купфера з подальшим NF-κB-залежним виробленням прозапальних цитокінів. Додатковим тригером є підвищена проникність кишкового бар’єра: бактеріальні продукти потрапляють у печінку через ворітну вену, значно посилюючи запальну відповідь. У результаті формується хибне коло, в якому метаболічна дисфункція та СНЗ взаємно потенціюють одне одного, зумовлюючи мультиорганні зміни [15].
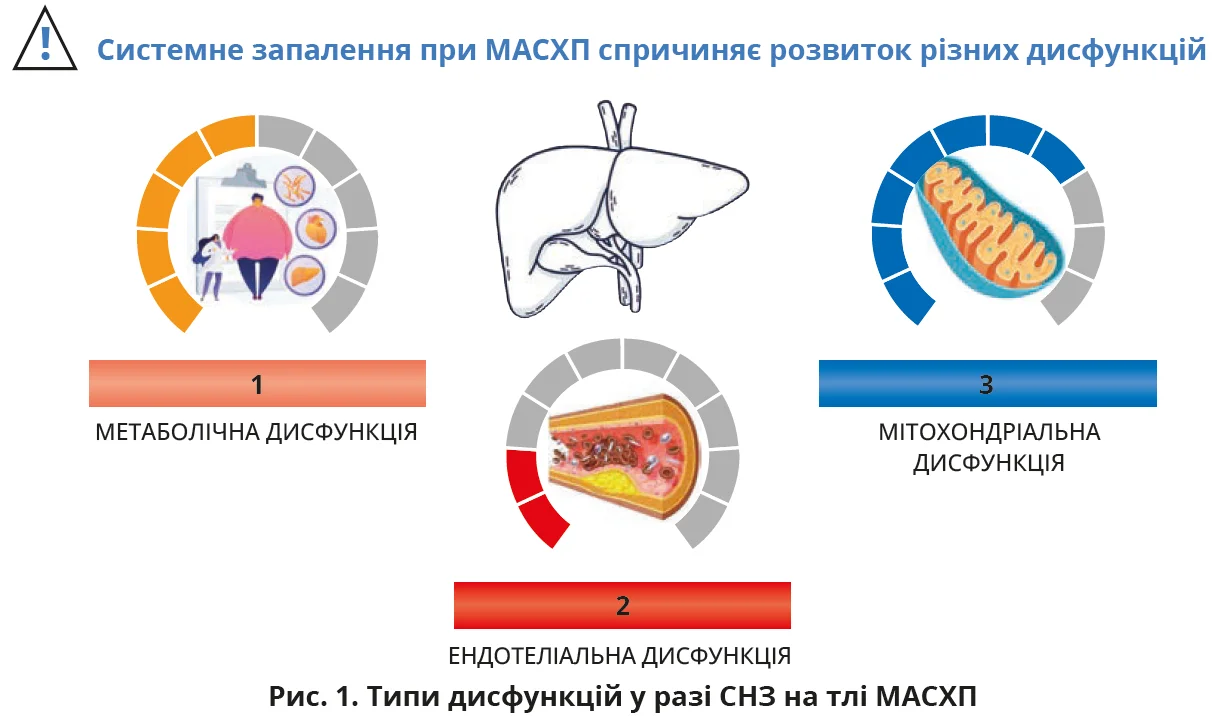
Які типи дисфункцій формуються при СНЗ на тлі МАСХП? Чому це важливо?
СНЗ при МАСХП спричиняє розвиток трьох взаємопов’язаних типів дисфункцій – метаболічної, ендотеліальної та мітохондріальної (рис. 1). Вони формують єдиний патогенетичний континуум і взаємно підсилюють одна одну. Метаболічна дисфункція проявляється посиленням ІР, порушенням ліпідно-вуглеводного гомеостазу; ендотеліальна – зниженням біодоступності оксиду азоту, формуванням проатерогенного фенотипу. Ключовою ланкою цього каскаду є мітохондріальна дисфункція.
Перевантаження печінки вільними жирними кислотами при МАСХП призводить до надмірної активації β-окислення [10]. Коли потік жирів перевищує компенсаторні можливості клітини, зростає вироблення активних форм кисню (АФК), виникає оксидативний стрес. Пошкоджені мітохондрії вивільняють мітохондріальну ДНК у цитозоль клітини, активуючи NLRP3-інфламосоми та посилюючи вивільнення прозапальних цитокінів. Водночас фактор некрозу пухлин-α (ФНП-α) й інтерлейкін-6 (ІЛ-6) порушують роботу дихального ланцюга, знижують синтез аденозинтрифосфату (АТФ) і пригнічують мітохондріальний біогенез. Порушення мітофагії підтримує накопичення пошкоджених мітохондрій, які продовжують генерувати вільні радикали та підтримують хронічне СНЗ. Отже, мітохондріальна дисфункція є не лише наслідком, а й тригером СНЗ, формуючи замкнене коло енергетичного виснаження клітин і прогресування хвороби.
Чому СНЗ при МАСХП має принципове клінічне значення?
СНЗ при МАСХП є своєрідним патогенетичним містком, який поєднує локальне ураження печінки з мультиорганною дисфункцією та визначає довгостроковий прогноз. На рівні печінки хронічне СНЗ спричиняє трансформацію простого стеатозу в стеатогепатит з подальшим прогресуванням фіброзу та цирозу. На системному рівні СНЗ індукує ендотеліальну дисфункцію, прискорює атеросклероз і підвищує серцево-судинний ризик [16]. Системне запалення при МАСХП підвищує ризик розвитку ЦД 2-го типу, артеріальної гіпертензії та серцево-
судинних катастроф (інфарктів, інсультів) [11]. Тривале персистування СНЗ формує проонкогенне мікросередовище, що створює умови для розвитку раку печінки.
Які лабораторні маркери відображають СНЗ при МАСХП?
Системний характер запального процесу при МАСХП підтверджується змінами низки лабораторних показників. До ключових маркерів належить підвищення рівня високочутливого С-реактивного білка (СРБ) як білка гострої фази. Спостерігається зростання концентрації прозапальних цитокінів (ІЛ-6, ФНП-α, ІЛ-1β), що відображає активацію вродженого імунітету. У клінічній практиці додаткову інформацію можуть надавати інтегральні гематологічні індекси (нейтрофільно-лімфоцитарне співвідношення, системний індекс імунного запалення), а також підвищення феритину, гаптоглобіну та пентраксину-3.
Водночас дослідження, проведені за участю хворих на МАСХП, свідчать, що запальні маркери (IЛ-6, ФНП-α, СРБ) тісніше корелюють з показниками метаболічної дисфункції, ніж зі ступенем фіброзу печінки, що обмежує їх використання як сурогатних маркерів фіброзу на ранніх стадіях МАСХП. Їхня клінічна цінність полягає у відображенні системного запального тла та кардіометаболічного ризику. Виявлення СНЗ має не лише діагностичне, а й терапевтичне значення, оскільки саме ця ланка стає ключовою мішенню лікування МАСХП.
Які основні принципи алгоритму лікування МАСХП, якщо враховувати головний патогенетичний чинник – СНЗ?
Алгоритм лікування МАСХП з огляду на роль СНЗ ґрунтується на інтегрованому підході «печінка – метаболізм – судини» та передбачає усунення метаболічного перенавантаження як першопричини запального каскаду. Він охоплює декілька взаємопов’язаних напрямів терапії. Базисом залишається модифікація способу життя [17]. Зниження маси тіла на ≥7-10% асоціюється з регресом стеатогепатиту та зменшенням умісту прозапальних цитокінів. Рекомендовано середземноморський тип харчування, обмеження швидких вуглеводів і фруктози, регулярні аеробні та силові фізичні навантаження не менш ніж 150 хвилин на тиждень [17].
Другим напрямом є корекція ІР як метаболічного компонента МАСХП. Із цієї метою використовують піоглітазон (активує PPAR-γ, зменшує вихід жирних кислот із жирової тканини та пригнічує системне запалення), агоністи рецепторів глюкагоноподібного пептиду-1 (сприяють зниженню маси тіла, покращують функцію ендотелію та чинять пряму протизапальну дію на печінку) [17]. Наступний напрям – контроль серцево-судинного ризику – заснований на корекції дисліпідемії за допомогою статинів
і лікування артеріальної гіпертензії переважно шляхом призначення препаратів, що блокують ренінангіотензинову систему.
Ще одним важливим і клінічно значущим напрямом є гепатопротекція з протизапальним ефектом – сфера, в якій адеметіонін (SAMe) має переконливі переваги завдяки своїм багатофакторним механізмам дії, зокрема здатності відновлювати рівень глутатіону, необхідного для повноцінного функціонування мітохондрій.
Комплексний підхід до лікування МАСХП дає змогу впливати одночасно на печінкові, метаболічні й судинні механізми виникнення хвороби та зменшувати СНЗ, яке лежить в основі її прогресування.
Яке патогенетичне обґрунтування застосування SAMe при МАСХП?
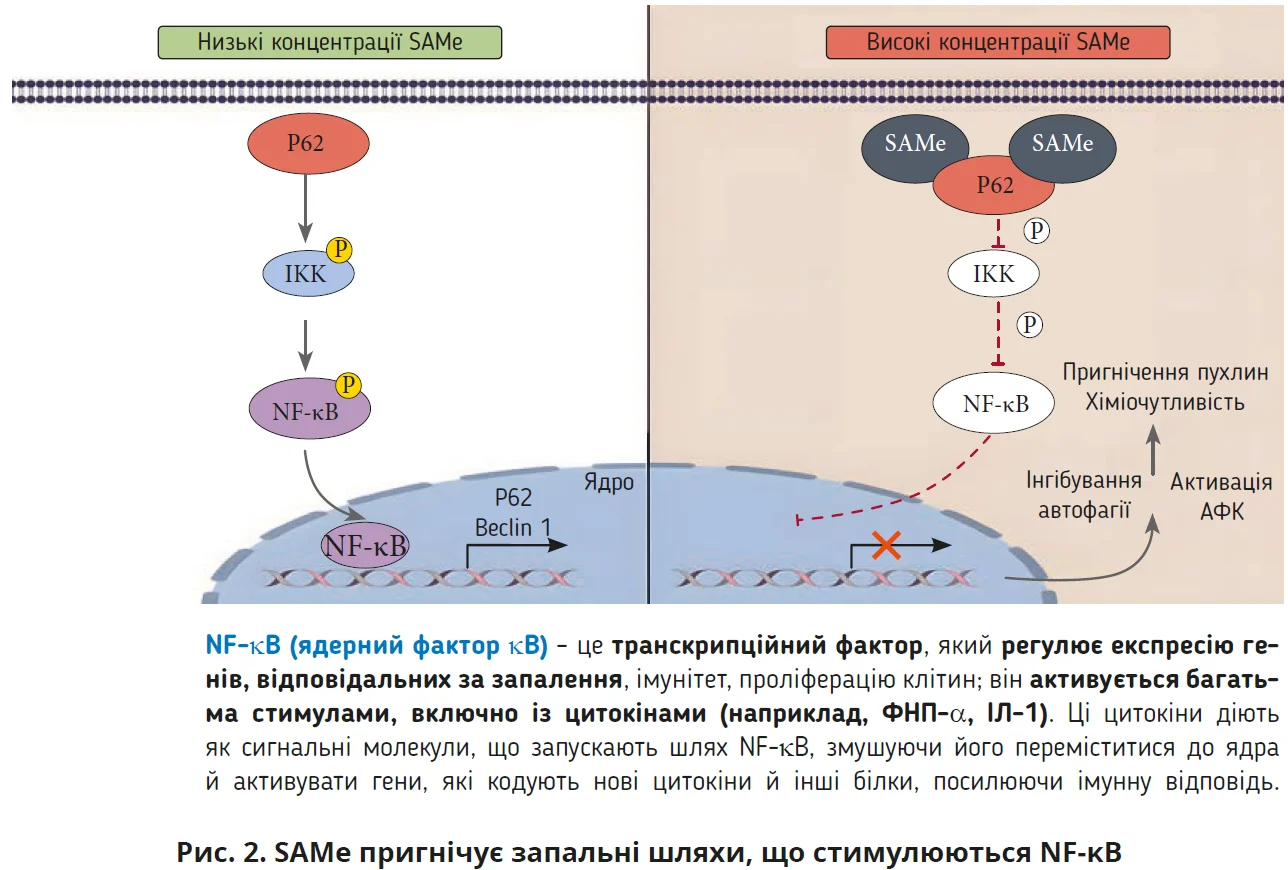
Патогенетичне обґрунтування застосування SAMe при МАСХП полягає в його здатності впливати на ключові ланки патогенезу – СНЗ і мітохондріальну дисфункцію. SAMe є ключовим донором метильних груп, завдяки чому він бере участь у реакціях трансметилювання, що регулюють експресію генів запальної відповіді: впливаючи на NF-κB-залежні сигнальні шляхи, він зменшує синтез прозапальних цитокінів (рис. 2) [7].
Водночас SAMе запобігає пошкодженню мітохондрій, спричиненому АФК. SAMe відновлює рівень глутатіону – ключового внутрішньоклітинного антиоксиданту; така особливість дії сприяє зниженню оксидативного стресу та захисту мітохондрій від ушкодження реактивними формами кисню.
Крім того, SAMе бере участь у синтезі фосфатидилхоліну, підтримуючи тим самим плинність мітохондріальних мембран, що необхідно для нормальної роботи дихального ланцюга та запобігання відкриттю мітохондріальної пори, яка запускає апоптоз клітини [6]. Отже, SAMе впливає на ключові механізми прогресування МАСХП, що обґрунтовує його використання як компонента комплексної терапії.
В Україні оригінальний препарат SAMе представлений під торговою назвою Гептрал® і має як показання внутрішньопечінковий холестаз (ВПХ) у дорослих, у тому числі у хворих на хронічний гепатит різної етіології та цироз печінки; ВПХ у вагітних.
Які клінічні дані підтверджують ефективність SAMе у пацієнтів з метаболічно-асоційованим стеатогепатитом (МАСГ)?
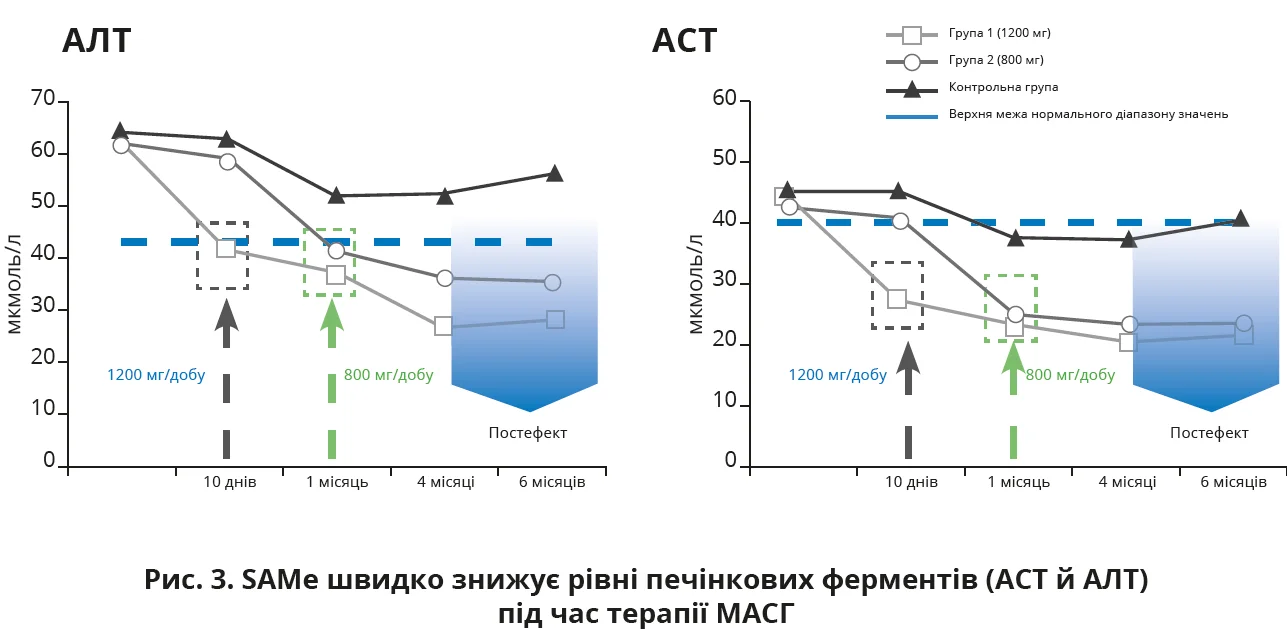
Ефективність SAMe при МАСГ продемонстровано в проспективному дослідженні, в якому 90 пацієнтів з неалкогольним стеатогепатитом / МАСГ були рандомізовані на три групи: приймання SAMе (Гептрал®) у дозі 1200 мг/добу, 800 мг/добу або відсутність фармакотерапії [2].
Лікування тривало 4 місяці, 84 пацієнти завершили дослідження. Уже на ранніх етапах терапії спостерігався швидкий біохімічний ефект у групі Гептрал®: рівні аланінамінотрансферази (АЛТ) й аспартатамінотрансферази (АСТ) у сироватці крові нормалізувалися більш ніж у 80% пацієнтів протягом перших 10 днів лікування (рис. 3). Дослідники відзначили дозозалежний ефект: швидше зниження показників трансаміназ спостерігали при застосуванні 1200 мг Гептрал® порівняно з дозою 800 мг. Позитивна динаміка показників печінкових ферментів зберігалася й після завершення лікування: поліпшення рівнів АЛТ й АСТ відзначалося протягом щонайменше 2 місяців після припинення терапії.
Які додаткові клінічні переваги SAMе при МАСГ і які ключові ефекти його застосування?
У пацієнтів з МАСГ лікування SAMе супроводжується не лише покращенням біохімічних показників печінки, але й зменшенням гепатогенної втоми як одного із симптомів ВПХ [1]. Тривале 4-місячне приймання SAMе сприяло достовірному зменшенню гепатогенної втоми; цей ефект зберігався щонайменше протягом 2 місяців після припинення лікування, що свідчить про тривалу дію препарату [2].
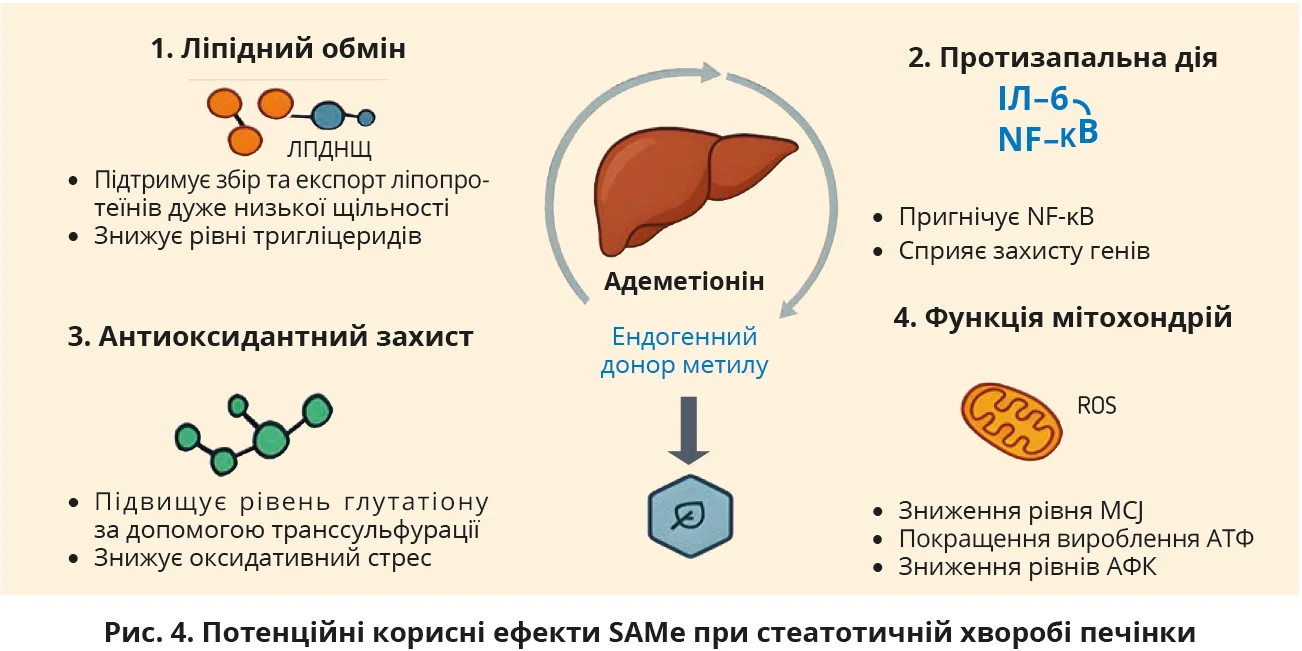
Додаткові ефекти SAMе пов’язані з його участю в регуляції метаболізму ліпідів і антиоксидантного захисту [9]. Як донор метильних груп, він бере участь у синтезі фосфатидилхоліну; це сприяє експорту ліпопротеїнів дуже низької щільності та зменшенню внутрішньопечінкового накопичення тригліцеридів, що важливо для зменшення стеатозу [14]. SAMе відновлює рівень глутатіону, що покращує антиоксидантний захист, зменшення інтенсивності оксидативного стресу [4]. Препарат пригнічує NF-κB-залежні запальні механізми, знижуючи рівень ІЛ-6 та інших прозапальних цитокінів. Покращення мембранної стабільності мітохондрій і синтезу АТФ додатково поліпшує енергетичний статус клітин [3].
У сукупності ці ефекти дають змогу розглядати SAMе (Гептрал®) як компонент комплексної терапії МАСХП, спрямованої на корекцію метаболічних, запальних і енергетичних порушень (рис. 4) [13].
Висновки
МАСХП сьогодні – це не просто локальне накопичення ліпідів у гепатоцитах, а центральний вузол метаболічної дезінтеграції. Ключовим драйвером прогресування хвороби є системне запалення, що нерозривно пов’язане з порушенням мітохондріальної функції. У цьому контексті SAMе виступає не лише як гепатопротектор, а і як стратегічний метаболічний агент. Відновлюючи рівень мітохондріального глутатіону та стабілізуючи мембрани гепатоцитів, він ефективно розриває зв’язок між оксидативним стресом і ендотеліальною дисфункцією, забезпечуючи комплексний захист печінки.
Література
- Anstee Q.M., Day C.P. S-adenosylmethionine (SAMe) therapy in liver disease: a review of current evidence and clinical utility. Journal of Hepatology. 2012; 57 (5): 1097-1109. doi: 10.1016/j.jhep.2012.04.041.
- Baranovsky A.Yu., Raykhelson K.L., Marchenko N.V. S-adenosylmethionine (Heptral®) in treatment of patients with non-alcoholic steatohepatitis. Клінічні перспективи гастроентерології, гепатології. 2010.
- Barbier-Torres L., Chhimwal J., Kim S.Y., et al. S-adenosylmethionine negatively regulates the mitochondrial respiratory chain repressor MCJ in the liver. International Journal of Biological Sciences. 2024; 20 (4): 1218-1237. doi: 10.7150/ijbs.90104.
- Cederbaum A.I. Hepatoprotective effects of S-adenosyl-L-methionine against alcohol and cytochrome P450 2E1 induced liver injury. World Journal of Gastroenterology. 2010; 16 (11): 1366-1376. doi: 10.3748/wjg.v16.i11.1366.
- Eid R.A., Hamed A.M., Elgendy S.O., et al. Associations between systemic inflammatory markers, metabolic dysfunction, and liver fibrosis scores in patients with MASLD. Metabolites. 2025; 16: 25. doi: 10.3390/metabo16010025.
- Goicoechea L., Torres S., Fàbrega L., et al. S-adenosyl-L-methionine restores brain mitochondrial membrane fluidity and GSH content improving Niemann-Pick type C disease. Redox Biology. 2024; 72: 103150. doi: 10.1016/j.redox.2024.103150.
- Jin X., Zhang L., Ying C., et al. S-adenosylmethionine inhibits non-small cell lung cancer and enhances chemosensitivity by targeting the P62/NF-κB axis and regulating autophagy and oxidative stress. Bioorganic Chemistry. 2025; 160: 108509. doi: 10.1016/j.bioorg.2025.108509.
- Le M.H., et al. Forecasted 2040 global prevalence of nonalcoholic fatty liver disease using hierarchical Bayesian approach. Clinical and Molecular Hepatology. 2022; 28 (4): 841-850. doi: 10.3350/cmh.2022.0239.
- Luque Urbano M.R., Fernández Ramos D., Lopitz Otsoa F., et al. S-adenosylmethionine deficit disrupts very low density lipoprotein metabolism promoting liver lipid accumulation in mice. Journal of Lipid Research. 2025; 66 (5): 100794. doi: 10.1016/j.jlr.2025.100794.
- Meroni M., Paolini E., Longo M., et al. Exploring multiorgan mitochondrial dysfunction in the switch toward progressive MASLD in AMLN mice. iScience. 2025; 28 (9): 113449. doi: 10.1016/j.isci.2025.113449.
- Michalopoulou E., Thymis J., Lampsas S., et al. The triad of risk: linking MASLD, cardiovascular disease and type 2 diabetes; from pathophysiology to treatment. Journal of Clinical Medicine. 2025; 14 (2): 428. doi: 10.3390/jcm14020428.
- Mofrad P., et al. Clinical and histologic spectrum of nonalcoholic fatty liver disease associated with normal ALT values. Hepatology. 2003; 37: 1286-1292.
- Mora S.I., García Román J., Gómez Ñáñez I., et al. Chronic liver diseases and the potential use of S-adenosyl-L-methionine as a hepatoprotector. European Journal of Gastroenterology and Hepatology. 2018; 30 (8): 893-900.
- S-adenosylmethionine: a metabolite critical to the regulation of autophagy. PMC. Available at: https://pmc.ncbi.nlm.nih.gov/articles/PMC7653241.
- Sandireddy R., Sakthivel S., Gupta P., et al. Systemic impacts of metabolic dysfunction-associated steatotic liver disease (MASLD) and metabolic dysfunction-associated steatohepatitis (MASH) on heart, muscle, and kidney related diseases. Frontiers in Cell and Developmental Biology. 2024; 12: 1433857. doi: 10.3389/fcell.2024.1433857.
- Solleiro-Villavicencio H., Viurcos-Sanabria R., Aguayo-Guerrero J.A., et al. Inflammation: a key mechanism connecting metabolic-associated steatotic liver disease and systemic arterial hypertension. Frontiers in Immunology. 2025; 16: 1620585. doi: 10.3389/fimmu.2025.1620585.
- Tacke F., Horn P., Wong V.W.-S., et al. EASL–EASD–EASO Clinical Practice Guidelines on the management of metabolic dysfunction-associated steatotic liver disease (MASLD). Journal of Hepatology. 2024. doi: 10.1016/j.jhep.2024.04.031.