Сеульський консенсус – 2025 «Клінічні настанови із синдрому подразненого кишківника»
Переклала й адаптувала канд. мед. наук Тетяна Можина
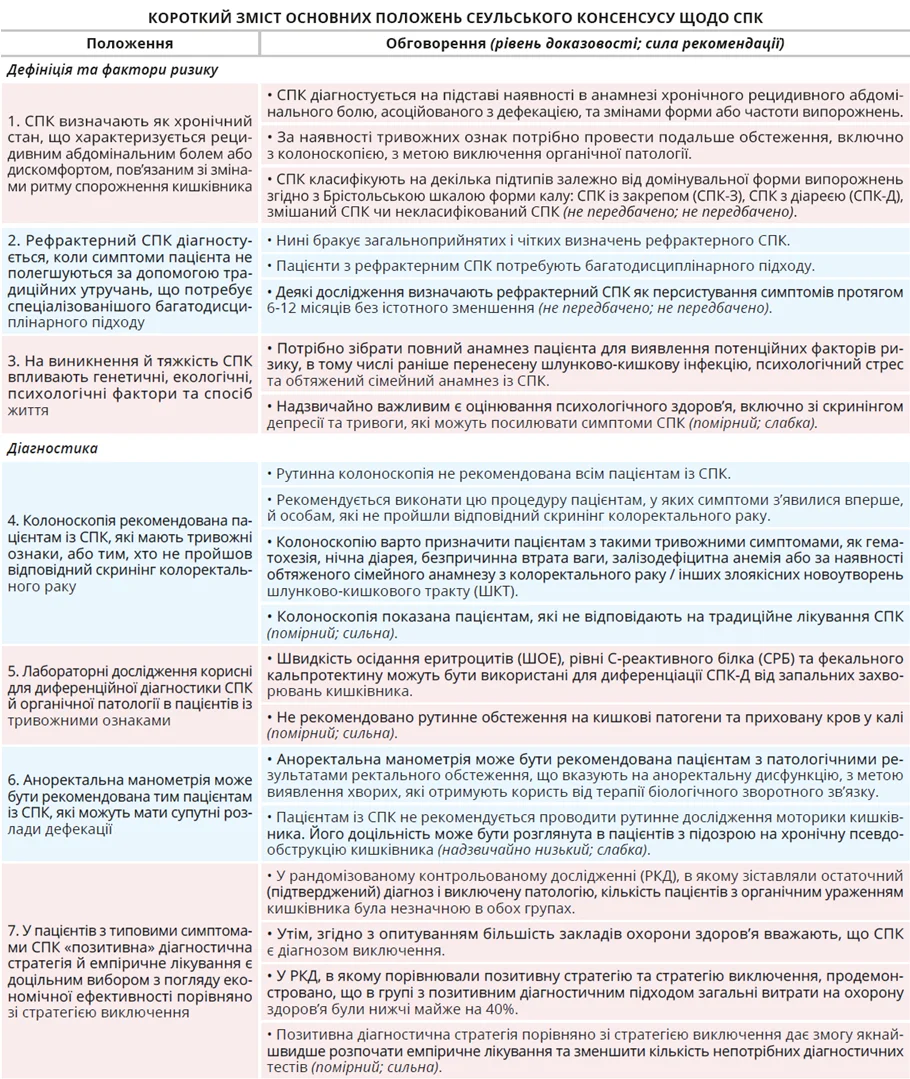
Синдром подразненого кишківника (СПК) є хронічним, іноді інвалідизувальним функціональним захворюванням кишківника [1, 2], яке характеризується періодичним абдомінальним болем, асоційованим з порушенням форми або частоти випорожнень [3]. Згідно з IV Римськими критеріями [4], розробленими багатонаціональною групою експертів з функціональних гастроінтестинальних (ГІ) розладів, СПК діагностується на підставі періодичного абдомінального болю, пов’язаного з дефекацією чи зміною частоти/форми випорожнень. Це поширене функціональне ГІ-захворювання, що чинить істотний вплив на якість життя й соціальне функціонування [1, 2], вражає приблизно 10% загальної популяції в усьому світі [5] та, як повідомляється, знижує якість життя та збільшує соціальні витрати [6]. Патофізіологія СПК остаточно не вивчена [2], тому для нівелювання симптомів і покращення якості життя застосовують різні методи лікування, в тому числі модифікацію способу життя, медикаментозну терапію та психологічну підтримку [6].
Однак терапія часто зосереджується лише на нівелюванні найнеприємніших симптомів і часто є незадовільною [6]. За таких обставин виникає потреба в науково обґрунтованих і систематичних клінічних настановах для зменшення дискомфорту пацієнтів і соціально-економічного тягаря.
Корейське товариство нейрогастроентерології та моторики (KSNM) оновило клінічні настанови з діагностики й лікування СПК, надавши рекомендаціям форму систематизованих настанов і включивши інформацію щодо нових методів лікування. Основною цільовою групою є дорослі пацієнти (≥18 років) з діагностованим або підозрюваним СПК за винятком дітей і осіб зі специфічними станами (наприклад, діарея, спричинена жовчними кислотами). Клінічні настанови розглядають дефініцію, епідеміологію та фактори ризику СПК; доцільність використання й обмеження наявних методів діагностики; доступні способи лікування, включно з модифікацією способу життя, фармако- та психотерапією, разом з їхніми перевагами й недоліками.
Американська колегія гастроентерологів рекомендує якомога швидше розпочати емпіричне лікування з метою зменшення кількості непотрібних діагностичних тестів. Такий спосіб дій відповідає «позитивній» діагностичній стратегії, яка покращує економічну ефективність на відміну від поширеної стратегії виключення [17]. Британські клінічні настанови наполегливо рекомендують лікарям користуватися позитивною стратегією та діагностувати СПК на підставі клінічних ознак за умови відсутності тривожних симптомів і патологічних відхилень у рутинних аналізах крові й калу [16]. У рекомендаціях Європейського товариства нейрогастроентерології та моторики щодо функціональних розладів кишківника з діареєю рекомендується підхід, заснований на аналізі симптомів, порівняно з діагностичною стратегією виключення; водночас мінімальне діагностичне оцінювання є обов’язковим через безліч станів, що спричиняють хронічну діарею [102].
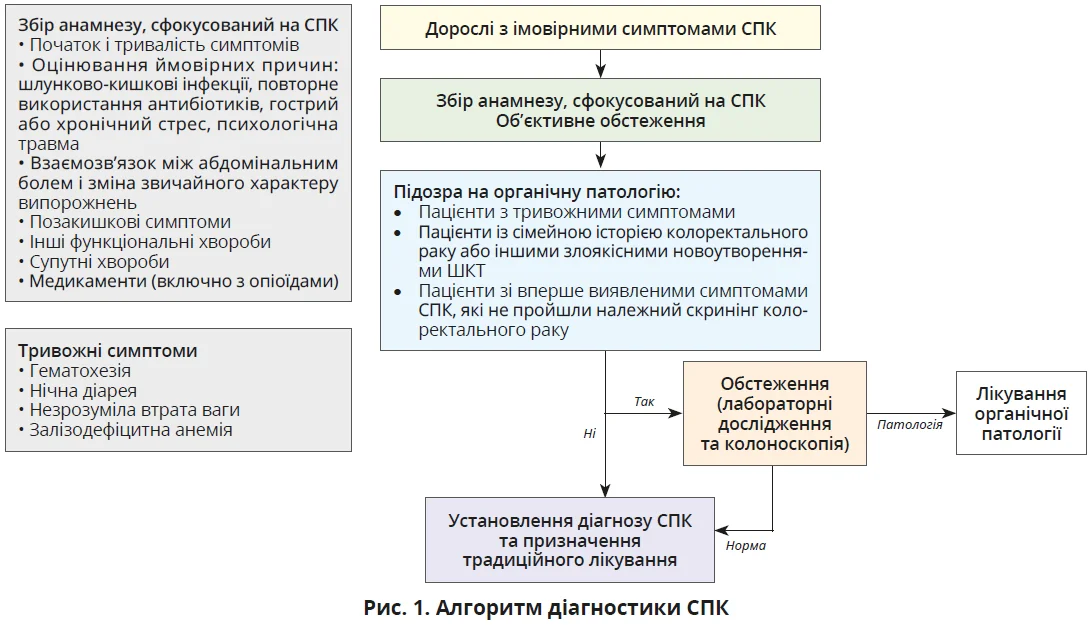
Щоб допомогти лікарям первинної медичної допомоги зрозуміти стандартні методи лікування СПК, Комітет з розроблення клінічних настанов KSNM запропонував клінічний алгоритм діагностики (рис. 1) та лікування (рис. 2) СПК. Спочатку в пацієнтів з підозрою на СПК слід зібрати анамнез, зосередившись на СПК, а потім виконати фізикальне обстеження та базові лабораторні дослідження. Хворим з підозрою на органічну патологію треба провести відповідне обстеження та лікування. Колоноскопія рекомендується пацієнтам із тривожними симптомами, як-от гематохезія, нічна діарея, нез’ясоване зниження ваги або залізодефіцитна анемія, а також пацієнтам з обтяженим сімейним анамнезом щодо злоякісних новоутворень ШКТ, включно з колоректальним раком, а також хворим, які не проходили відповідний колоректальний скринінг, особам зі вперше виниклими симптомами СПК, яким ніколи не виконували колоноскопію. Пацієнтам, які не належать до перелічених категорій, або тим хворим, які отримали нормальні результати колоноскопії, встановлюють діагноз СПК та рекомендують розпочати лікування.
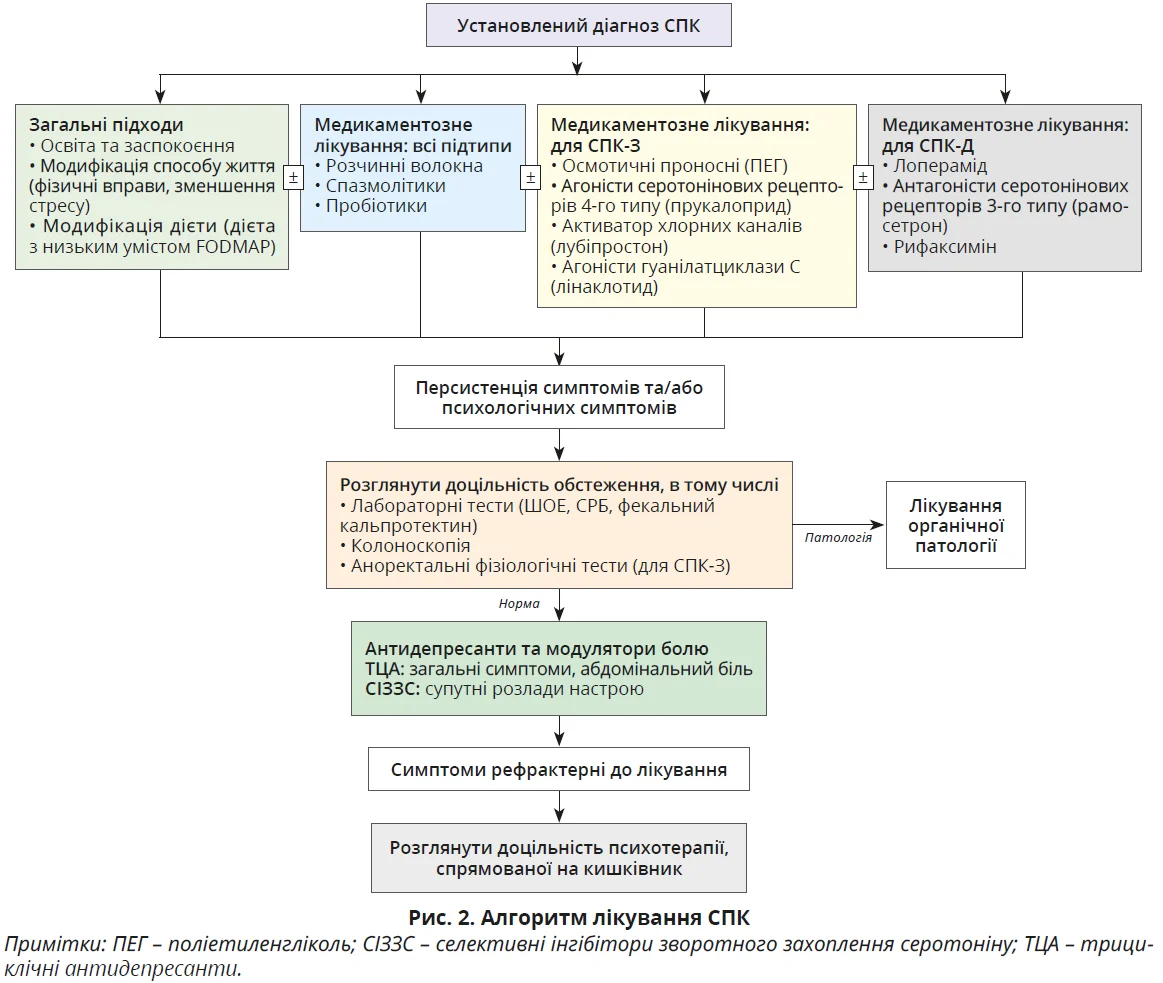
Лікування СПК передбачає першочергове застосування загальних заходів, як-от зміна способу життя та корекція раціону харчування. Згодом можна додати фармакологічне лікування, спрямоване на нівелювання домінувальних симптомів, як-от біль у животі, діарея та закреп. Якщо симптоми не зменшуються на тлі застосування традиційної медикаментозної терапії або якщо пацієнт має супутні психіатричні симптоми, то рекомендується додати психотропні препарати та психотерапію, спрямовану на кишківник, і провести лабораторно-інструментальне обстеження, включно з колоноскопією.
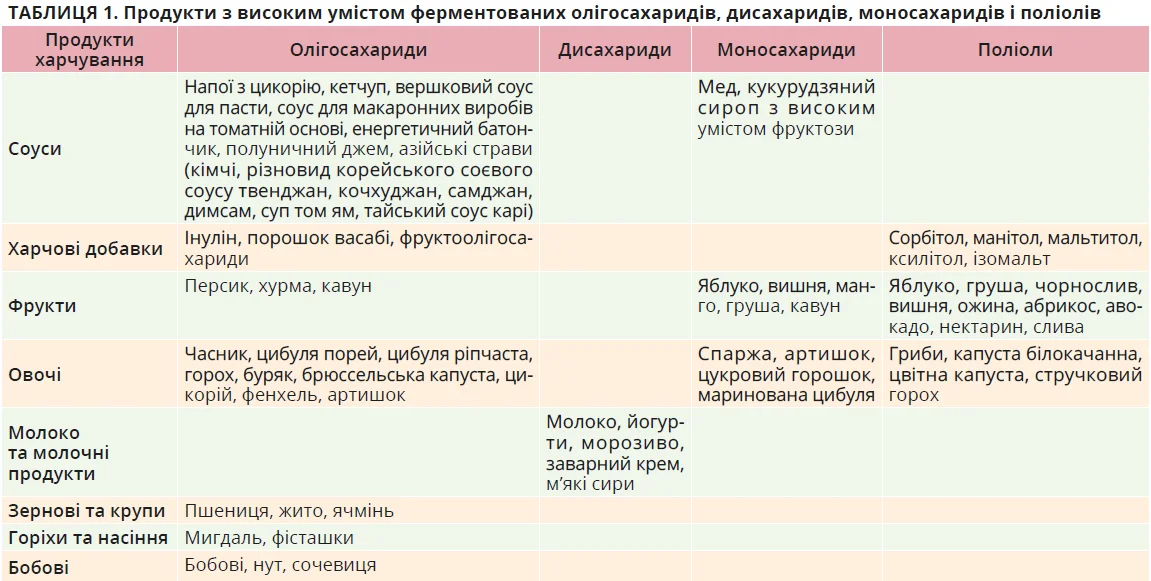
Понад 80% хворих на СПК повідомляють, що виникнення симптомів провокує прийом їжі; понад 60% пацієнтів змінюють раціон харчування з метою лікування СПК [105, 106]. Унаслідок цього дієтотерапію розглядають як ефективний спосіб лікування СПК. Одним з найпоширеніших підходів до корекції раціону є дієта з низьким умістом ферментованих олігосахаридів, дисахаридів, моносахаридів і поліолів (FODMAP) (табл. 1). FODMAP включають коротколанцюгові вуглеводи, які ферментуються кишковими бактеріями та здатні підвищити осмотичний тиск у кишківнику, змінюючи характер випорожнень або спричиняючи газоутворення, що посилює симптоми в пацієнтів із СПК [107].
Дієта з низьким умістом FODMAP асоційована зі значним зменшенням симптомів порівняно з усіма контрольними втручаннями (відношення ризиків 1,51; 95% довірчий інтервал (ДІ) 1,26-1,80). Дієта з низьким умістом FODMAP пов’язана зі значним зниженням значень шкали вираженості симптомів СПК (IBS-SSS; середня різниця −66,2; 95% ДІ від −81,62 до −50,77) на відміну від інших порівняльних показників. Дієта з низьким умістом FODMAP сприяє зменшенню здуття живота, скороченню частоти випорожнень і поліпшенню консистенції випорожнень.
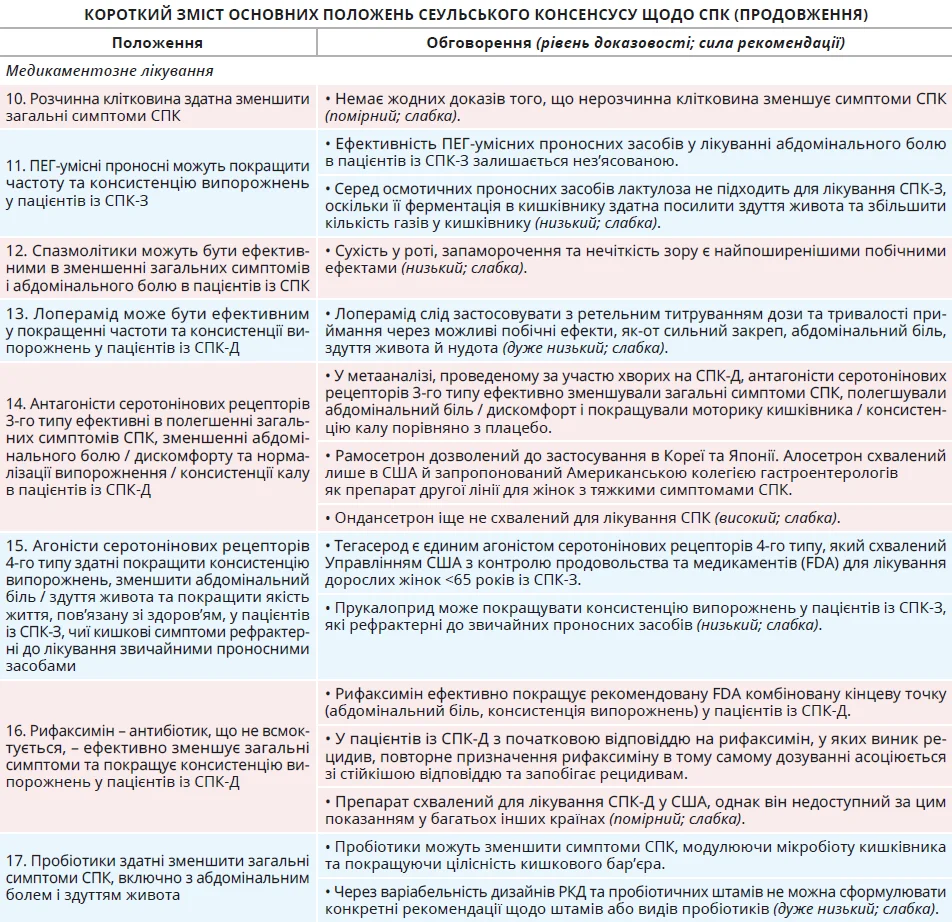
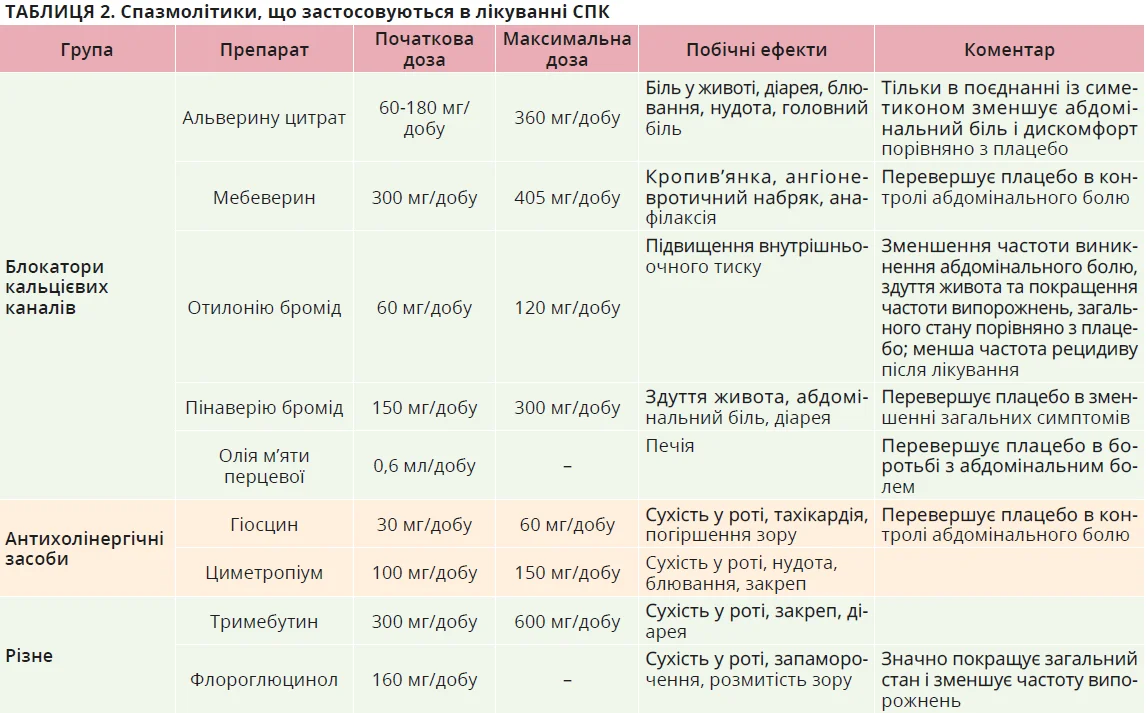
Спазмолітики є одними з найзастосовуваніших препаратів для лікування СПК; зазвичай їх поділяють на антимускаринові засоби (отилоній, гіосцин, циметропіум, дицикломін) і міорелаксанти (альверин, мебеверин, пінаверій, дротаверин, тримебутин, роциверин). Ці препарати розслаблюють гладкі м’язи кишківника та зменшують гіперчутливість внутрішніх органів, потенційно зменшуючи такі симптоми СПК, як біль у животі [137]. У численних РКД доведено, що отилоній, пінаверій, гіосцин, циметропіум, дротаверин і дицикломін значно зменшують симптоми СПК порівняно з плацебо. Навпаки, альверин, мебеверин, тримебутин і роциверин не сприяють значному поліпшенню порівняно з плацебо. Дозування, побічні ефекти та застереження щодо застосування нині доступних спазмолітиків наведені в таблиці 2.
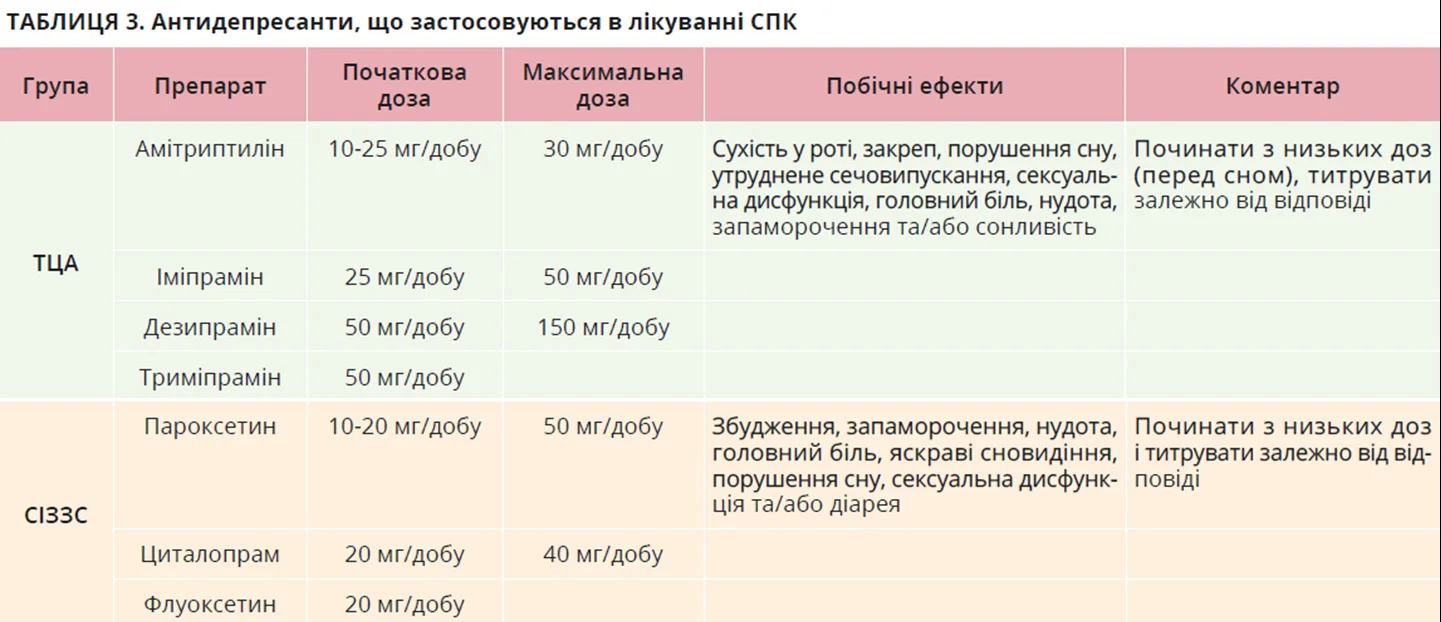
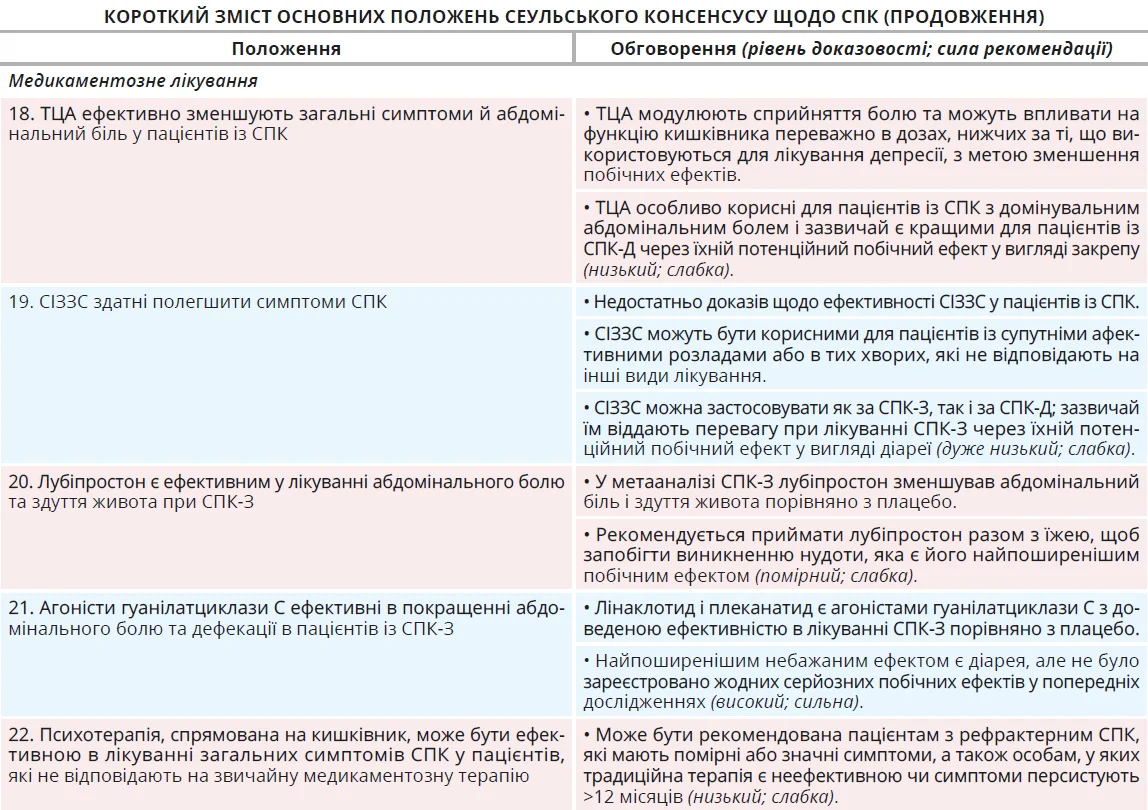
Доцільність застосування трициклічних антидепресантів (ТЦА) в лікуванні СПК підтверджено результатами декількох РКД та метааналізів [200-209]. ТЦА забезпечують симптоматичне полегшення при СПК за допомогою декількох механізмів. Вони чинять центральну аналгетичну дію, збільшуючи синаптичну концентрацію таких нейромедіаторів, як серотонін і норадреналін, які беруть участь у модуляції болю та регуляції настрою [210]. ТЦА мають антихолінергічні властивості, які допомагають зменшити ГІ-спазми, що сприяє полегшенню абдомінального болю [211]. Їхній вплив на моторику кишківника є складним і не повністю зрозумілим, але ТЦА здатні нормалізувати роботу кишківника, сповільнюючи ГІ-транзит, що може бути особливо корисно при діареї.
Такі селективні інгібітори зворотного захоплення серотоніну (СІЗЗС), як циталопрам, флуоксетин і пароксетин, підвищують біодоступність серотоніну в тканинах, зменшуючи його зворотне захоплення епітеліальними клітинами, посилюючи тим самим прокінетичний і просекреторний ефекти серотоніну. Метааналіз 7 РКД (n=356) довів, що СІЗЗС перевершують плацебо в нівелюванні загальних симптомів СПК чи абдомінального болю [200]. Зазвичай СІЗЗС краще переносяться, ніж ТЦА, та мають менше побічних ефектів, а ймовірність виникнення серйозних побічних ефектів є мінімальною. Зважаючи на кращу переносимість і меншу кількість побічних дій порівняно з ТЦА, СІЗЗС можуть бути кращим варіантом для пацієнтів, які не відповідають на ТЦА. Дозування, побічні ефекти та застереження щодо застосування наявних на цей час антидепресантів наведені в таблиці 3.
Література
Choi Y., et al. 2025 Seoul Consensus on Clinical Practice Guidelines for Irritable Bowel Syndrome. J. Neurogastroenterol. Motil. 2025; 31 (2): 133-169. doi: 10.5056/jnm25007.