Підходи до корекції відсутності скорочень стравоходу: чи можемо ми зробити краще?
Переклала й адаптувала канд. мед. наук Тетяна Можина
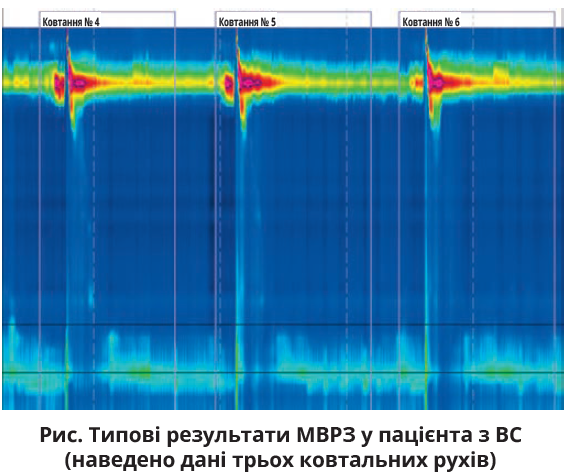
За Чиказькою класифікацією, відсутність скорочень (ВС) стравоходу є основним порушенням його моторної функції, котру визначають як повну ВС поряд із нормальним розслабленням нижнього стравохідного сфінктера (НСС) та інтегральним тиском розслаблення (ІТР) (рис.) [1, 2]. Діагноз ВС ґрунтується на результатах манометрії з високою роздільною здатністю (МВРЗ).
Ахалазія 1-го типу являє собою інший розлад, який також характеризується ВС стравоходу та може імітувати ВС [2]. Ахалазії 1-го типу притаманне порушення розслаблення НСС, саме ця ознака дає змогу відрізнити її від ВС; зазначені два різні стани можуть мати спільні клінічні прояви та результати манометрії. Проведення додаткових досліджень (ковтання барію, застосування технології EndoFLIP) може бути необхідним для встановлення правильного діагнозу, якщо при МВРЗ отримано пограничні значення [2]. У пацієнтів із ВС спостерігають втрату перистальтичного резерву при багаторазовому швидкому ковтанні під час МВРЗ [3].
ВС асоціюється з іншими хворобами та станами. ВС може бути ідіопатичною, а також виникати при патології сполучної тканини, ревматологічних/автоімунних захворюваннях (склеродермія), нервово-м’язових розладах (розсіяний склероз, м’язова дистрофія), цукровому діабеті 1-го типу, після променевої терапії, при довгосегментному стравоході Барретта чи тяжкому рефлюкс-езофагіті (ступінь D за Лос-Анджелеською класифікацією), прийомі деяких ліків (стероїди, опіати, антихолінергічні засоби, імунодепресанти), після перенесених інфекцій (поліомієліт, хвороба Шаґаса, інфекційний мононуклеоз, вірус імунодефіциту людини) та хірургічних процедур (міотомія за Геллером, пероральна ендоскопічна міотомія) [4] (табл. 1).
Пацієнти з ВС часто страждають на гастроезофагеальну рефлюксну хворобу (ГЕРХ). Ерозивний езофагіт (ЕЕ) є поширеним явищем у разі ВС і спостерігається в 65% хворих на склеродермію з ВС і супутнім ураженням стравоходу [6]. Потенційні симптоми рефлюксу, притаманні тяжкому ЕЕ, ВС, стриктурі та кандидозу стравоходу, синдрому Барретта, аспірації чужорідного тіла, раку стравоходу й мальнутриції, здатні негативно впливати на якість життя [6, 7]. У цьому огляді наведено сучасні терапевтичні підходи до лікування ВС і його ускладнень з акцентом на терапію ГЕРХ, нутритивну підтримку та потенційну роль ендоскопічних/хірургічних утручань.
Лікування ГЕРХ та ЕЕ в пацієнтів із ВС
Основою лікування ГЕРХ у хворих із ВС є інгібітори протонної помпи (ІПП), але питання щодо стандартної рекомендованої дози ІПП, їхньої довгострокової ефективності, необхідності комбінованої терапії потребують подальшого вивчення [13]. У літературі відсутні спеціальні дослідження, проведені за участю пацієнтів із ВС. Hendel і співавт. продемонстрували добру ефективність омепразолу в контролюванні симптомів ГЕРХ і зменшенні тяжкості ЕЕ у хворих на склеродермію. Однак повне загоєння ЕЕ не досягнуто в 50% випадків, оскільки рефлюкс продовжував існувати одночасно з основним розладом моторики [30]. В одному дослідженні доведено, що лансопразол (30 мг) ефективно контролює симптоми ГЕРХ протягом 6 місяців у хворих на склеродермію; проте цей ефект не зберігався через 6 місяців [31]. Muro та співавт. вивчали ефективність рабепразолу (10 мг) при склеродермії у хворих на ГЕРХ і ЕЕ за допомогою валідованого опитувальника та встановили, що рабепразол достовірно зменшує виразність симптомів ГЕРХ через 4 і 8 тижнів лікування [32].
У клінічній практиці часто використовується подвійна доза ІПП для контролю симптомів ГЕРХ та ЕЕ, хоча доказів на користь такого підходу небагато [33-36].
Калій-конкурентні блокатори секреції соляної кислоти (К-КБК) діють шляхом інгібування шлункової воднево-калієвої АТФази. До цього класу відносять фексупразан, кеверпразан, ревапразан, тегопразан і вонопразан; інші представники групи К-КБК (лінапразан, застапразан) перебувають на стадії розроблення. Нині вонопразан є найвідомішим і найвивченішим препаратом із групи К-КБК [37]. Це пероральний К-КБК, схвалений для лікування ЕЕ. Вонопразан визнаний ефективним у лікуванні ЕЕ та зіставним із лансопразолом за результативністю [37]. В аналізах post hoc пацієнти з тяжким езофагітом (ступінь C або D за Лос-Анджелеською класифікацією) мали кращі результати при прийомі вонопразану, ніж у разі застосування лансопразолу.
Ефективність комбінованої терапії рідко аналізується у хворих на склеродермію та ГЕРХ. У дослідженні Foocharoen і співавт. узяли участь 148 хворих на склеродермією та ГЕРХ, які частково відповідали на терапію ІПП [39]. Автори порівнювали комбінацію ІПП з домперидоном або альгіновою кислотою; вони дійшли висновку, що комбінована терапія є ефективною в більшості випадків. Однак у 20% пацієнтів не спостерігали жодного покращення [39]. Сукральфат, який складається із сульфату сахарози та гідроксиду алюмінію, часто використовують як додаткову терапію для контролю рефлексу й ЕЕ. Один метааналіз, у якому спостерігали за хворими на ГЕРХ та ЕЕ (43 статті, 7635 пацієнтів), довів, що загальна частота одужання при застосуванні сукральфату становить 39,2±22,4% (95% довірчий інтервал 3,6-74,8%) [40].
Утворення пептичних стриктур стравоходу є значним ускладненням хронічної ГЕРХ, яке посилює симптоми дисфагії. Застосування ІПП знижує частоту виникнення стриктур стравоходу. При виявленні пептичної стриктури доцільно призначати ІПП та проводити ендоскопічну дилатацію [41].
Отже, ГЕРХ та ЕЕ є дуже поширеними в пацієнтів із ВС, а ІПП залишаються наріжним каменем лікування цих пацієнтів.
Прокінетики в пацієнтів із ВС
Існує обмежена кількість доказів доцільності застосування прокінетиків у пацієнтів із ВС. Більша частина сучасних знань щодо ефективності прокінетиків в осіб із патологією стравоходу походить із досліджень, проведених за участю пацієнтів, результати манометрії яких відрізнялися від ВС. Тому в цьому огляді ми лише припускаємо їхню потенційну ефективність у разі ВС. Хоча прокінетики здатні забезпечити певне полегшення симптомів за легких стадій неврологічних/міопатичних порушень, на пізніх стадіях, які характеризуються розвитком фіброзу (що притаманно ВС), прокінетична терапія є неефективною в покращенні моторики стравоходу [42, 43].
Прокінетики являють собою різноманітну групу препаратів, які впливають на нейромедіатори, що відповідають за скоротливість гладких м’язів; до них належать антагоністи допаміну (метоклопрамід, домперидон), антагоністи серотоніну (буспірон, прукалоприд, мосаприд) і агоністи рецепторів мотиліну (еритроміцин) [44]. Прокінетики позитивно впливають на НСС і перистальтику стравоходу, збільшуючи амплітуду його скорочень. Однак більшість із цих засобів мають високий ризик виникнення побічних ефектів, особливо при тривалому застосуванні, в тому числі серйозних, включаючи зупинку серця й екстрапірамідні симптоми. Тому більшість наявних доказів отримані в короткострокових клінічних дослідженнях із невеликою кількістю пацієнтів і низькою якістю доказів.
У здорових добровольців антагоністи допамінових рецепторів-2 збільшують скорочення стравоходу (метоклопрамід) і покращують базальний тонус НСС (домперидон, метоклопрамід). Незважаючи на це, вони не змогли покращити моторику тіла стравоходу в рандомізованому подвійному сліпому плацебо-контрольованому дослідженні в пацієнтів з ЕЕ [45].
Серотонінергічні засоби є прокінетичними препаратами, які покращують моторику стравоходу, впливаючи на пресинаптичні 5-HT1A-рецептори (буспірон) або на постсинаптичні 5-HT4-рецептори (прукалоприд, ітоприд, мосаприд), що забезпечує підвищення вивільнення ацетилхоліну з кишкових нервів, стимулювання перистальтики стравоходу завдяки активності мускаринових рецепторів. Прукалоприд покращує швидкість випорожнення шлунка в здорових осіб, посилює перистальтику та зменшує час впливу шлункової кислоти на слизову стравоходу в осіб із ГЕРХ і вповільненою моторикою стравоходу [46]. Агоніст мотиліну, макролідний антибіотик еритроміцин здатний активувати мотилінові рецептори на гладком’язових волокнах. Внутрішньовенне введення еритроміцину хворим на цукровий діабет із гіпомоторикою стравоходу сприяло збільшенню часу стравохідного транзиту (за даними езофагогастральної сцинтиграфії) та покращенню скорочень стравоходу [47, 48]. Прийом цього препарату пов’язаний із ризиком розвитку серйозних серцевих побічних ефектів (подовження інтервалу QT), швидкої тахіфілаксії, що робить непридатним його тривале застосування.
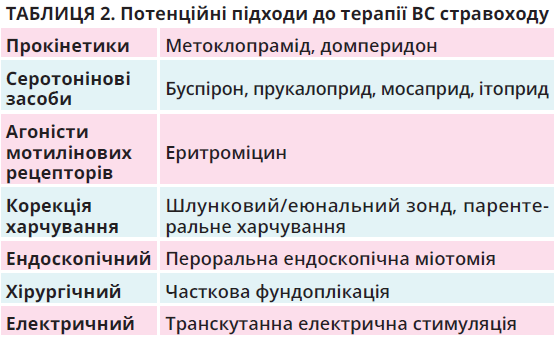
Отже, ефективність прокінетиків здебільшого вивчали в короткотривалих дослідженнях за участю невеликої кількості пацієнтів зі зниженням скоротливості стравоходу. Жоден із досліджуваних препаратів не сприяв покращенню показників манометрії, нівелюванню симптомів із боку верхніх відділів шлунково-кишкового тракту в пацієнтів
із ВС порівняно з плацебо (табл. 2).
Корекція харчування
Пацієнти з порушеннями моторики стравоходу можуть страждати від дисфагії, що ускладнює адекватне споживання калорій і білків. Нездатність макро- та мікроелементів дістатися шлунка здатна призвести до недоїдання [56]. Нутритивна підтримка важлива для покращення результатів лікування ВС і підтримання росту в дітей [56, 57]. Усіх пацієнтів із позитивними результатами скринінгу нутритивної недостатності рекомендується направити до кваліфікованого дієтолога/нутриціолога [56, 58], який має розробити дієту, збалансовану за рідиною, білками, жирами та вуглеводами відповідно до віку, ваги й індивідуальних особливостей пацієнта [57].
Загалом ентеральне харчування перевершує парентеральне, оскільки воно дає змогу зберегти функцію кишківника, архітектуру слизової оболонки, кишково-асоційовану лімфоїдну тканину та кишкову мікробіоту, знизити вартість і тривалість перебування в стаціонарі, зменшити кількість інфекційних ускладнень [57]. Якщо пероральний прийом їжі не переноситься, ентеральне харчування треба здійснювати через назогастральний зонд, що знижує ризик аспірації [56]. У пацієнтів із тяжким порушенням гастроінтестинальної моторики / протипоказаннями до ентерального харчування парентеральне харчування є ефективним методом лікування рефрактерної мальнутриції.
Ендоскопічне, хірургічне та транскутанне лікування
Пацієнти з ВС часто мають симптоми рефлюксу/дисфагії [28, 60]. Нещодавнє дослідження показало, що хворі з рефлюксом мають нижчий ІТР, що підтверджує його здатність спричиняти рефлюкс шлункового вмісту в стравохід [60]. З іншого боку, пацієнтам із домінувальною дисфагією притаманний вищий ІТР (хоча він усе-таки перебуває в межах норми), що зумовлює застрявання їжі в стравохідно-шлунковому переході. Ці відмінності в ІТР свідчать про те, що втручання на стравохідно-шлунковому з’єднанні (міотомія в пацієнтів із дисфагією та відносно високим внутрішньочеревним тиском або фундоплікація в пацієнтів із рефлюксом і низьким ІТР) може мати фізіологічне підґрунтя для віднесення таких пацієнтів до ВС [60].
Висновки
Нещодавні дослідження покращили наше розуміння ВС, розладу моторики стравоходу, який часто недооцінюють. Однак досі бракує якісних доказів щодо ефективності лікування, основою якої залишаються агресивна терапія ІПП для нівелювання ознак рефлюксу й ЕЕ, дієтотерапія та модифікація способу життя. Інші препарати, як-от прокінетики, мають невелику доказову базу на підтримку їх використання. Існує обмежена кількість досліджень, у яких продемонстровано ефективність таких втручань, як фундоплікація, в лікуванні ВС. Проведення проспективних клінічних досліджень, у яких вивчатиметься ефективність зазначених способів лікування, безумовно, є виправданим.
Література
Mari A., et al. Approach to esophageal absent contractility: can we do better? Ann. Gastroenterol. 2024. doi: 10.20524/aog.2024.0860.