Основні форми стеатотичної хвороби печінки в клінічних прикладах: час замислитися, змінюватися та діяти
Автор: Олександра Юріївна ФІЛІППОВА, доктор медичних наук, професор, кафедра внутрішньої медицини 2, фтизіатрії, професійних хвороб і клінічної імунології, Дніпровський державний медичний університет
 Минулого року на Міжнародному гепатологічному конгресі Європейської асоціації з вивчення захворювань печінки (EASL), який відбувся у Відні 21-24 червня, прийнято нову класифікацію та номенклатуру жирової хвороби печінки, представлено положення Делфі-консенсусу. Згідно із сучасними уявленнями нині замість термінів «неалкогольна жирова хвороба печінки» (НАЖХП) і «неалкогольний стеатогепатит» (НАСГ) слід використовувати нові дефініції – «стеатотична хвороба печінки, пов’язана з метаболічною дисфункцією» (СХПМД) і «стеатогепатит, пов’язаний із метаболічною дисфункцією» (СГМД) відповідно [7].
Минулого року на Міжнародному гепатологічному конгресі Європейської асоціації з вивчення захворювань печінки (EASL), який відбувся у Відні 21-24 червня, прийнято нову класифікацію та номенклатуру жирової хвороби печінки, представлено положення Делфі-консенсусу. Згідно із сучасними уявленнями нині замість термінів «неалкогольна жирова хвороба печінки» (НАЖХП) і «неалкогольний стеатогепатит» (НАСГ) слід використовувати нові дефініції – «стеатотична хвороба печінки, пов’язана з метаболічною дисфункцією» (СХПМД) і «стеатогепатит, пов’язаний із метаболічною дисфункцією» (СГМД) відповідно [7].
Експерти зауважують, що найпоширенішими причинами стеатотичної хвороби печінки (CХП) є СХПМД, алкоголь-асоційована хвороба печінки (АХП) та їх перекриття (МетАХП). СХПМД визначають як наявність стеатозу печінки в поєднанні з одним кардіометаболічним фактором ризику та відсутністю будь-якої іншої видимої причини ураження гепатоцитів [7]. Установлення діагнозу СХПМД не означає, що інші причини CХП не потрібно розглядати. Запроваджено також окрему категорію для пацієнтів із СХПМД та підвищеним споживанням алкоголю – МетАХП – для опису пацієнтів із СХПМД, які споживають більшу кількість алкоголю на тиждень (140 г/тиж для жінок і 210 г/тиж для чоловіків) [7].
Основною метаболічною дисфункцією, що лежить в основі СХПМД, є резистентність до інсуліну, а обрані метаболічні фактори ризику неоднаково прогнозують резистентність до інсуліну. Резистентність до інсуліну та стеатоз можуть бути наявними за відсутності будь-яких кардіометаболічних факторів ризику, особливо в молодих пацієнтів [7]. Установлювати діагноз СХПМД рекомендують на підставі виявлення щонайменше одного з 5 кардіометаболічних критеріїв:
- індекс маси тіла (ІМТ) ≥25 кг/м2 (для осіб азійського походження – 23 кг/м2) чи окружність талії >94 см у чоловіків і >80 см у жінок або з урахуванням етнічної приналежності;
- рівень глюкози в сироватці крові натще ≥5,6 ммоль/л, або рівень глюкози через 2 години після навантаження ≥7,8 ммоль/л, або глікозильований гемоглобін (HbA1c) ≥5,7%, або цукровий діабет (ЦД) 2-го типу, або лікування ЦД 2-го типу;
- артеріальний тиск (АТ) ≥130/85 мм рт. ст. або специфічне антигіпертензивне лікування;
- тригліцериди (ТГ) у плазмі ≥1,7 ммоль/л або гіполіпідемічна терапія;
- холестерин (ХС) ліпопротеїнів високої щільності (ЛПВЩ) у плазмі <1,0 ммоль/л у чоловіків і <1,3 ммоль/л у жінок або гіполіпідемічна терапія [7].
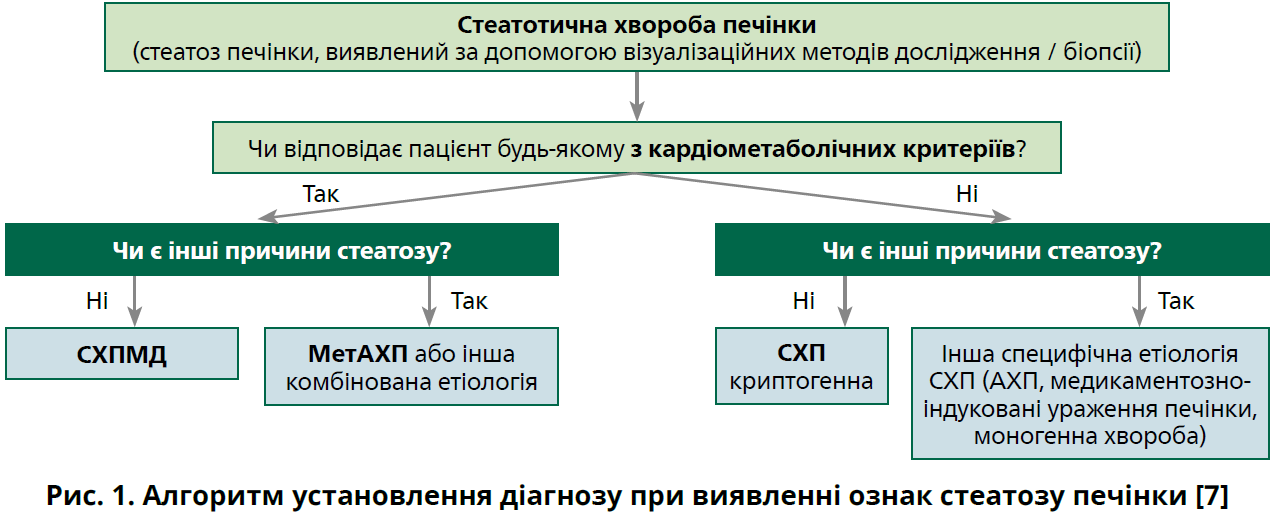
Експерти наводять діагностичний алгоритм у разі виявлення ознак стеатозу печінки за допомогою візуалізаційних методів досліджень або біопсії печінки (рис. 1).
Отримані знання лікар завжди використовує у своїй практичній діяльності, тому розглянемо кілька клінічних випадків саме з позицій оновлених уявлень щодо СХПМД.
Клінічний випадок № 1
Пацієнтка Є., 1980 р. н., звернулася зі скаргами на виражене здуття живота, тяжкість в епігастрії після прийому їжі, періодичний головний біль, підвищене потовиділення, постійну загальну слабкість, яка не зникала повністю після відпочинку. З анамнезу життя відомо, що пацієнтка має зайву вагу протягом останніх 6 років, припускає харчові навантаження, не дотримується будь-якої дієти та веде малорухливий спосіб життя; вживання алкоголю заперечує. Періодично відзначає підвищення АТ до 150/95 мм рт. ст. Під час об’єктивного дослідження підтверджено наявність надлишкової маси тіла: ІМТ – 28,3 кг/м2. Дані лабораторного обстеження продемонстрували відповідність печінкових проб нормативним значенням (білірубін – 16,2 ммоль/л, АЛТ – 31 од/л, АСТ – 26 од/л, лужна фосфатаза (ЛФ) – 74 од/л, гамма-глутамілтранс-пептидаза (ГГТП) – 34 од/л), виявлено ознаки дисліпідемії (загальний ХС – 5,6 ммоль/л, ТГ – 2,78 ммоль/л, ліпопротеїни низької щільності (ЛПНЩ) – 3,36 ммоль/л), а також прояви початкової інсулінорезистентності (HOMA-IR – 5,23 ммоль/л). Під час додаткового обстеження не виявлені маркери вірусних гепатитів В, С, антинуклеарні й антимітохондріальні антитіла. Ендо-
скопічне обстеження верхнього відділу шлунково-кишкового тракту виявило ознаки еритематозної гастродуоденопатії, уреазний тест негативний; пізніше отримано патогістологічний висновок щодо хронічного поверхневого активного (+) гастриту. Ультразвукове дослідження (УЗД) підтвердило наявність стеатозу печінки 1-го ступеня, виявило дифузну неоднорідність структури органа з підвищенням акустичної щільності та помірним дистальним згасанням звуку в VII сегменті; відзначено згладженість рельєфу печінкових вен (рис. 2). Електрокардіограма: частота серцевих скорочень – 78 уд./хв, ритм синусовий, електрична вісь серця горизонтальна.
Виконані стеатометрія й еластометрія, отримано такі результати: S0-S1 та F0 за шкалою METAVIR відповідно. На підставі виявлення інструментальних ознак стеатозу печінки та трьох кардіометаболічних критеріїв (ІМТ – 28,3 кг/м2, АТ – 160/95 мм рт. ст., ТГ – 2,78 ммоль/л), а також установлених змін на гастроскопії сформульовано клінічний діагноз: СХПМД; хронічний поверхневий активний гастрит, неасоційований із Нelicobacter pylori; артеріальна гіпертензія (АГ) І стадії, 2-го ступеня, ризик 2; серцева недостатність (СН) 0 ст. Пацієнтці надано рекомендації з модифікації способу життя, призначено препарати для лікування хронічного гастриту та корекції АТ: пантопразол 20 мг 2 р/добу, симетикон 80 мг 3 р/добу, ітоприду гідрохлорид 50 мг 3 р/добу, раміприл 5 мг 1 р/добу. Пацієнтка має також СХПМД. Ураховуючи наявність кардіометаболічних критеріїв, хвора потребує динамічного спостереження, контролю ІМТ, показників печінкового комплексу, ліпідного профілю, індексу HOMA-IR, контролю АТ. У разі прогресування захворювання необхідно розглянути питання щодо призначення препаратів із гепатотропними властивостями. Зважаючи на механізми розвитку СХПМД, де все-таки основним органом-мішенню є власне печінка, перспективним напрямом слід вважати корекцію функції гепатоцитів. У нашій клінічний практиці ми застосовуємо оригінальний адеметіонін з огляду на те, що при будь-яких захворюваннях печінки, навіть у разі стеатозу, зменшується синтез ендогенного адеметіоніну, що спричиняє прогресування захворювань печінки [6].
Клінічний випадок № 2
Пацієнт К., 1961 р. н., звернувся зі скаргами на загальну слабкість, швидку втомлюваність, головний біль, поганий настрій, здуття живота, гіркоту в роті.
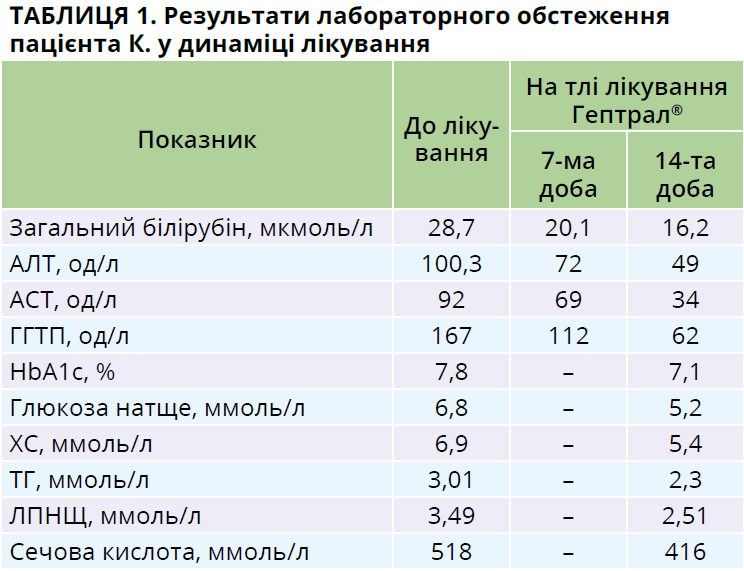
З анамнезу життя відомо, що протягом 13 років пацієнт страждає на ЦД 2-го типу (з приводу чого отримує метформін), гіпотиреоз, жовчнокам’яну хворобу, АГ, протягом 20 років має зайву вагу. Алкоголь не вживає. У ході об’єктивного дослідження діагностовано ожиріння: ІМТ – 37,1 кг/м2. При проведенні ініціального лабораторного обстеження виявлено біохімічні ознаки цитолізу, холестазу, дисліпідемії та зміни показників вуглеводного обміну (табл. 1). Під час додаткового обстеження не виявлені маркери вірусних гепатитів В, С, антинуклеарні й антимітохондріальні антитіла.
У ході УЗД діагностовано стеатоз печінки 3-го ступеня, дифузну неоднорідну грубозернисту структуру печінки з високою щільністю та значним дистальним згасанням звуку, значну згладженість судинного рисунка (рис. 3). При проведенні еластографії отримані показники відповідали F2 за шкалою METAVIR.
Додатково проведено оцінювання за шкалами Fibro Test (фіброз печінки) – F2, ActiTest (активність некрозапального процесу в печінці) – А3, SteatoTest (стеатоз печінки) – S3, NashTest (тяжкість НАСГ в інсулінорезистентних пацієнтів із надмірною масою тіла, діабетом або гіперліпідемією) – N2, Ash Test (діагностика алкогольного гепатиту) – Н0.
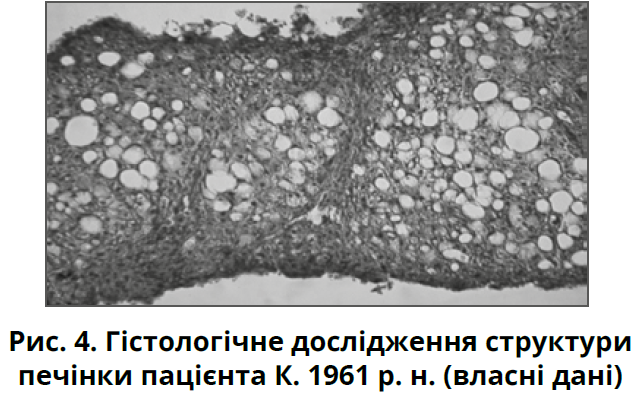
На підставі отриманих даних сформульовано клінічний діагноз: СГМД із мінімальною активністю; жовчнокам’яна хвороба, хронічний калькульозний холецистит у стадії нестійкої ремісії; ожиріння 2-го ступеня; АГ ІІ стадії, 2-го ступеня, ризик 3; ЦД 2-го типу, стадія субкомпенсації. Пацієнту дано рекомендації з модифікації способу життя, призначено Гептрал® у вигляді ступінчастої терапії (1000 мг/добу на 250 мл 0,9% розчину натрію хлориду внутрішньовенно крапельно протягом 14 днів із подальшим переходом на таблетовану форму 500 мг 3 р/добу протягом 3 місяців), Дуспаталін® 200 мг 2 р/добу, метформін 1000 мг/добу, периндоприл 8 мг/добу, аторвастатин 20 мг/добу. Надалі, під час лікування хворого в умовах хірургічного відділення з приводу жовчнокам’яної хвороби, було проведено лапароскопічну холецистектомію. Під час холецистектомії виконано інтраопераційну біопсію печінки з подальшим дослідженням її гістологічної структури. Встановлено ознаки макровезикулярного стеатозу 90% площі печінки (3-й ступінь), одиничні фіброзні септи в паренхімі печінки (рис. 4).
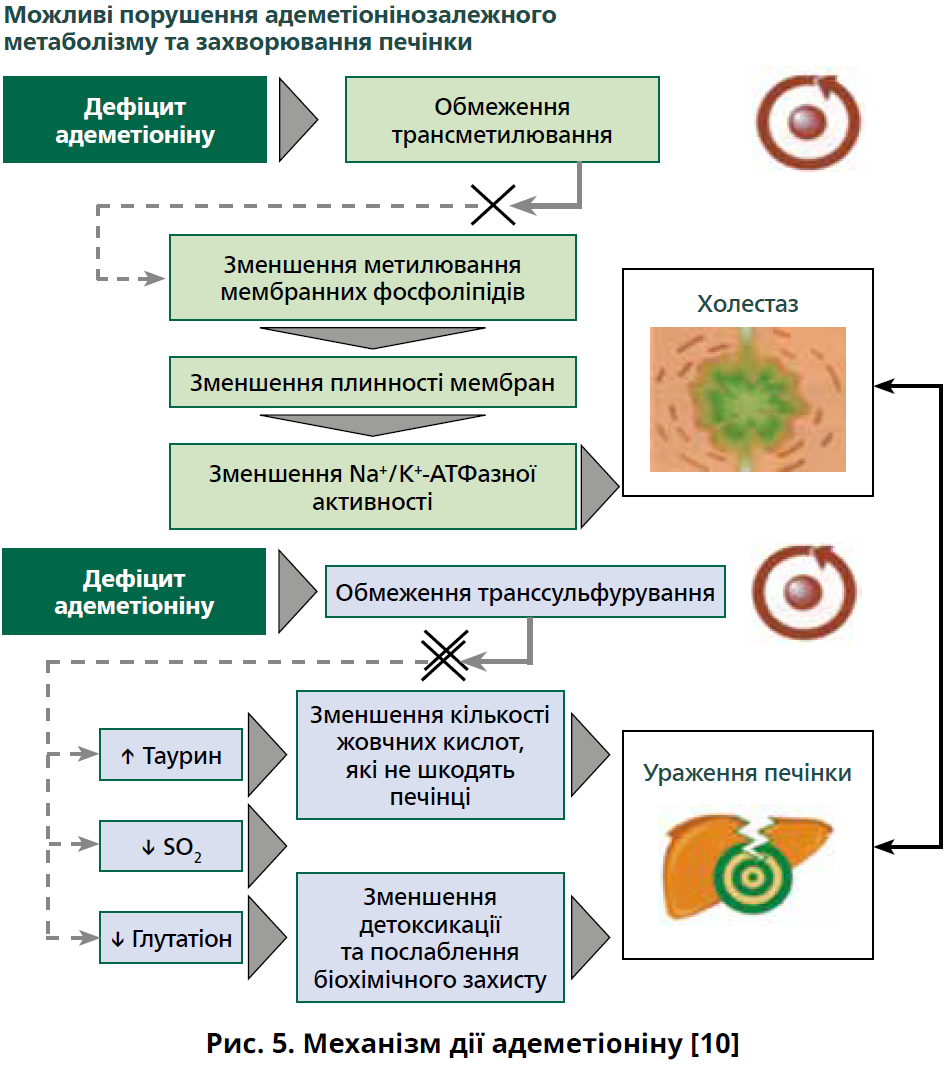
Введення SAMe дає змогу покращити процеси трансметилювання та транссульфурування, за рахунок чого зменшуються, відповідно, внутрішньопечінковий холестаз і показники цитолізу (рис. 5).
Ми спостерігали позитивну клінічну динаміку вже після перших 2 тижнів парентерального застосування Гептрал®: покращився суб’єктивний стан пацієнта, відзначено позитивну динаміку неспецифічної клінічної симптоматики та певних біохімічних показників (табл. 1), що супроводжувалося високою прихильністю хворого до терапії та дало змогу призначити оригінальний препарат SAMe (Гептрал®) на тривалий час (3 місяці).
Клінічний випадок № 3
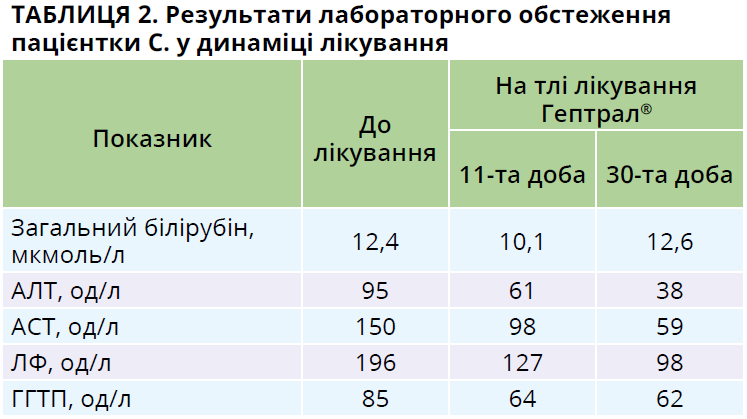
Пацієнтка С., 1977 р. н., звернулася зі скаргами на підвищення АТ до 180/110 мм рт. ст., ранкову нудоту, загальну слабкість, головний біль, хиткість, запаморочення. З анамнезу життя відомо, що підвищення АТ вперше зафіксовано у 2016 р., нині пацієнтка страждає на АГ І стадії, 2-го ступеня, СН 0, постійно приймає периндоприл. Спадковий характер АГ заперечує. Алкоголь не вживає. Під час об’єктивного огляду визначено ІМТ – 22,3 кг/м2, відзначені блідість шкіри та видимих слизових оболонок, приглушеність тонів серця, акцент ІІ тону над аортою, тахікардія (98 уд./хв), АТ – 125/70 мм рт. ст. (контрольована АГ на момент огляду), помірна болючість в епігастрії, незначна гепатомегалія. У клінічному аналізі крові звертали на себе увагу явища залізодефіцитної анемії (гемоглобін –
106 г/л, еритроцити – 3,62×1012/л, гематокрит – 31,5%, MCV – 87,1) на тлі незміненої лейкоцитарної формули, ШОЕ. Сироваткове залізо – 3,33 мкмоль/л. Виявлено біохімічні ознаки цитолізу, холестазу (табл. 2). Загальний ХС – 3,61 ммоль/л, інші показники ліпідного профілю на цьому етапі спостереження не досліджувалися. С-реактивний білок <6 мг/л, глюкоза – 4,93 ммоль/л (у межах норми), HbA1c – 5,0%. Зафіксовано зниження швидкості клубочкової фільтрації (ШКФ) за формулою CKD-EPI (70 мл/хв). У загальному аналізі сечі, аналізі сечі за Нечипоренко, а також у пробі Реберга патологічних змін не виявлено.
Під час УЗД органів черевної порожнини, нирок виявлено ехографічні ознаки дифузних змін печінки за типом стеатогепатозу, дисметаболічної нефропатії. УЗД щитоподібної залози структурних змін не виявило.
Електрокардіограма: частота серцевих скорочень – 70 уд./хв, ритм синусовий, електрична вісь серця горизонтальна. Проведено доплер-ехокардіографію: скорочувальна здатність міокарда задовільна, фракція викиду в нормі. Фіброз кореня аортального клапана та стулок мітрального клапана. Незначна недостатність стулок мітрального клапана, трикуспідального клапана. Порожнини серця не збільшені, тиск у легеневій артерії в межах норми.
Магнітно-резонансна томографія не виявила ознак вогнищевої та структурної патології головного мозку. Ретельне гінекологічне дослідження не виявило ознак специфічної патології, але тривалі менорагії, які відзначала пацієнтка, на думку гінеколога, могли призвести до виникнення залізодефіцитної анемії. Пацієнтка консультована додатковими спеціалістами: психіатром, неврологом, кардіологом, нефрологом, окулістом.
На підставі отриманих даних сформульовано клінічний діагноз: СХП, можливо, пов’язана з метаболічною дисфункцією; АГ І стадії, 2-го ступеня, ризик 2, СН 0 ст.; хронічна хвороба нирок ІІ ст. (ШКФ за формулою CKD-EPI – 70 мл/хв), гіпертонічна нефропатія, хронічна ниркова недостатність 0 ст.; менорагія; залізодефіцитна анемія середньої тяжкості, комбінованого ґенезу; астено-депресивний синдром.
На цьому етапі спостереження пацієнтка має нормальні показники ІМТ, глюкози сироватки крові, HbA1c, але скаржиться на підвищення АТ й отримує антигіпертензивну терапію. Пацієнтка потребує динамічного спостереження, дослідження всіх показників ліпідного профілю (ТГ, ХС ЛПВЩ). За відсутності явних кардіометаболічних критеріїв необхідно провести вторинне тестування на інсулінорезистентність, а також обов’язково виключити інші можливі причини стеатозу. Також необхідно контролювати сироваткове залізо та загальний аналіз крові.
З урахуванням цитолізу, холестазу хворій призначено препарат SAMe (таблетки Гептрал® 1500 мг/добу протягом 3 місяців), периндоприл 5 мг, амлодипін 5 мг зранку 1 р/день постійно, гідроксид заліза (III) фол 1 жувальна таблетка 3 р/добу, L-гліцин із вітамінами групи В 1 таблетка 2 р/добу.
Перспективним напрямом лікування СХПМД вважається корекція функцій гепатоцитів, тому в схемах комплексної терапії СХПМД можуть використовуватися препарати з антиоксидантною активністю
та гепатотропні засоби, які мають мембраностабілізуючі, протизапальні, антиапоптотичні й антифібротичні ефекти [3]. SAMe, на відміну від інших молекул, впливає не тільки на прояви запалення, але й на весь каскад кардіоваскулярних подій і діє на кожному етапі перебігу СХПМД: стеатозу, запалення, фіброзу та цирозу [10]. Одним із патогенетичних механізмів дії препарату є відновлення рівня ендогенного адеметіоніну, недостатність якого виникає на ранніх етапах розвитку хронічних захворювань печінки на тлі стеатозу, при розвитку стеатогепатиту, навіть за нормальних біохімічних показників та/або мінімального цитолізу, що дає змогу застосовувати SAMe як патогенетичну терапію різноманітної гепатологічної патології [6]. Доведено, що низький рівень SAMe призводить до зменшення співвідношення фосфатидилхолін/фосфатидилетаноламін, що спричиняє накопичення ТГ. Дефіцит SAMe також асоціюється з вивільненням прозапальних цитокінів, трансформацією стеатозу в стеатогепатит [6]. Порушення метаболізму адеметіоніну також здатне посилити ураження печінки, збільшити вірогідність розвитку фіброзу та гепатоцелюлярної карциноми. В експериментальних дослідженнях in vivo й in vitro доведено, що поліпшення метаболізму адеметіоніну та пов’язаних із ним ферментів/метаболітів здатне зменшити пошкодження печінки [4].
Зазначені властивості SAMe, а також призначене лікування АГ, залізодефіцитної анемії сприяли швидкому покращенню стану пацієнтки С.: уже на першому тижні лікування значно зменшилися загальна слабкість, головний біль. На 11-ту добу лікування відзначили позитивну динаміку печінкових проб (табл. 2), зменшення біохімічних показників цитолізу та холестазу. Через 2 тижні регулярного антигіпертензивного лікування встановилися нормальні показники АТ згідно з щоденником контролю АТ. Через 1 місяць після початку терапії пацієнтка C. скарг не пред’являла.
Висновки
СХП має декілька форм, найпоширенішими є СХПМД та СГМД. Комплексна терапія СХПМД припускає використання гепатотропних препаратів, які мають мембраностабілізуючі, протизапальні, антиапоптотичні й антифібротичні ефекти. Оптимальним гепатотропним препаратом можна вважати Гептрал®, що містить SAMe, аналогічний ендогенному [5, 12]. Застосування Гептрал® сприяє поліпшенню печінкових проб уже на 7-му добу лікування [1, 2, 8] з покращенням самопочуття, зниженням гепатогенної втоми при внутрішньопечінковому холестазі [2]. Адеметіоніну властивий дозозалежний ефект [11]. Застосування Гептрал® є зручним для лікарів і пацієнтів завдяки наявності різноманітних форм випуску, збереженню гепатотропного ефекту протягом 3 місяців після припинення прийому препарату [12], терапія Гептрал® сприяє зниженню смертності серед пацієнтів з алкогольним цирозом печінки [5]. Враховуючи механізм дії оригінального препарату SAMe, Гептрал® може бути призначений хворим на різні форми СХП, у тому числі СХПМД та СГМД.
Література
- Fiorelli G. S-adenosylmethionine in the treatment of intrahepatic cholestasis of chronic liver disease: a field trial. Current Therapeutic Research. 1999; 60 (6): 335-348. doi: 10.1016/S0011-393X(99)80010-1.
- Frezza M., Surrenti C., Manzillo G., Fiaccadori F., Bortolini M., Di Padova C. Oral S-adenosylmethionine in the symptomatic treatment of intrahepatic cholestasis. A double-blind,
placebo-controlled study. Gastroenterology. 1990 Jul; 99 (1): 211-5. doi: 10.1016/0016-5085(90)91250-a. - Huang J., Ou W., Wang M., Singh M., Liu Y., Liu S., Wu Y., Zhu Y., Kumar R., Lin S. MAFLD criteria guide the subtyping of patients with fatty liver disease. Risk Management and Healthcare Policy. 2021; 14: 491-501.
- Li Z., Wang F., Liang B., Su Y., Sun S., Xia S., Shao J., Zhang Z., Hong M., Zhang F., Zheng S. Methionine metabolism in chronic liver diseases: an update on molecular mechanism
and therapeutic implication. Signal Transduct. Target. Ther. 2020 Dec 4; 5 (1): 280. doi: 10.1038/s41392-020-00349-7. - Mato J.M., et al. S-adenosylmethionine in alcoholic liver cirrhosis: a randomized, placebo-controlled, double-blind, multicenter clinical trial. Journal of Hepatology. 1999; 30: 1081-1089.
- Noureddin M., Mato J.M., Lu S.C. Nonalcoholic fatty liver disease: update on pathogenesis, diagnosis, treatment and the role of S-adenosylmethionine. Exp. Biol. Med. (Maywood).
2015 Jun; 240 (6): 809-20. doi: 10.1177/1535370215579161. - Rinella M.E., Lazarus J.V., Ratziu V., et al. A multisociety Delphi consensus statement on new fatty liver disease nomenclature. Hepatology. 2023 Dec 1; 78 (6): 1966-1986. doi: 10.1097/HEP.0000000000000520.
- Santini D., Vincenzi B., Massacesi C., Picardi A., Gentilucci U.V., Esposito V., Liuzzi G., La Cesa A., Rocci L., Marcucci F., Montesarchio V., Groeger A.M., Bonsignori M., Tonini G. S-adenosylmethionine (AdoMet) supplementation for treatment of chemotherapy-induced liver injury. Anticancer Res. 2003 Nov-Dec; 23 (6D): 5173-9.
- Stable salts of S-adenosylmethionine and process for the preparation thereof. US8258115B2. Sep 4, 2012. Available at: https://patentimages.storage.googleapis.com/ac/e2/00/170391bdcc60f4/US8258115.pdf (last access: 23.10.2023).
- Virukalpattigopalratnam M.P., Singh T., Ravishankar A.C. Heptral (ademetionine) in patients with intrahepatic cholestasis in chronic liver disease due to non-alcoholic liver disease: results of a multicentre observational study in India. J. Indian Med. Assoc. 2013; 111: 856-859.
- Інструкція з медичного застосування лікарського препарату Гептрал® (адеметіонін) ліофілізат/таблетки.
- Міжнародний конгрес «ІІІ наукові читання пам’яті професора А.С. Свінціцького «Внутрішня медицина: наука та практика». 4-6 жовтня 2023 р.